Clear Sky Science · es
Reducción de la expresión de BIRC2 y BIRC3 asociada con mayor supervivencia en gliomas pediátricos de alto grado
Por qué los tumores cerebrales infantiles necesitan nuevas pistas
Los gliomas pediátricos de alto grado están entre los tumores cerebrales infantiles más letales, y la cirugía, la radiación y la quimioterapia actuales benefician solo a una minoría de los pacientes. Este estudio plantea una pregunta simple pero crucial: ¿existen “conmutadores de supervivencia” moleculares dentro de estos tumores que ayudan a las células cancerosas a resistir la muerte, y pueden esos conmutadores explicar por qué algunos niños viven más que otros?
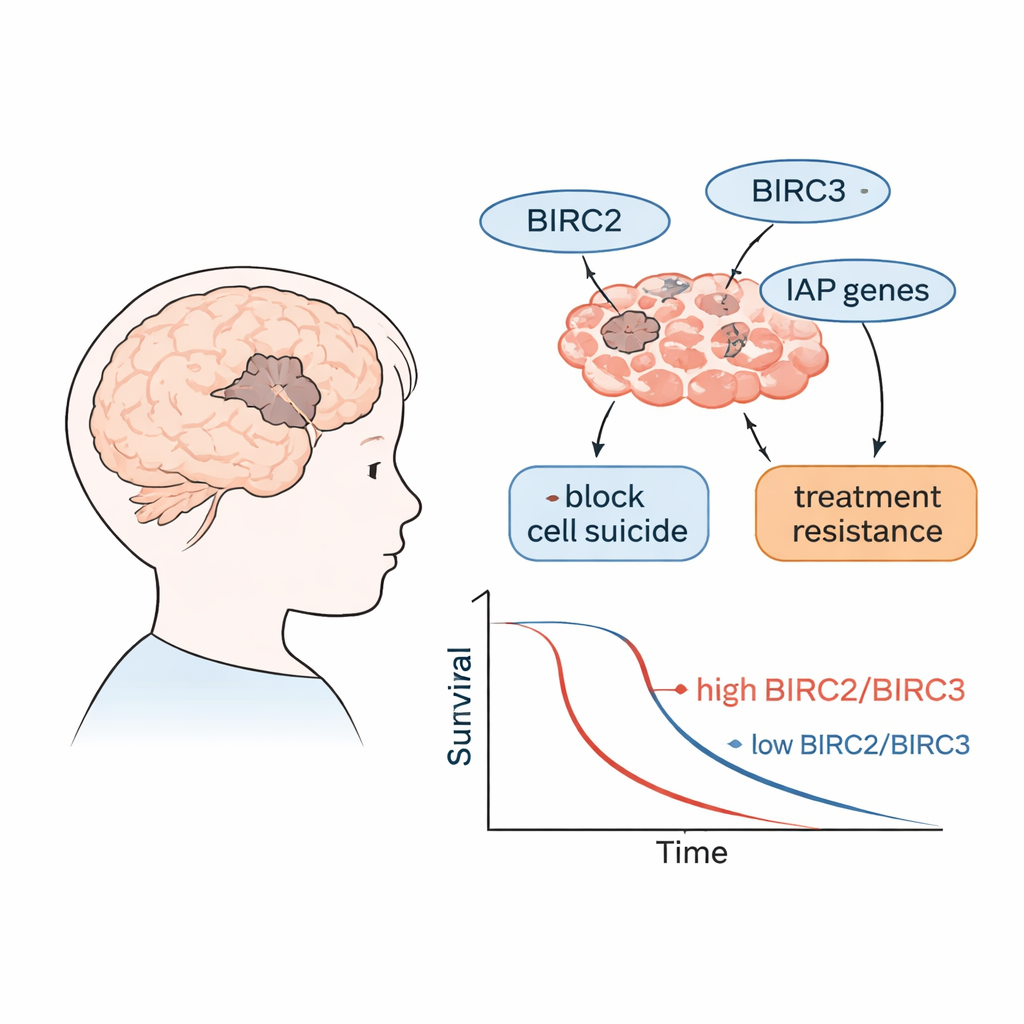
Proteínas que no dejan morir a las células cancerosas
Nuestras células disponen de un sistema de autodestrucción integrado, llamado muerte celular programada o apoptosis, que elimina células dañadas o peligrosas. Una familia de proteínas conocidas como IAPs (inhibidores de las proteínas apoptóticas) puede bloquear esta maquinaria de autodestrucción. Los genes que codifican estas proteínas se denominan genes BIRC. En muchos cánceres, las IAP están sobreactivadas, ayudando a las células tumorales a ignorar las señales de muerte y a continuar proliferando. Los investigadores se centraron en varios miembros de esta familia, incluidos BIRC2 y BIRC3, junto con genes relacionados que promueven u oponen la muerte celular, para evaluar su actividad en tumores cerebrales agresivos en niños.
Estudiando tumores reales de pacientes jóvenes
El equipo analizó muestras tumorales de 26 jóvenes, todos tratados en un centro pediátrico de neurooncología y diagnosticados con la forma más agresiva de glioma. Utilizando tejido preservado tomado durante la cirugía, midieron la actividad de múltiples genes vinculados a la supervivencia y muerte celular, como BIRC2, BIRC3, BIRC5, BIRC6, BIRC7, NAIP, XIAP, DIABLO, XAF1, CASP3 y CASP9. También compararon estas lecturas moleculares con características clínicas: cuánto tiempo vivió cada paciente, cuánto tiempo permaneció estable la enfermedad antes de empeorar, y la presencia de marcadores tumorales habituales como Ki‑67 (un indicador de proliferación), PD‑1 (un freno inmune), Olig2, p53, GFAP y un pequeño ARN regulador llamado miR‑155‑5p.
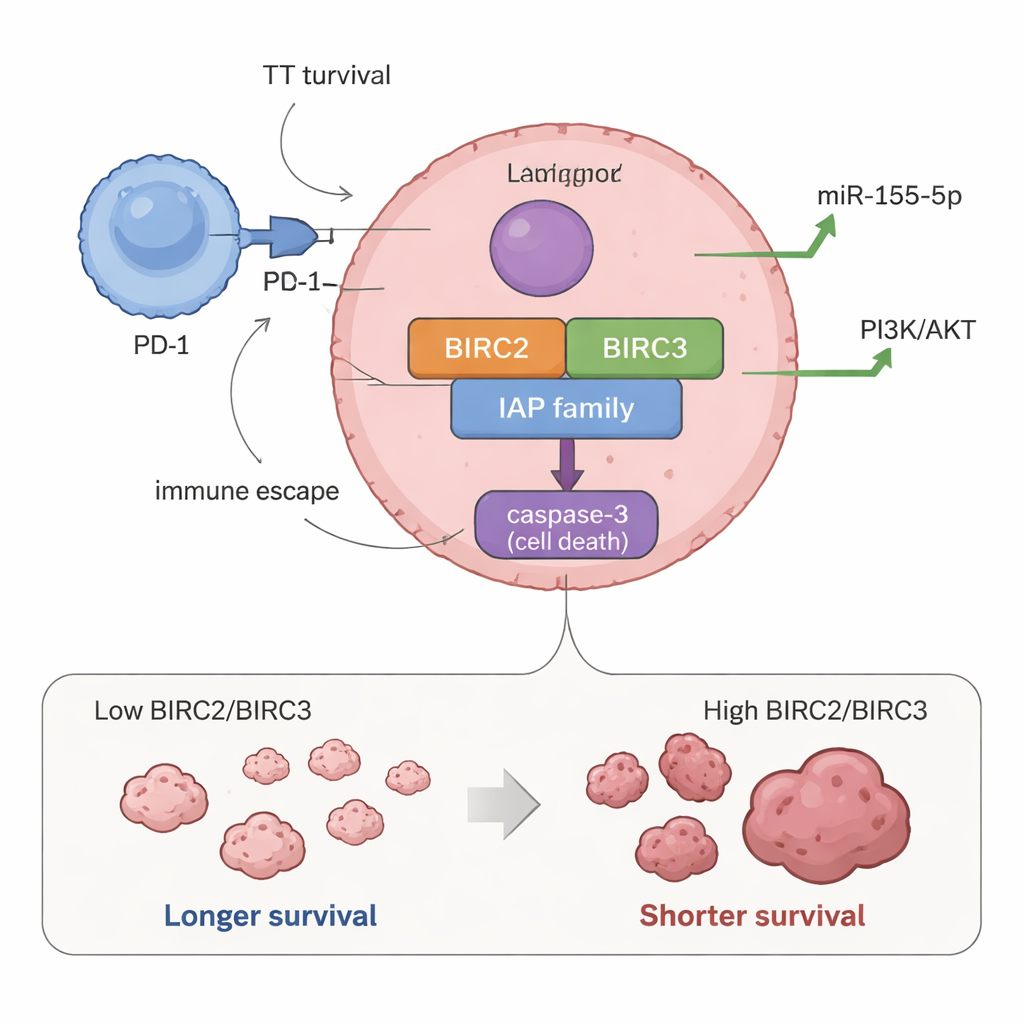
Conmutadores de supervivencia vinculados a vidas más cortas
Al comparar la actividad génica con los resultados de los pacientes, dos genes resaltaron. Los niños cuyos tumores mostraban niveles más altos de BIRC2 y BIRC3 tendieron a tener una supervivencia global más corta y periodos libres de progresión más breves. En otras palabras, cuando estos conmutadores de “no morir” estaban más activados, la enfermedad se comportaba de forma más agresiva. Los tumores con altos niveles de BIRC2 y BIRC3 también se asociaron con mayores niveles de miR‑155‑5p, un pequeño ARN que previamente se ha mostrado promotor del crecimiento celular y reductor de la muerte celular, lo que sugiere que estas moléculas pueden actuar en conjunto para reforzar la resistencia del tumor frente al tratamiento.
Vínculos con el crecimiento tumoral y la evasión inmune
El estudio también exploró cómo encajan estos conmutadores de supervivencia en el entorno tumoral más amplio. Sorprendentemente, algunos genes que pueden fomentar o regular la muerte celular, como NAIP, BIRC3 y XAF1, estaban más activos en tumores que carecían del marcador de proliferación Ki‑67, lo que apunta a un equilibrio complejo entre señales de crecimiento y de muerte. Niveles elevados de BIRC3 y XAF1 tendieron a aparecer en tumores con más PD‑1, un freno inmune clave que ayuda al cáncer a ocultarse de las defensas del organismo. Además, una mayor actividad de CASP3, un ejecutor central de la muerte celular, se asoció fuertemente con la expresión de PD‑1, lo que sugiere que las interacciones entre células cancerosas y células inmunitarias podrían remodelar cómo se utiliza o bloquea la maquinaria de muerte dentro del tumor.
Qué podría significar esto para tratamientos futuros
Para las familias y los clínicos que afrontan gliomas pediátricos de alto grado, estos hallazgos aún no cambian el tratamiento, pero ofrecen pistas importantes. El trabajo sugiere que la alta actividad del gen BIRC2 en particular, y posiblemente de BIRC3, identifica tumores más resistentes y con mayor probabilidad de recurrir rápidamente, lo que convierte a estos genes en potenciales señales de alerta de mal pronóstico. Dado que las proteínas IAP ya se están estudiando como dianas farmacológicas en cánceres adultos, los nuevos resultados permiten contemplar la posibilidad de que fármacos diseñados para apagar estos conmutadores de supervivencia puedan, en el futuro, combinarse con los tratamientos actuales de los tumores cerebrales o con inmunoterapias que apunten a PD‑1. El estudio es pequeño y exploratorio, por lo que sus conclusiones deben confirmarse en grupos más amplios y a nivel proteico, pero apunta hacia un futuro en el que el tumor de un niño podría perfilarse según estos conmutadores clave para predecir mejor el resultado y, eventualmente, orientar terapias más personalizadas y eficaces.
Cita: Petniak, A., Gil-Kulik, P., Zarychta, J. et al. Reduced expression of BIRC2 and BIRC3 associated with longer survival in pediatric high-grade gliomas. Sci Rep 16, 6665 (2026). https://doi.org/10.1038/s41598-026-35887-7
Palabras clave: tumor cerebral pediátrico, glioma, apoptosis, BIRC2 BIRC3, inmunoterapia