Clear Sky Science · es
KIN17 facilita la iniciación y progresión del tumor renal a través de la vía PI3K‑AKT‑mTOR
Por qué importa este estudio sobre cáncer de riñón
El cáncer de riñón se detecta con más frecuencia, pero para muchos pacientes la enfermedad sigue siendo difícil de controlar una vez que se disemina. Este estudio examina el problema a nivel microscópico —hasta el nivel de moléculas individuales dentro de las células cancerosas— para entender qué impulsa el crecimiento e invasión de los tumores renales y si un fármaco experimental puede frenar ese proceso. Los hallazgos señalan a una proteína poco conocida, KIN17, como un nuevo factor perjudicial en el cáncer renal y sugieren una forma de atacarla indirectamente con un tratamiento oral.
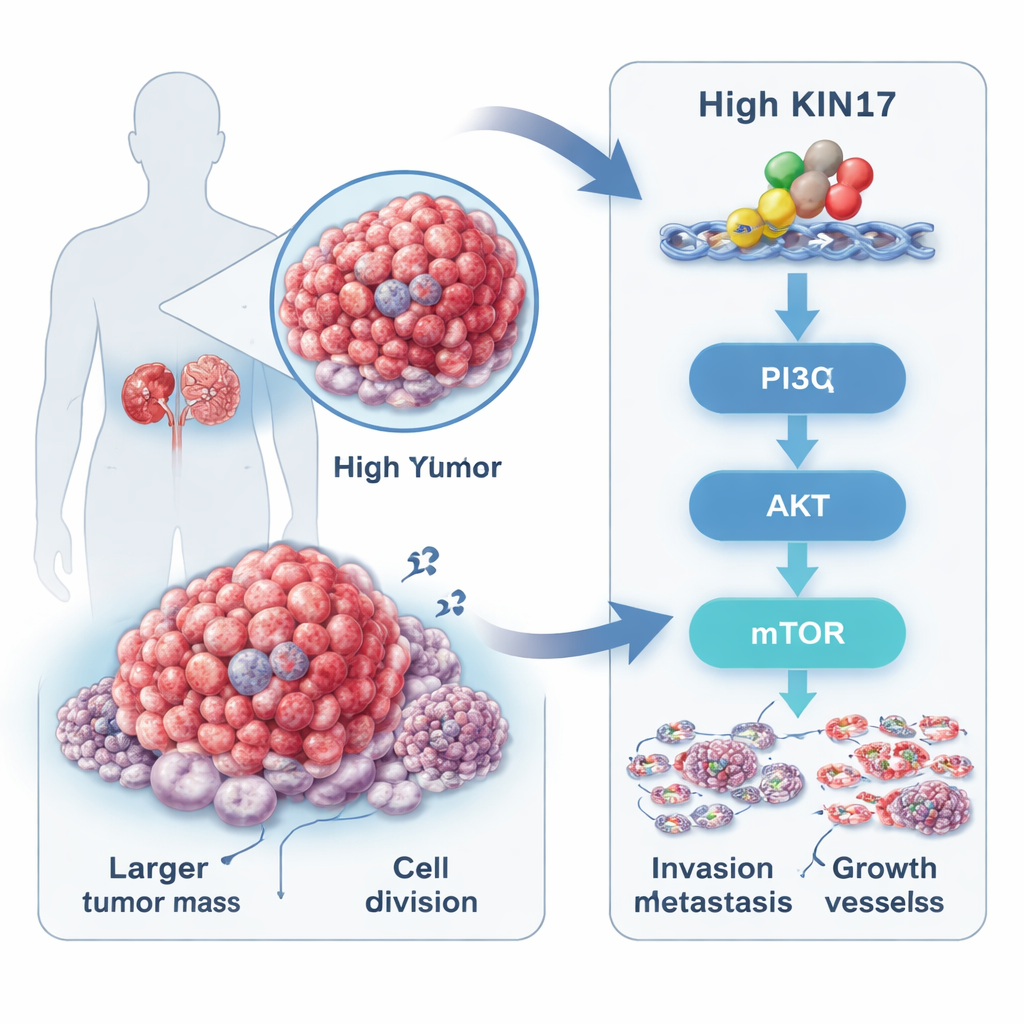
Un impulsor oculto dentro de los tumores renales
El carcinoma de células renales, la forma más común de cáncer de riñón, suele comenzar sin síntomas y con frecuencia se descubre tarde. Los investigadores se centraron en una proteína llamada KIN17, conocida desde hace tiempo por su papel en la protección y replicación del ADN, pero solo recientemente vinculada con varios otros cánceres. Al analizar bases de datos públicas de cáncer y muestras tumorales de 88 pacientes, hallaron que los niveles de KIN17 eran mucho más altos en los tumores renales que en el tejido no canceroso adyacente. Los pacientes cuyos tumores contenían más KIN17 tendían a tener cánceres de mayor tamaño, enfermedad de mayor grado, estadio más avanzado y más diseminación a distancia, y vivieron menos tiempo que quienes tenían baja expresión de KIN17. Este patrón sugiere que KIN17 no es solo un observador, sino que está estrechamente ligado a la agresividad del tumor.
Probando KIN17 en células cancerosas
Para averiguar qué hace realmente KIN17 dentro de las células de cáncer renal, el equipo modificó líneas celulares de laboratorio para reducir o aumentar su expresión. Cuando disminuyeron KIN17, las células crecían más despacio, formaban menos colonias y tenían menor capacidad de moverse e invadir a través de membranas artificiales. Más de estas células quedaban atrapadas en la fase de reposo del ciclo celular y morían en mayor proporción, mostrando niveles más altos de muerte celular programada. Ocurrió lo contrario cuando KIN17 se sobreexpresó: las células se multiplicaron más rápido, replicaron su ADN con mayor facilidad, cerraron más rápidamente huecos simulados en capas celulares y mostraron una invasión más agresiva. Estos experimentos demostraron que KIN17 actúa como un pedal de aceleración para el crecimiento y la diseminación de las células de cáncer renal.
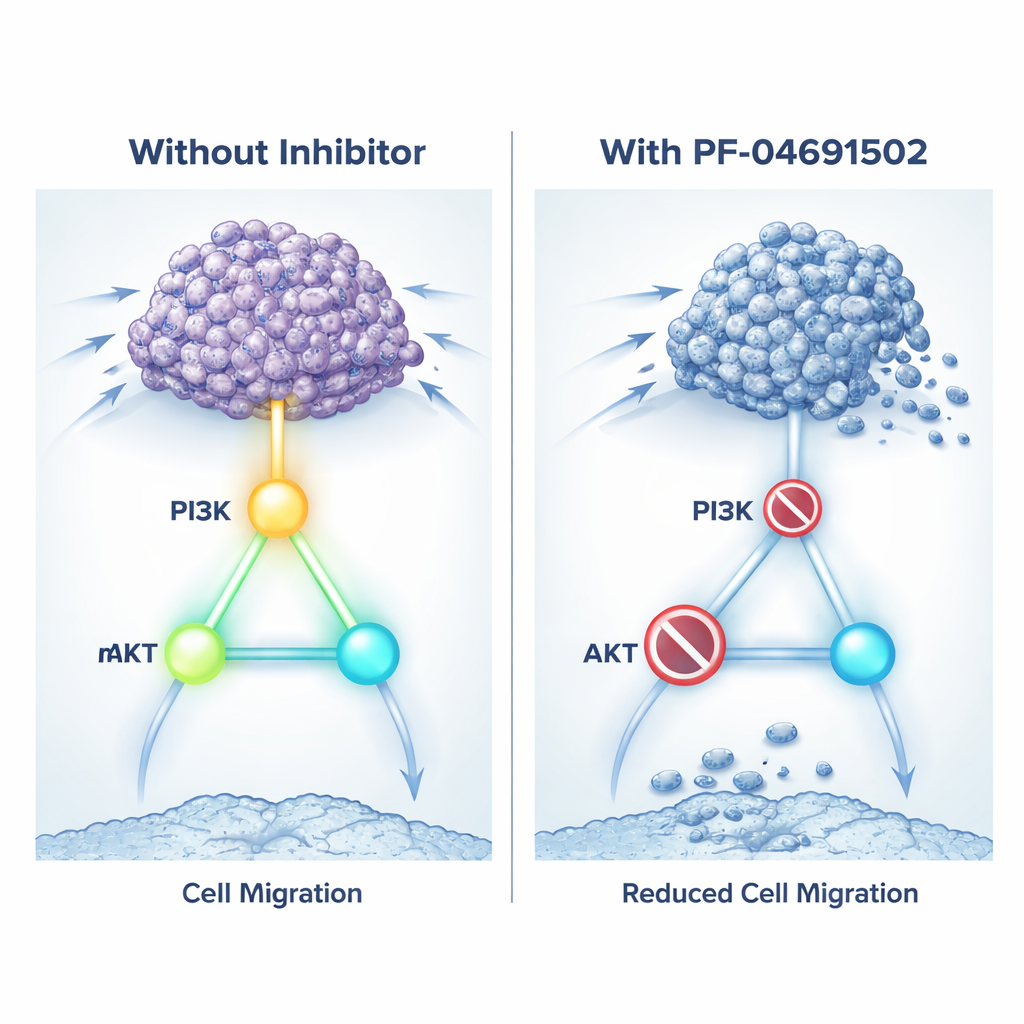
Una vía de crecimiento descubierta en acción
Los investigadores preguntaron a continuación cómo ejerce KIN17 este efecto. Sus estudios de actividad génica y pruebas proteicas apuntaron a una red conocida de crecimiento y supervivencia dentro de las células llamada vía PI3K–AKT–mTOR. A menudo se compara esta vía con un centro de control que indica a las células cuándo crecer, dividirse y evitar la muerte. Las células de cáncer renal con altos niveles de KIN17 mostraron señales de “encendido” más fuertes —marcas químicas llamadas fosfatos— en componentes clave de esta vía, aunque la cantidad total de esas proteínas no cambió. Cuando se redujo KIN17, esas marcas de activación disminuyeron y también cambiaron moléculas relacionadas con el movimiento y la invasión celular. En experimentos con ratones, los tumores formados por células ricas en KIN17 crecieron más y más rápido, y el tinción de los tejidos mostró que la misma vía de crecimiento estaba fuertemente activada en esos tumores.
Atenuar la señal con un fármaco de doble diana
Dado que bloquear directamente KIN17 no es aún posible con medicamentos existentes, el equipo probó una táctica diferente: apagar la vía de crecimiento que parece controlar. Usaron PF‑04691502, un fármaco experimental que inhibe tanto PI3K como mTOR, dos interruptores clave de la vía. En cultivos, tratar células de cáncer renal con alta expresión de KIN17 con este inhibidor ralentizó su crecimiento, redujo su capacidad de migrar y formar colonias, y aumentó la muerte celular. El fármaco también redujo las marcas de activación en PI3K, AKT y mTOR y disminuyó los niveles de proteínas relacionadas con la invasión. En ratones con tumores renales, dosis diarias de PF‑04691502 redujeron el tamaño de los tumores que sobreexpresaban KIN17 y disminuyeron los marcadores de división celular mientras aumentaban señales de muerte celular. En esencia, el fármaco pudo mitigar los efectos nocivos de KIN17 al silenciar su vía de crecimiento preferida.
Qué podría significar esto para los pacientes
Para las personas afectadas por cáncer de riñón, estos hallazgos sugieren dos ideas esperanzadoras. Primero, medir KIN17 en muestras tumorales podría ayudar a los médicos a evaluar cuán agresivo es un cáncer y su probabilidad de diseminarse. Segundo, los tumores que dependen en gran medida de KIN17 podrían ser particularmente vulnerables a fármacos que atacan la vía PI3K–AKT–mTOR, como PF‑04691502 o inhibidores de doble diana similares que ya están en ensayos clínicos para otros cánceres. Aunque queda mucho trabajo antes de que cualquier tratamiento nuevo llegue a la clínica, este estudio traza una cadena clara de acontecimientos —desde KIN17, a través de una vía de crecimiento clave, hasta la expansión tumoral descontrolada— y muestra que romper esa cadena puede frenar el cáncer renal en el laboratorio y en modelos animales.
Cita: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Palabras clave: carcinoma de células renales, KIN17, PI3K AKT mTOR, terapia dirigida, PF-04691502