Clear Sky Science · es
Aspectos comunes en los cambios de expresión génica y metilación en dos modelos de rata de epilepsia adquirida
Por qué importan los cambios génicos para las convulsiones
La epilepsia afecta a millones de personas y, en aproximadamente uno de cada tres casos, los fármacos actuales no controlan completamente las crisis. La mayoría de los medicamentos simplemente atenúan las tormentas eléctricas en el cerebro, pero no impiden que la epilepsia se desarrolle. Este estudio explora si las marcas químicas duraderas en el ADN y la forma en que los genes se activan o desactivan podrían explicar cómo un cerebro sano se vuelve epiléptico, y si esos cambios son comunes entre distintas formas de la enfermedad.
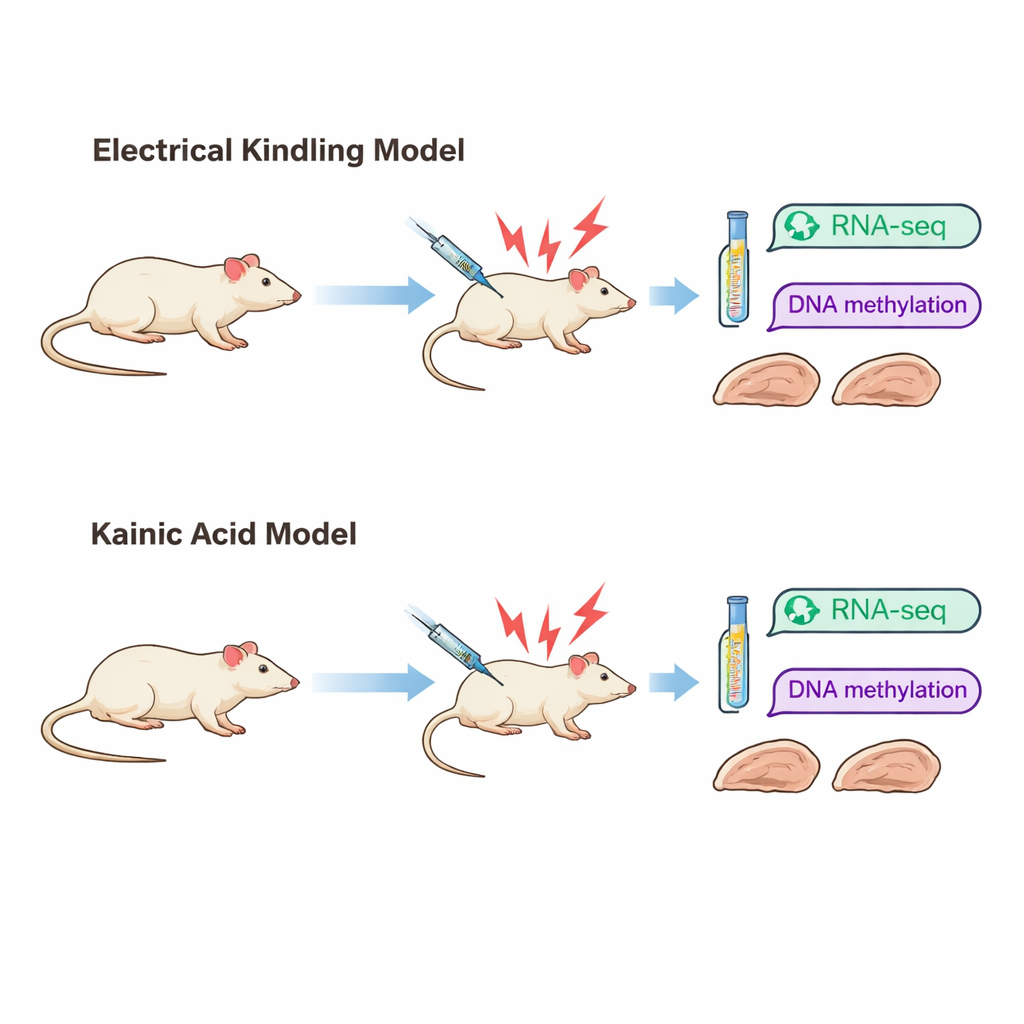
Dos caminos distintos hacia la misma enfermedad
Los investigadores se centraron en la epilepsia del lóbulo temporal, una forma común de la enfermedad que con frecuencia resiste al tratamiento. Usaron dos modelos bien establecidos en ratas que reproducen diferentes maneras en que puede surgir la epilepsia. En el modelo de “kindling” (sensibilización), se aplican pulsos eléctricos breves a una parte del hipocampo a lo largo del tiempo hasta que las convulsiones se vuelven fáciles de desencadenar. En el modelo de “ácido kainico”, un químico provoca un episodio intenso de convulsiones, tras el cual aparecen convulsiones espontáneas más adelante. Aunque ambos modelos producen finalmente un comportamiento externo similar —convulsiones convulsivas severas—, el daño cerebral que muestran es muy distinto. Las ratas sensibilizadas presentan una estructura tisular en gran medida conservada, mientras que las tratadas con ácido kainico muestran una pérdida celular pronunciada y cicatrización en regiones clave del hipocampo.
Leer la actividad genética del cerebro
Para ver cómo estos diferentes caminos hacia la epilepsia cambian el cerebro a nivel molecular, el equipo examinó el hipocampo después de que las ratas de cada modelo hubieran experimentado tres convulsiones severas. Midieron qué genes estaban más o menos activos mediante secuenciación de ARN y cartografiaron las marcas químicas llamadas grupos metilo en el ADN usando un método conocido como secuenciación de bisulfito de representación reducida. Los cambios en la actividad génica reflejan cómo las células responden y se adaptan, mientras que las marcas de metilación suelen considerarse una “memoria” a más largo plazo que puede influir en si los genes se activan o se silencian.
Los cambios en la actividad génica superan a las marcas de ADN
Los dos modelos produjeron patrones de actividad génica notablemente diferentes. El modelo de sensibilización mostró cambios en más de diez veces más genes que el modelo de ácido kainico. Sin embargo, cuando los investigadores solaparon las dos listas, aún encontraron más de cien genes que cambiaron en ambos modelos, y la mayoría lo hizo en la misma dirección. Un ejemplo es Mmp9, un gen relacionado con la remodelación de las conexiones neuronales y con el daño asociado a las convulsiones; se aumentó de forma intensa en ambos modelos. Estos cambios compartidos sugieren que existen respuestas génicas centrales a la epileptogénesis, incluso cuando el desencadenante inicial y la lesión cerebral visible difieren.
Las marcas de ADN cuentan otra historia
Al observar la metilación del ADN, el panorama cambió. Ambos modelos mostraron muchos genes con metilación alterada, y hubo una superposición considerable entre ellos. Sin embargo, solo un subconjunto modesto de genes mostró tanto metilación alterada como actividad alterada dentro del mismo modelo, y todavía menos se comportaron así en ambos modelos. En algunos de estos genes compartidos, como Nedd9 y Ptpre, la expresión aumentó en ambos modelos, pero la dirección del cambio de metilación del ADN en sitios individuales pudo ser opuesta entre los modelos. En conjunto, no hubo una regla simple de que “más metilación signifique menos actividad génica” o viceversa. Esto sugiere que, en estos modelos de epilepsia, la mayoría de los cambios en la actividad génica no están directamente impulsados por cambios generalizados en la metilación del ADN.
Qué significa esto para futuros tratamientos
Para quienes esperan mejores terapias contra la epilepsia, estos hallazgos ofrecen tanto cautela como orientación. El trabajo muestra que los programas génicos activados durante el desarrollo de la epilepsia pueden ser bastante específicos del modelo, y que la metilación del ADN es solo una parte de un panorama regulador más amplio y complejo. Los genes prometedores identificados en un solo modelo animal pueden no generalizarse, por lo que deberían probarse en múltiples modelos antes de avanzar hacia tratamientos humanos. Al mismo tiempo, el pequeño conjunto de genes que cambian tanto en expresión como en metilación entre modelos puede representar puntos de partida particularmente robustos para desarrollar terapias modificadoras de la enfermedad que no solo calmen las convulsiones, sino que prevengan que la epilepsia se instale.
Cita: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Palabras clave: epileptogénesis, metilación del ADN, expresión génica, epilepsia del lóbulo temporal, modelos en rata