Clear Sky Science · es
Respuestas bioenergéticas y migratorias celulares de fibroblastos gingivales humanos a la fotobiomodulación con láser de diodo de 940 nm
Luz que ayuda a sanar las heridas bucales
Cualquiera que se haya sometido a una extracción dental o a una cirugía de encías sabe lo incómodo que puede ser el proceso de cicatrización en la boca. Los tejidos están sometidos constantemente a tensión por la masticación, el habla y la presencia de bacterias, por lo que cualquier método que pueda acelerar la reparación de forma segura interesa tanto a dentistas como a pacientes. Este estudio investigó si un láser dental común, usado a muy baja potencia, puede “entrenar” suavemente a las células gingivales para que trabajen más y se desplacen más rápido mientras reconstruyen el tejido dañado, sin quemarlas ni dañarlas.
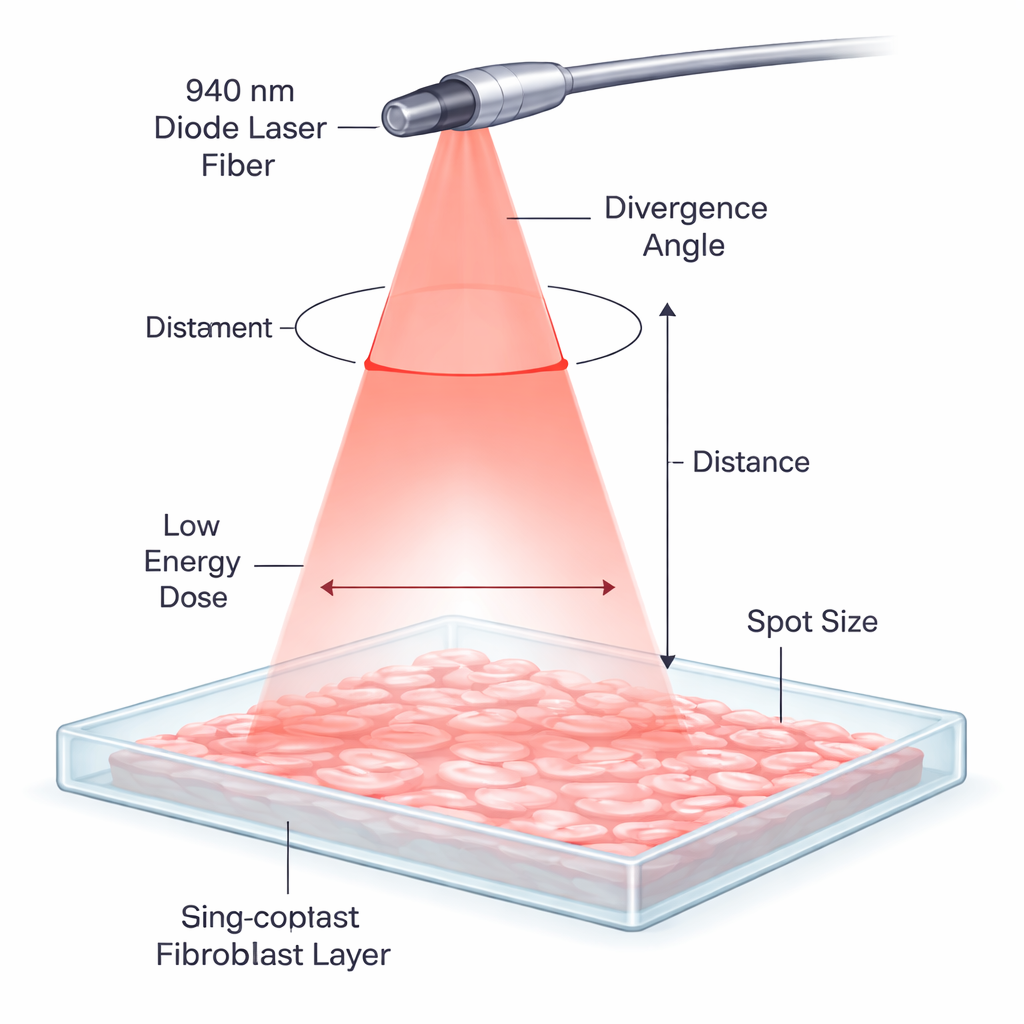
Cómo difiere un láser suave de un láser de corte
En muchas clínicas dentales, los diodos láser se utilizan rutinariamente para cortar o remodelar tejido blando generando calor. Aquí, el mismo tipo de láser de 940 nanómetros se atenuó y se empleó de forma muy distinta. En lugar de tocar y quemar el tejido, la luz se aplicó durante sólo un segundo desde una corta distancia, difundiéndose en un cono suave sobre una fina capa de células gingivales humanas cultivadas en placa. A estas dosis bajas, la intención no es cortar sino estimular la maquinaria interna de las células, un proceso conocido como fotobiomodulación, para que se reparen y se reorganicen con mayor eficiencia.
Evaluando la energía y la seguridad de las células gingivales
Los investigadores se centraron en los fibroblastos, las células principales responsables de producir las fibras y la matriz que dan resistencia al tejido gingival. Fibroblastos gingivales humanos de origen comercial se cultivaron en capas uniformes y se expusieron a tres dosis energéticas diferentes del láser de 940 nm, mientras que un cuarto grupo no recibió luz. El equipo midió varios marcadores: cuán metabólicamente activas estaban las células, si sus membranas externas resultaban dañadas, cuánto combustible celular (ATP) producían y si liberaban óxido nítrico, una molécula vinculada a la inflamación. En todas las dosis láser evaluadas, las células no mostraron signos de fuga ni lesiones y no activaron una señal inflamatoria, lo que indica que la breve exposición lumínica fue suave y biológicamente compatible bajo las condiciones probadas.
Más “combustible” celular y un punto óptimo para el movimiento
Aunque las células permanecieron saludables en todos los grupos, su producción de energía cambió de forma dependiente de la dosis y del tiempo. A niveles de luz moderados, los fibroblastos aumentaron la producción de ATP, la moneda energética universal de las células, hasta en aproximadamente una cuarta parte respecto a las células no tratadas después de 24 horas. Su actividad metabólica global también aumentó de forma moderada, especialmente en la dosis más alta. Para ver si esta energía adicional se traducía en un mejor comportamiento de reparación, los científicos crearon un “rasguño” recto en la capa celular y utilizaron imagen holográfica digital para observar la rapidez con que las células se desplazaban para cerrar la brecha. Encontraron que una dosis láser baja aumentó ligeramente la velocidad de migración y condujo al cierre más rápido, mientras que la dosis más alta ralentizó el movimiento y retrasó el cierre, aunque los niveles de energía seguían elevados. Este patrón, en el que una pequeña estimulación ayuda pero el exceso comienza a obstaculizar, se conoce como respuesta bifásica.
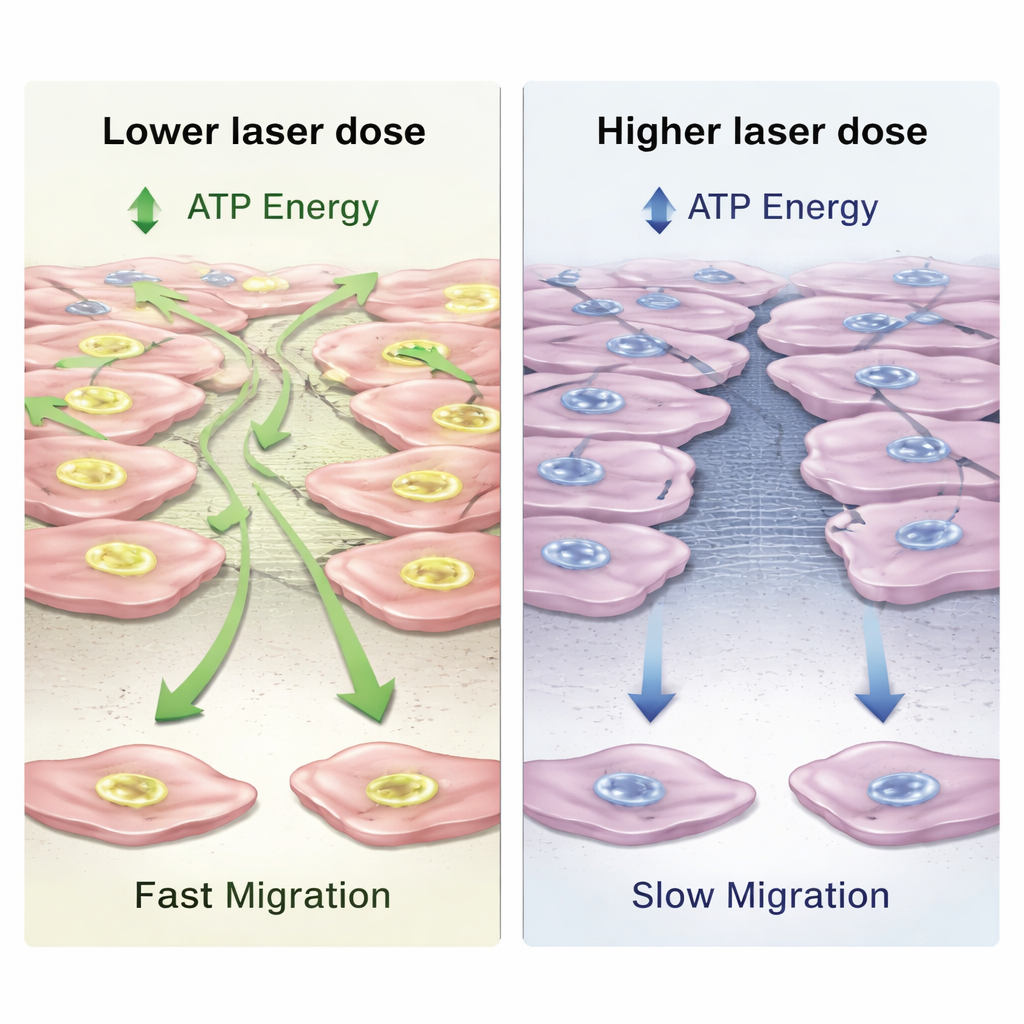
Qué podría significar esto para la cicatrización dental
Dado que estos experimentos se realizaron en un modelo simplificado en placa, no pueden capturar por completo la complejidad de una herida que cicatriza en una boca viva, donde el flujo sanguíneo, las células inmunitarias y las bacterias juegan papeles importantes. Aun así, los resultados delinean una ventana prometedora de dosis de luz en la que un láser dental de 940 nm puede aumentar la energía de las células gingivales y guiar su movimiento sin causar daño ni inflamación. El trabajo también demuestra que afinar la dosis importa: las condiciones que maximizaron el combustible celular no fueron exactamente las mismas que produjeron el cierre más rápido de la herida artificial.
Conclusión para pacientes y clínicos
Para el público general, el mensaje clave es que la luz láser de bajo nivel, controlada con cuidado, podría en el futuro ayudar a que las encías cicatricen más rápido y de forma más predecible tras procedimientos como injertos, implantes o extracciones. En este estudio, una exposición muy breve y sin contacto a un láser de diodo de 940 nm animó a las células gingivales cultivadas a mantenerse saludables, producir más energía y, en el rango de dosis adecuado, desplazarse más rápido para sellar una brecha similar a una herida. Estos parámetros aún no están listos para aplicarse directamente en la clínica, pero proporcionan una base científica para futuros estudios en animales y humanos orientados a convertir un láser dental cotidiano en una herramienta precisa para potenciar la reparación natural del tejido en lugar de limitarse a cortar.
Cita: Mizrahi, I.K., Neculau, C., Balasea, B.V. et al. Cellular bioenergetic and migratory responses of human gingival fibroblasts to 940 nm diode laser photobiomodulation. Sci Rep 16, 5972 (2026). https://doi.org/10.1038/s41598-026-35824-8
Palabras clave: cicatrización de heridas gingivales, terapia láser de bajo nivel, recuperación tras cirugía oral, fotobiomodulación, fibroblastos gingivales