Clear Sky Science · es
El mechano-estrés favorece la migración de células heterogéneas de cáncer de pulmón hacia canales confinados e investiga el crecimiento de esferoides tumorales de células que migran en espacios confinados
Por qué importa que las células cancerosas se aprieten
El cáncer no se disemina en un espacio abierto. Cuando las células tumorales abandonan su sitio de origen, deben comprimirse para atravesar diminutos huecos en tejidos, paredes de vasos sanguíneos y otras estructuras densamente pobladas. Este estudio plantea una pregunta simple pero poderosa: dentro de una multitud mixta de células de cáncer de pulmón, ¿cuáles son las que realmente atraviesan estos puntos estrechos y qué tipo de tumores generan después? Las respuestas pueden ayudar a explicar por qué algunas células cancerosas son más peligrosas que otras y podrían orientar nuevas formas de predecir o frenar la metástasis.
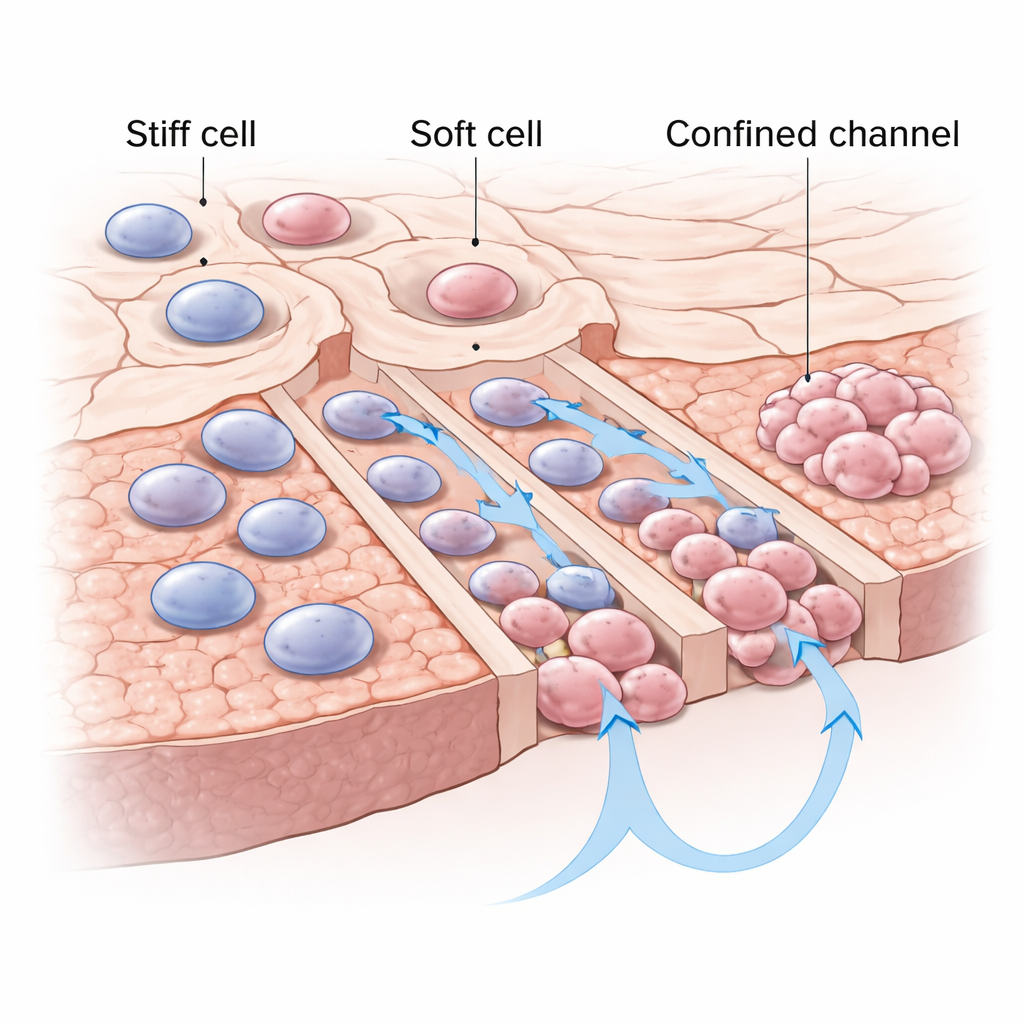
Las células más blandas ganan en espacios estrechos
Los autores se centraron en un rasgo físico de las células que la mayoría de la gente nunca escucha: la rigidez. Algunas células cancerosas son relativamente rígidas, mientras que otras son blandas y se deforman con facilidad. Empleando chips microfluídicos diseñados ad hoc —pequeños dispositivos plásticos grabados con canales más estrechos que una célula típica— atraparon células individuales de cáncer de pulmón en las entradas de canales estrechos (confinados) y altos (no confinados). Tras 24 horas, más células individuales eligieron y atravesaron con éxito los canales estrechos confinados que los más abiertos, y se desplazaron más rápido dentro de estos pasajes ajustados. Cuando los investigadores analizaron posteriormente la mecánica de las células con un microscopio de fuerza atómica (una especie de “dedo” a escala nanométrica), hallaron que las viajeras en los canales confinados eran consistentemente más blandas que sus contrapartes que se quedaron o se movieron por canales no confinados.
Una firma molecular de la blandura
Para entender qué hacía que algunas células fueran más blandas, el equipo examinó una proteína estructural llamada vimentina y una proteína de soporte nuclear codificada por el gen LMNA. La vimentina forma parte del armazón interno que ayuda a la célula a resistir la deformación. Las células que habían atravesado canales confinados mostraron niveles más bajos de vimentina en comparación con las células en canales espaciosos o en placas de cultivo convencionales. Imágenes de alta resolución revelaron que, en los migrantes confinados, la red de vimentina estaba dispuesta de forma más laxa tanto alrededor del cuerpo celular como cerca del núcleo, en vez de estar densamente agrupada. Tests de expresión génica a nivel de célula individual confirmaron que tanto el gen de vimentina (VIM) como LMNA, que contribuye a mantener el núcleo mecánicamente robusto, estaban regulados a la baja en las células que preferían rutas confinadas.
Hacer las células más blandas aumenta la migración confinada
Los investigadores se preguntaron después si podían ablandar intencionadamente las células y ver si eso cambiaba su comportamiento. Usaron dos enfoques: un tratamiento bioquímico (TGF-β1) conocido por remodelar el esqueleto celular, y una compresión mecánica suave con planchas de silicona blanda que presionaban las células. Ambos métodos redujeron la rigidez y bajaron los niveles de vimentina sin matar a las células. Cuando estas células pre-ablantadas se introdujeron en el dispositivo microfluídico, una fracción aún mayor migró hacia los canales estrechos en comparación con las células no tratadas. Esto sugiere que la blandura no es solo un efecto secundario del confinamiento; es una propiedad que puede ajustarse y que influye fuertemente en si una célula puede entrar y atravesar aberturas pequeñas.
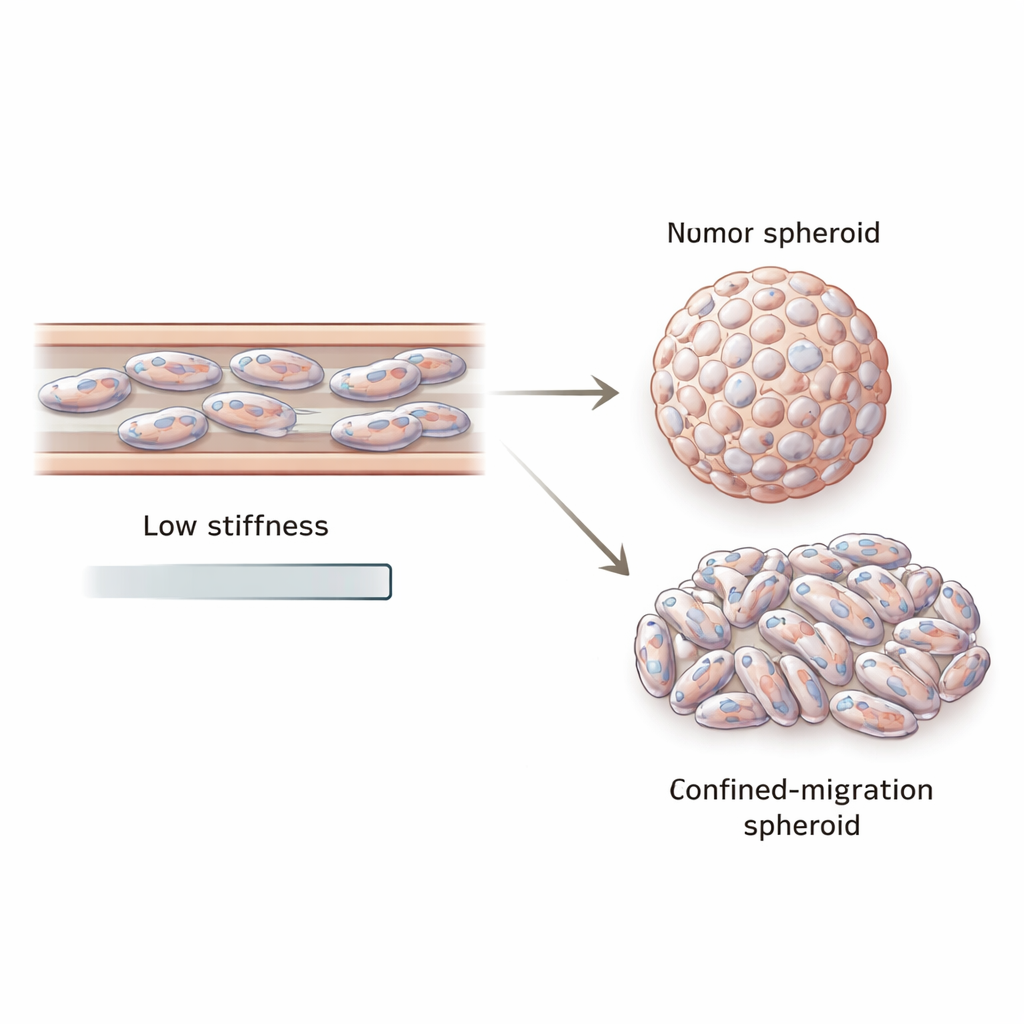
De células exprimidas a pelotas tumorales deformes
La metástasis, sin embargo, no es solo movimiento. Las células que escapan deben también regenerarse como nuevos tumores. Para imitar este paso, el equipo usó un segundo sistema de confinamiento llamado trans-well, donde las células migran a través de poros diminutos antes de ser recogidas y cultivadas en pocillos antiadherentes para formar esferoides tumorales tridimensionales. Los esferoides formados por células que habían migrado por confinamiento eran más pequeños y visiblemente menos redondeados que los esferoides formados por las mismas líneas celulares sin haber sido exprimidas previamente. Los núcleos celulares estaban más alargados y deformados, y esos esferoides continuaron mostrando una expresión reducida de VIM y LMNA. Incluso dentro de esferoides individuales, los niveles de vimentina variaban del centro a la periferia, lo que apunta a una diversidad mecánica y genética en el tumor hijo.
Qué significa esto para entender la metástasis
Dicho claramente, este estudio muestra que, entre muchas células de cáncer de pulmón, las más blandas tienen más probabilidades de deslizarse por espacios estrechos, sobrevivir al viaje y después formar agregados tumorales de forma extraña y mecánicamente frágiles con núcleos distorsionados. Esas células portan y mantienen una firma molecular distintiva —niveles bajos de genes estructurales clave— que vincula cómo se mueven con cómo crecen. Aunque el trabajo se realizó en dispositivos de laboratorio cuidadosamente controlados y no en pacientes, ofrece un plan físico y genético de una célula cancerosa “migrante por confinamiento”. A largo plazo, medir o apuntar a la blandura celular y a sus marcadores moleculares podría formar parte de estrategias para comprender, rastrear o, eventualmente, interrumpir las subpoblaciones celulares más invasivas.
Cita: Alam, M.K., Ma, Y., Zhai, J. et al. Mechano-stress endorsing heterogeneous lung cancer cells migration into confined channels and investigating tumor spheroids growth of confined space migrating cells. Sci Rep 16, 6649 (2026). https://doi.org/10.1038/s41598-026-35818-6
Palabras clave: rigidez de células cancerosas, migración celular confinada, esferoides de cáncer de pulmón, vimentina y LMNA, mecánica tumoral