Clear Sky Science · es
La pérdida de masa muscular asociada a la sepsis se atenúa con la inhibición farmacológica de la vía de señalización STAT3 en ratones
Por qué las infecciones graves te pueden robar la fuerza
Sobrevivir a una infección potencialmente mortal como la sepsis es solo la mitad de la batalla. Muchos pacientes salen de la unidad de cuidados intensivos tan débiles que caminar, subir escaleras o incluso levantar los brazos se vuelve una lucha. Este estudio plantea una pregunta sencilla pero urgente: ¿podemos evitar que el cuerpo se coma sus propios músculos durante la sepsis y, si es así, cómo? Usando ratones, células musculares en cultivo y observaciones de personas en una unidad de cuidados intensivos, los investigadores trazan una vía de señalización clave que impulsa la pérdida muscular y muestran que un fármaco dirigido puede bloquear parcialmente el daño.
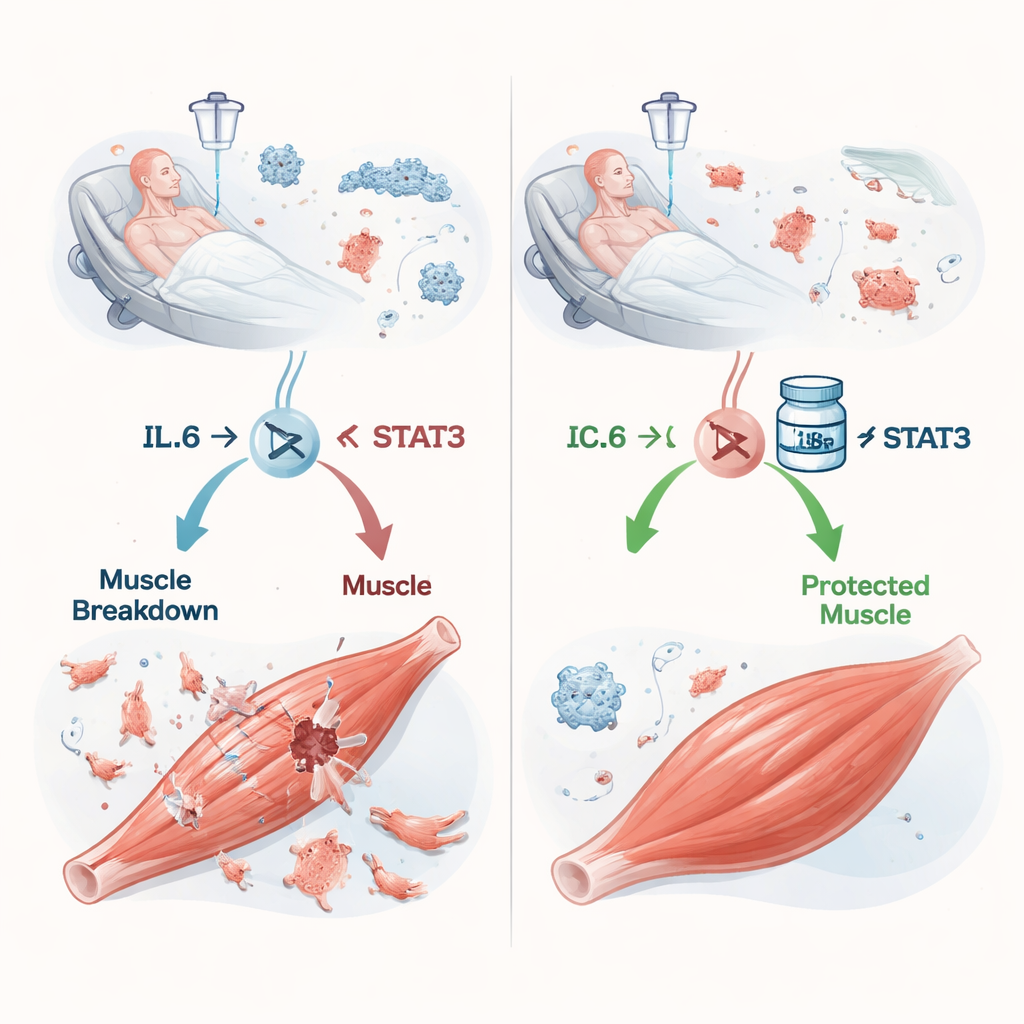
Una reacción en cadena desde la infección hasta la pérdida muscular
La sepsis ocurre cuando la respuesta del cuerpo a una infección se descontrola, inundando el torrente sanguíneo con moléculas inflamatorias. Una de las más importantes es la interleucina‑6 (IL‑6). Trabajos previos insinuaron que la IL‑6 puede indicar a los músculos que degraden sus propias proteínas, pero los detalles eran confusos. Los autores se centraron en STAT3, una proteína intracelular que transmite el mensaje de la IL‑6 al núcleo, donde se activan o desactivan genes. En ratones a los que se administró un slurry cecal —esencialmente una infección controlada con bacterias mixtas— los niveles de IL‑6 en sangre y en los músculos de las patas aumentaron a medida que la sepsis empeoraba. Al mismo tiempo, STAT3 se activó en el músculo y los animales perdieron peso, masa muscular y fuerza de agarre de forma dependiente de la gravedad, un cuadro muy parecido al que se observa en pacientes críticos.
Cómo la sepsis reprograma las células musculares
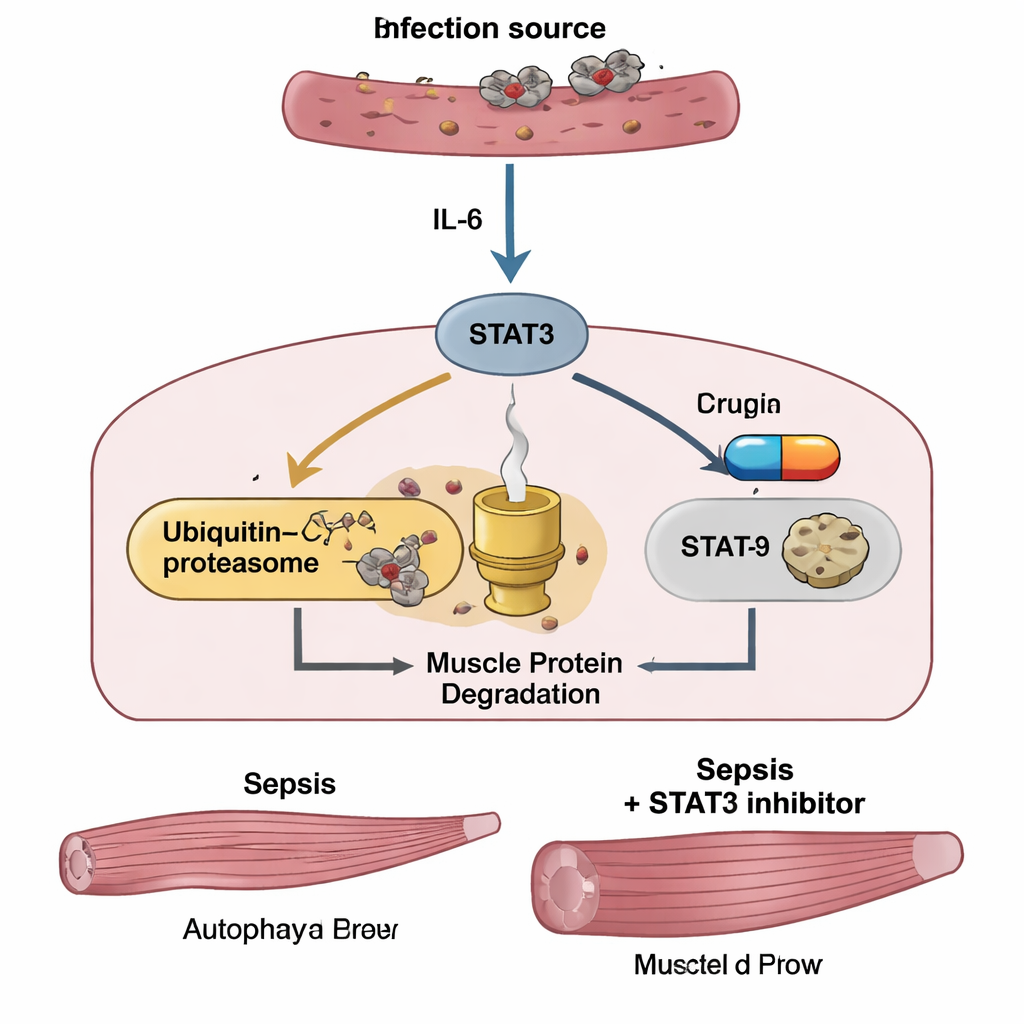
Para entender qué hacía la sepsis dentro de las fibras musculares, el equipo analizó la actividad génica en el tibial anterior, un músculo importante de la pata. Miles de genes cambiaron su actividad en los ratones sépticos en comparación con los controles sanos. Se activaron vías relacionadas con la inflamación, el estrés celular y, especialmente, la señalización IL‑6/STAT3. Se intensificaron dos sistemas principales de eliminación de proteínas: el sistema ubiquitina–proteasoma, que etiqueta proteínas musculares específicas para su destrucción, y la autofagia, un proceso de reciclaje más general. Las principales enzimas «destructoras» de músculo, MuRF1 y atrogin‑1, aumentaron de forma marcada, mientras que las vías promotoras del crecimiento y las señales clásicas de muerte celular permanecieron en gran medida sin cambios. En experimentos paralelos, células musculares de ratón en cultivo expuestas a lipopolisacárido (LPS), un componente de la pared de bacterias Gram‑negativas, mostraron el mismo patrón: activación de IL‑6 y STAT3, aumento de MuRF1 y atrogin‑1, más autofagia y adelgazamiento visible de las fibras musculares.
Bloquear un interruptor clave para proteger el músculo
El experimento central probó si apagar STAT3 podría ahorrar músculo. Ratones con sepsis recibieron un inhibidor pequeño de STAT3 llamado C188‑9, empezando una hora después de la infección y luego a diario. El fármaco no mitigó la «tormenta de citoquinas» inicial: los niveles sanguíneos de IL‑6 y de otro factor inflamatorio, TNF‑α, permanecieron altos, y el peso corporal y el apetito no se recuperaron rápidamente. Sin embargo, C188‑9 protegió claramente el músculo esquelético: los ratones tratados conservaban más masa del tibial anterior, tenían una mayor fuerza de agarre y presentaban fibras musculares de mayor tamaño al microscopio que los ratones sépticos no tratados. En el interior de los músculos, C188‑9 redujo de forma pronunciada STAT3 activado y disminuyó los niveles de MuRF1 y atrogin‑1, pero dejó los marcadores de autofagia en gran medida sin cambios. En experimentos en placa, el pretratamiento de células musculares con C188‑9 también atenuó la activación de STAT3 y el aumento de MuRF1 y atrogin‑1, y evitó el encogimiento inducido por LPS de las fibras, nuevamente sin apagar la autofagia.
Pistas de pacientes en la unidad de cuidados intensivos
Para comprobar si estos mecanismos tienen relevancia en humanos, los investigadores siguieron a 67 adultos con sepsis ingresados en una unidad de cuidados intensivos en Japón. Los análisis de sangre al ingreso mostraron que los pacientes con shock séptico tenían niveles de IL‑6 especialmente elevados. En todo el grupo, la IL‑6 —pero no TNF‑α— se correlacionó estrechamente con las puntuaciones de gravedad de la sepsis y con marcadores sanguíneos de inflamación y daño muscular. En un subgrupo de 45 pacientes que se sometieron a dos tomografías computarizadas del abdomen, los niveles de IL‑6 al ingreso predijeron cuánto se redujo el músculo psoas a la altura lumbar durante las siguientes una a tres semanas. Los que perdieron más músculo tuvieron una supervivencia a dos años marcadamente peor que quienes mantuvieron más masa muscular, lo que subraya que la pérdida muscular relacionada con la sepsis no es solo estética: se asocia con mortalidad a largo plazo.
Qué podría significar esto para tratamientos futuros
En conjunto, los datos de ratones, células y humanos dibujan una historia plausible: durante la sepsis, la IL‑6 en ascenso activa STAT3 en el músculo, lo que a su vez aumenta un sistema degradador de proteínas que despoja a las fibras musculares de su maquinaria contráctil. La autofagia también aumenta pero parece estar menos controlada directamente por STAT3. Al bloquear farmacológicamente STAT3 con C188‑9, los investigadores pudieron interrumpir esta vía de «autocanibalismo» en ratones y en células musculares en cultivo, preservando la fuerza aun cuando la infección y la inflamación continuaban. Aunque este trabajo sigue siendo preclínico y no demuestra que los inhibidores de STAT3 ayudarán a pacientes humanos, apunta al eje IL‑6/STAT3 como un objetivo prometedor para fármacos destinados a prevenir o reducir la profunda debilidad muscular que aqueja a muchos supervivientes de la sepsis.
Cita: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Palabras clave: sepsis, pérdida muscular, STAT3, inflamación, recuperación tras enfermedad crítica