Clear Sky Science · es
Lightweight SwiM-UNet con adaptador multidimensional para segmentación médica eficiente en dispositivo
Exploraciones más inteligentes junto al paciente
Las exploraciones cerebrales pueden revelar tumores que amenazan la vida, pero convertir imágenes en bruto en contornos claros sobre los que los médicos puedan actuar sigue siendo lento y exigente en recursos. Este estudio presenta SwiM‑UNet, un nuevo algoritmo que puede segmentar tumores cerebrales a partir de IRM 3D con precisión de vanguardia mientras se ejecuta de forma eficiente en dispositivos locales, acercando el análisis preciso de imágenes al lado de la cama del paciente o incluso a clínicas móviles. 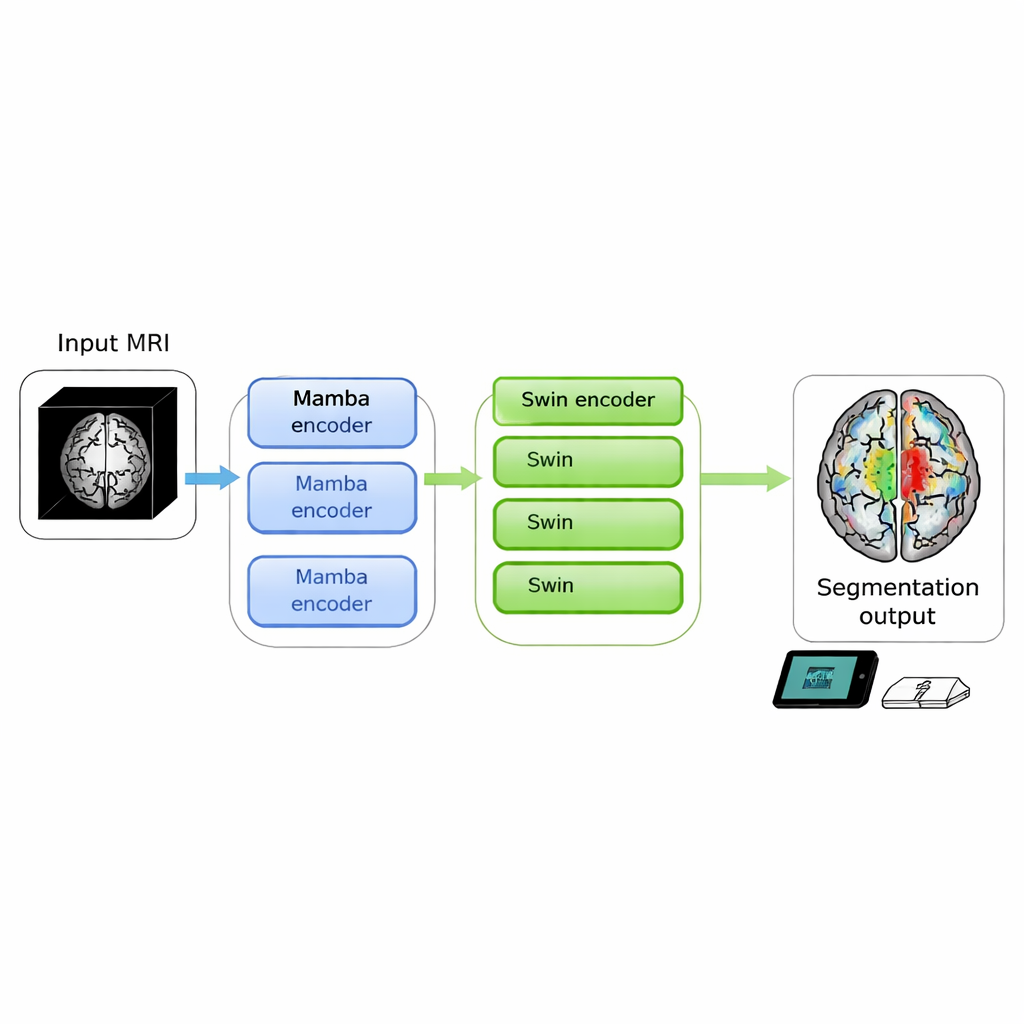
Por qué importan los contornos precisos de los tumores
La medicina moderna depende en gran medida de la imagenología para planificar cirugías, radioterapia y tratamientos farmacológicos. Para los tumores cerebrales, los médicos necesitan no solo ver que existe un tumor, sino conocer con exactitud dónde comienzan y terminan sus distintas partes. Esta tarea, llamada segmentación, suele realizarse o perfeccionarse por especialistas corte a corte —un proceso que consume tiempo, puede retrasar decisiones y varía entre expertos. Las herramientas automáticas de segmentación basadas en aprendizaje profundo han mejorado la situación, pero las más precisas a menudo requieren grandes procesadores gráficos, lo que dificulta su uso directo en la clínica, especialmente en máquinas más pequeñas o portátiles.
Dos ideas potentes que no caben fácilmente en máquinas pequeñas
Los avances recientes en visión por computador proceden principalmente de dos familias de modelos. Los sistemas basados en transformers, como el Swin Transformer, son excelentes para captar patrones globales en un escaneo 3D completo y han impulsado segmentadores de tumores cerebrales de alto rendimiento. Sin embargo, su operación central, llamada self‑attention, se vuelve extremadamente costosa a medida que crece el tamaño de la imagen, lo que limita su uso en tiempo real o en hardware compacto. Una familia más nueva, conocida como Mamba y basada en modelos de espacio de estados, ofrece una solución ingeniosa: procesa secuencias en tiempo efectivamente lineal, reduciendo las operaciones necesarias. Los experimentos iniciales en imagen médica mostraron que los modelos estilo Mamba son rápidos y eficientes, pero por lo general se quedan por detrás de los transformers en calidad de segmentación, especialmente con formas tumorales complejas.
Mezclando velocidad y precisión en un solo diseño
Los autores se propusieron fusionar las fortalezas de ambos enfoques en un único modelo 3D. Su SwiM‑UNet mantiene la estructura en forma de U, ampliamente usada en imagen médica, con un codificador que comprime la información y un decodificador que reconstruye segmentaciones detalladas. En las etapas iniciales, donde el escaneo aún es grande y de alta resolución, usan bloques Mamba eficientes para mantener las operaciones bajo control. Más profundo en la red, tras el muestreo descendente, cambian a bloques Swin Transformer optimizados que ahora pueden permitirse modelar relaciones a largo alcance sin sobrecargar el hardware. Un puente personalizado llamado MS‑adapter enlaza estos dos regímenes. Observa las características a lo largo del ancho, alto y profundidad del volumen por separado, y también a través de los canales, y luego aprende mediante pequeñas unidades de gating cuánto debe influir cada vista en la representación final. 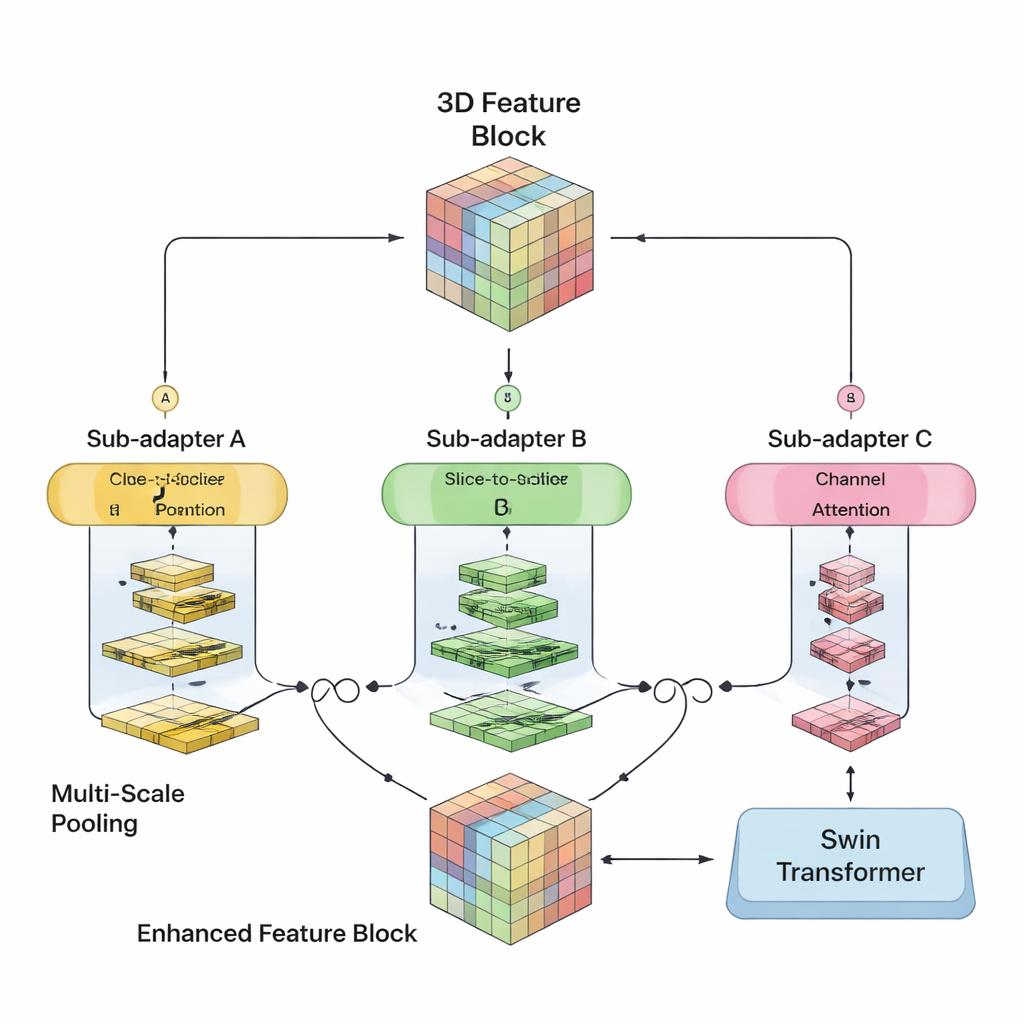
Hacer más con menos cómputo
Más allá de este diseño híbrido, el equipo recorta cómputo innecesario usando capas totalmente conectadas de bajo rango y un decodificador que reduce deliberadamente el número de canales que debe manejar. Probaron varias variantes con distintas mezclas de capas Mamba y Swin y encontraron que usar Mamba en las tres primeras etapas del codificador y Swin solo en la etapa más profunda ofrecía el mejor equilibrio entre velocidad y precisión. En dos grandes conjuntos públicos de tumores cerebrales de los desafíos BraTS 2023 y 2024, SwiM‑UNet alcanzó mayor precisión y límites más precisos que modelos líderes basados solo en transformers, solo en Mamba y modelos híbridos previos, mientras consumía muchas menos operaciones en coma flotante y reducía el tiempo de inferencia a alrededor de 45 milisegundos por parche de exploración en una tarjeta gráfica moderna.
Listo para dispositivos del mundo real
Para comprobar si estas mejoras importan fuera del laboratorio, los autores compararon las demandas computacionales del modelo con las capacidades de sistemas edge clínicos típicos: consolas de IRM portátiles, ordenadores punto de atención y estaciones de trabajo en quirófano. Su análisis sugiere que, a diferencia de los modelos transformer más pesados, SwiM‑UNet cabe cómodamente dentro de los límites de potencia, memoria y velocidad de tales dispositivos, cumpliendo a menudo los requisitos de tiempo real. También tuvo un buen rendimiento en un conjunto de datos separado de TC abdominal, lo que indica que el enfoque puede generalizar más allá de los tumores cerebrales e incluso más allá de la IRM.
Lo que esto significa para pacientes y clínicos
En términos prácticos, SwiM‑UNet demuestra que es posible acercarse a la precisión de los modelos de segmentación más sofisticados manteniendo el cómputo lo suficientemente ligero para uso en dispositivo. Eso podría permitir contornos tumorales más rápidos y consistentes en urgencias, hospitales rurales o unidades móviles de imagenología sin enviar exploraciones sensibles a servidores remotos. Aunque se requiere trabajo adicional para adaptar el método a distintos escáneres y condiciones, este diseño híbrido apunta a un futuro en el que el análisis de imágenes de alta calidad se ejecute donde esté el paciente, no solo en centros de datos.
Cita: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Palabras clave: segmentación de tumores cerebrales, IA en imágenes médicas, redes neuronales híbridas, inferencia en dispositivo, análisis 3D de IRM