Clear Sky Science · es
Variantes por empalme de KChIP1 modulan los canales Kv4 promoviendo rasgos de inactivación tipo P/C
Cómo los poros diminutos moldean el ritmo eléctrico del cerebro
Cada pensamiento, recuerdo y movimiento en el cerebro depende de señales eléctricas rápidas en las neuronas. Estas señales están finamente ajustadas por poros microscópicos—canales iónicos—que permiten el paso de partículas cargadas hacia dentro y fuera. Este artículo explora cómo variaciones sutiles de una proteína auxiliar, KChIP1, pueden cambiar de forma notable el comportamiento de una familia de canales (los Kv4), alterando la facilidad con la que las neuronas pueden disparar ráfagas repetidas de actividad eléctrica.
Los canales de potasio como pedal de freno del cerebro
Los canales Kv4 median una corriente de potasio llamada tipo A que se activa y desactiva con rapidez en el soma y las ramas de las neuronas. Esta corriente contribuye a fijar la propensión de una neurona a disparar y su fidelidad para seguir señales entrantes, especialmente a bajas tasas de disparo. Los canales Kv4 no actúan solos: se ensamblan con proteínas auxiliares en un complejo de varias partes que incluye proteínas DPP y las KChIP. Estos socios influyen en la velocidad con que los canales se cierran y en la rapidez con la que vuelven a estar listos para abrirse. Hasta ahora, la mayoría de los trabajos sugerían que las KChIP, en general, aceleran la recuperación de los Kv4 tras su apagado, permitiendo a las neuronas responder rápidamente a entradas repetidas.
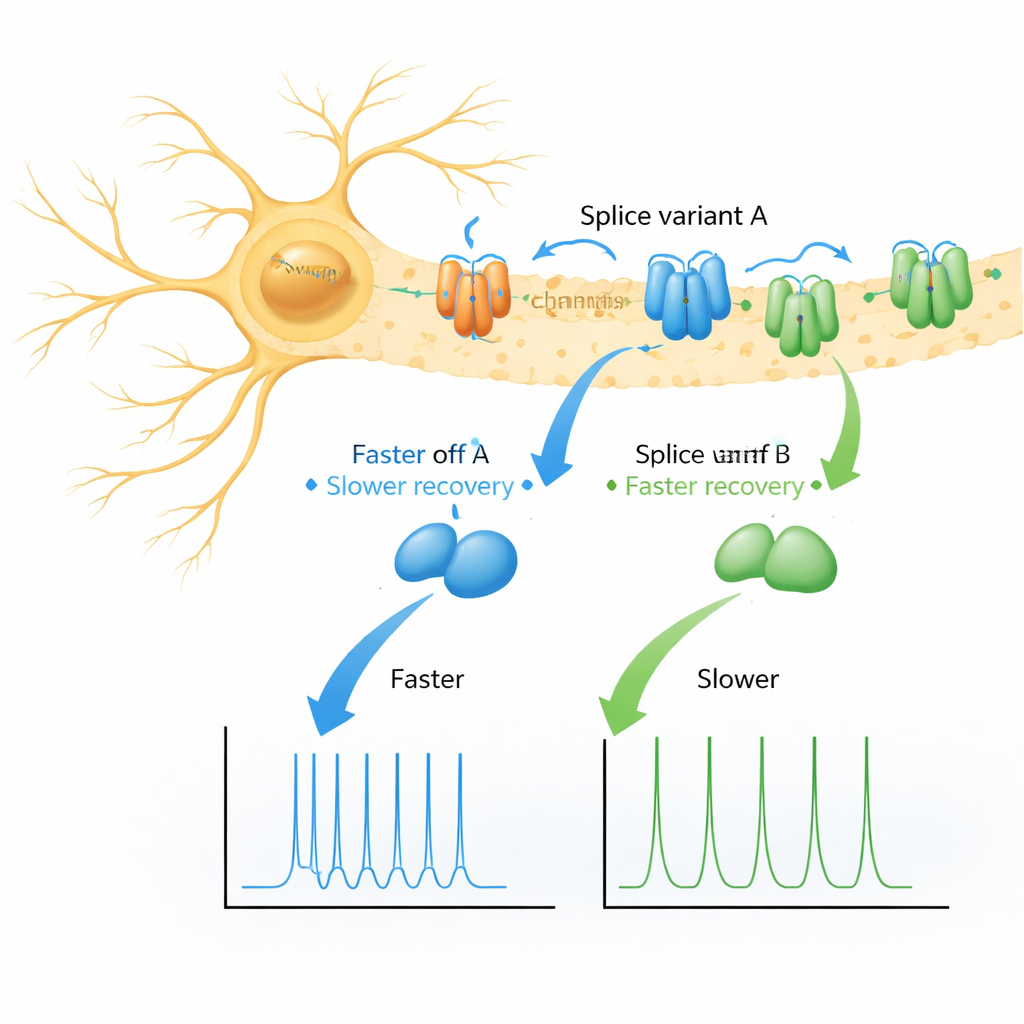
Dos variantes proteicas, dos sabores de recuperación
Los autores se centraron en dos versiones casi idénticas (variantes por empalme) de KChIP1, llamadas 1a y 1b, que difieren solo por una corta “cola” aromática al inicio de 1b. Usando ovocitos de rana como banco de pruebas controlado, expresaron varios tipos de canales Kv4 solos, con cada variante de KChIP1, con DPP, o con ambos auxiliares a la vez. Como era de esperar, tanto 1a como 1b remodelaron suavemente cómo los canales se apagaban durante un escalón de voltaje, sin cambios dramáticos. La sorpresa surgió al examinar la recuperación tras el apagado: en lugar de un regreso único y suave a la disponibilidad, los canales asociados con 1a o 1b mostraron dos fases de recuperación distintas—una rápida y otra mucho más lenta—siendo la vía lenta mucho más pronunciada con 1b.
Revelación de una vía lenta oculta
Cuando los canales Kv4 se expresaron sin KChIP1, se recuperaron por una vía simple y rápida, y DPP aceleró aún más esa recuperación. Añadir KChIP1 cambió ese patrón. Con 1a, la mayoría de los canales todavía se recuperaban rápido, pero una pequeña fracción tomaba un desvío lento de vuelta al estado listo. Con 1b, una fracción mucho mayor entraba en esta vía lenta, alargando la recuperación hasta segundos. Este efecto apareció en todos los subtipos de Kv4 probados y persistió incluso en presencia de DPP, lo que indica que la vía lenta es una característica intrínseca de los complejos que contienen KChIP1, no un artefacto de un canal o configuración experimental concreta. Los autores también observaron que 1b desplazaba el rango de voltajes de “apagado” de los canales hacia valores más negativos, sesgándolos aún más hacia la indisponibilidad durante la actividad continua.
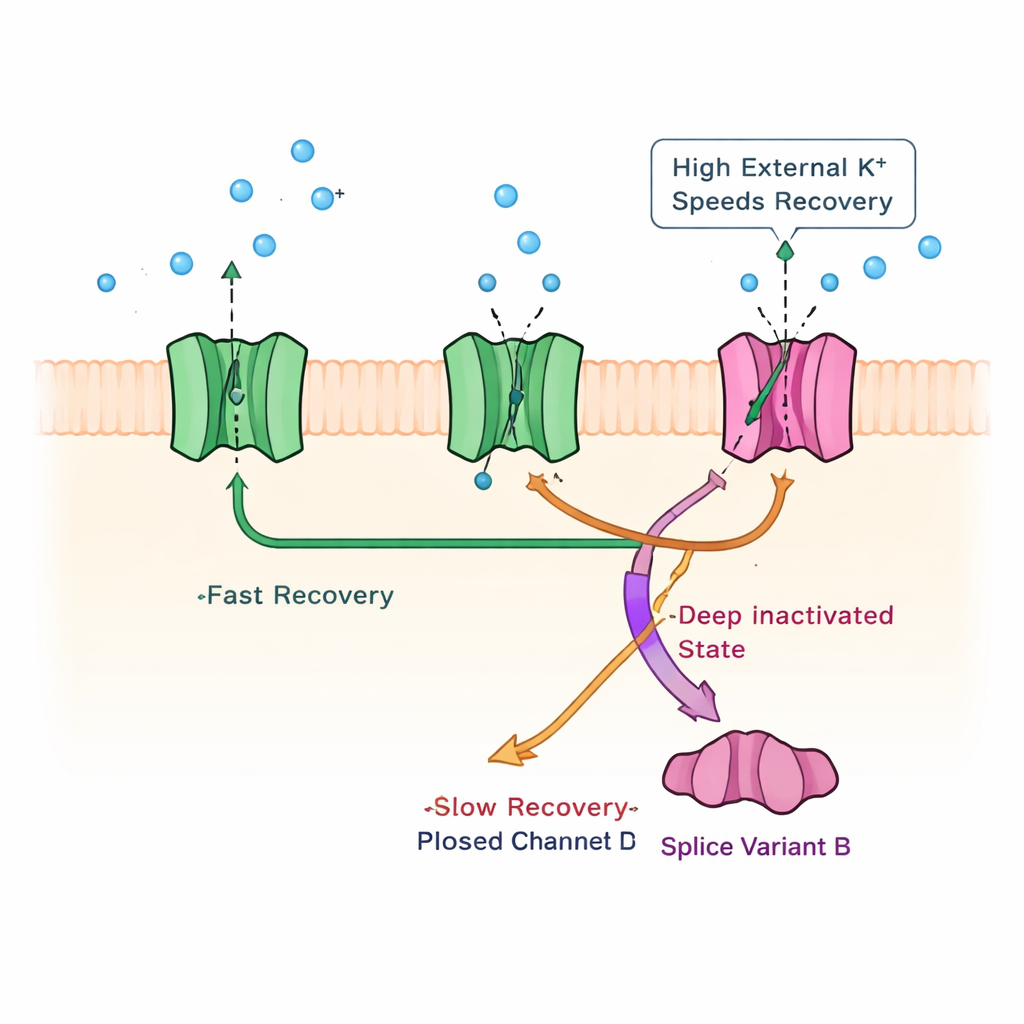
Descubriendo un mecanismo de inactivación latente
Para entender qué cambio físico dentro del canal subyace a esta recuperación lenta, el equipo investigó mecanismos de inactivación conocidos en otros canales de potasio. Razonaron en contra de un bloqueo clásico tipo “bola y cadena” en la boca interna del canal al cortar parte de la cola interna; la fase lenta persistió. Luego usaron altos niveles de potasio externo, un truco conocido por alterar un proceso de inactivación centrado en el poro en otros canales. Bajo estas condiciones, el apagado de la corriente se aceleró pero, crucialmente, la propia fase de recuperación lenta se aceleró de modo específico, como si el potasio elevado liberara canales de un estado bloqueado profundo y de larga duración. Mutaciones estratégicas en un segmento de la compuerta del canal apoyaron además la idea de que KChIP1b promueve una vía de inactivación centrada en el poro—normalmente débil en Kv4—que coexiste con su inactivación habitual, más rápida, en estado cerrado.
Por qué esto importa para la actividad cerebral
Los hallazgos sugieren que, al escoger entre KChIP1a, KChIP1b o mezclas de ambas, las neuronas pueden afinar con precisión la velocidad a la que las corrientes tipo A se recuperan entre picos. En células ricas en KChIP1b, una fracción significativa de los canales Kv4 queda “estacionada” en un estado inactivado profundo y de lenta reversión, limitando su disponibilidad durante el disparo rápido. Esto puede permitir que ciertos interneuronas—células que coordinan y restringen la actividad en circuitos cerebrales—disparen a frecuencias más altas o con patrones temporales distintos. En esencia, una pequeña diferencia por empalme en una proteína auxiliar desbloquea un modo de frenado oculto en los canales de potasio, añadiendo una nueva capa de flexibilidad a la manera en que el cerebro controla sus propios ritmos eléctricos.
Cita: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Palabras clave: Canales de potasio Kv4, Variantes por empalme de KChIP1, Corriente tipo A, Excitabilidad neuronal, Inactivación del canal