Clear Sky Science · es
El papel del receptor nicotínico de acetilcolina α7 en la promoción de la polarización de macrófagos M2 en sitios inflamatorios
Cómo los nervios ayudan a calmar la inflamación descontrolada
Cuando nos cortamos un dedo o combatimos una infección, nuestros cuerpos desencadenan inflamación para protegernos. Pero si esa reacción arde durante demasiado tiempo, puede dañar el tejido sano y promover enfermedades crónicas. Este estudio explora cómo un receptor específico de efecto "calmante" en las células inmunitarias, llamado receptor nicotínico de acetilcolina α7 (α7nAChR), ayuda a orientar la inflamación hacia la curación en lugar del daño, ofreciendo pistas para nuevos tratamientos de afecciones como la sepsis, las enfermedades intestinales y la artritis.
Las dos caras de los equipos de limpieza inmunitarios
Los macrófagos son células inmunitarias que actúan como equipos de limpieza y reparación. Pueden cambiar entre dos modos principales. En su modo de "ataque", a menudo llamado M1, liberan sustancias agresivas para matar gérmenes y eliminar desechos. En su modo de "curación", conocido como M2, liberan señales calmantes que reducen la inflamación y promueven la reparación tisular. Una respuesta saludable comienza con más células M1 y luego cambia gradualmente hacia M2 a medida que pasa el peligro. Los autores quisieron saber si α7nAChR, un receptor originalmente famoso por su papel en la comunicación nerviosa y los efectos de la nicotina en el cerebro, también ayuda a dirigir a los macrófagos hacia este estado curativo M2 durante la inflamación.
Un interruptor ligado a los nervios que favorece la curación
Para investigarlo, los investigadores usaron ratones que tenían o carecían del α7nAChR e indujeron inflamación en la cavidad abdominal de dos maneras: con un componente bacteriano (imitando infección) y con manipulación intestinal suave (imitando lesión quirúrgica estéril). Midieron marcadores moleculares que distinguen el comportamiento M1 del M2 y usaron citometría de flujo para contar las proporciones de cada tipo de macrófago. En ratones normales, la fase temprana de la inflamación estuvo dominada por señales M1, pero durante los siguientes uno o dos días aumentaron los marcadores de las células M2, reflejando un cambio natural hacia la reparación. En los ratones sin α7nAChR, sin embargo, los marcadores proinflamatorios fueron más altos, los marcadores de curación más bajos, y la proporción de macrófagos M2 en la zona inflamada se redujo de manera sostenida, inclinando el equilibrio local hacia un estado dominante M1, más dañino.
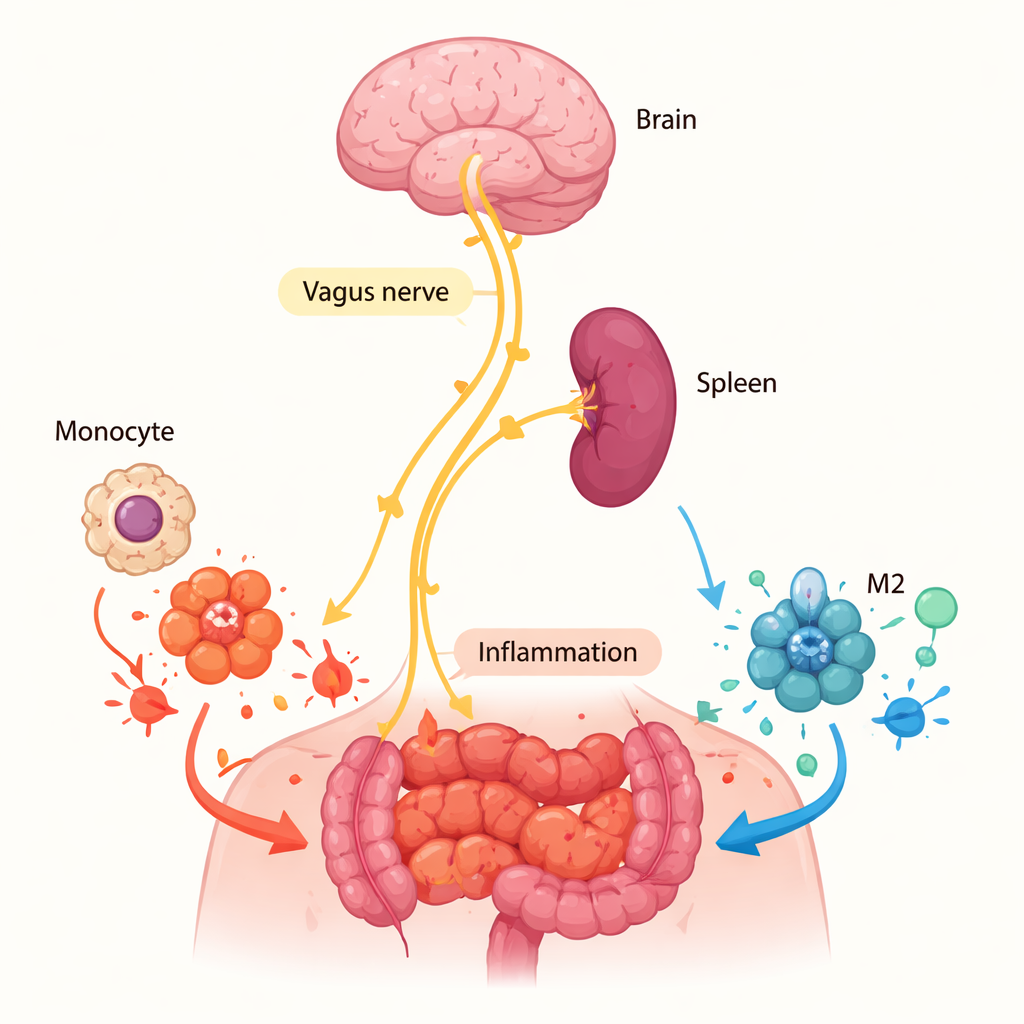
Por qué el bazo importa más que la herida
El equipo preguntó luego dónde estaba actuando α7nAChR. Podría haber actuado directamente en el sitio inflamado si las células locales liberaran acetilcolina, el químico que activa el receptor. Pero las mediciones de acetilcolina en el líquido abdominal y en cultivos celulares del tejido inflamado resultaron esencialmente negativas, lo que descarta una señal local fuerte. En su lugar, la atención se centró en el bazo, un órgano inmune clave ya conocido por participar en una "vía antiinflamatoria colinérgica" controlada por el nervio vago. Cuando los investigadores extirparon quirúrgicamente el bazo de ratones normales y luego indujeron inflamación abdominal, la proporción de macrófagos M2 en la cavidad peritoneal disminuyó y el número total de macrófagos cayó. Este patrón reflejó lo observado en ratones sin α7nAChR, lo que sugiere que las señales impulsadas por los nervios en el bazo predisponen a los monocitos —los precursores de los macrófagos— a convertirse en células M2 antes incluso de llegar al tejido inflamado.
Probando el interruptor en células humanas
Para ver si el mismo receptor puede modular células humanas, los científicos recurrieron a monocitos cultivados en el laboratorio a partir de una línea de leucemia (THP-1) y de sangre humana donada. Guiaron a estas células para que se desarrollaran en macrófagos M1 o M2 usando señales inmunes estándar y luego añadieron un fármaco específico que activa α7nAChR. En ambas fuentes humanas, activar α7nAChR no aumentó los marcadores M1 pero sí incrementó de forma clara rasgos clave del comportamiento M2, incluido el marcador de superficie CD206 y la molécula antiinflamatoria interleucina-10. Estos experimentos apoyan la idea de que α7nAChR actúa como un interruptor que sesga el desarrollo de los macrófagos hacia una identidad curativa sin simplemente apagar la respuesta inmune por completo.
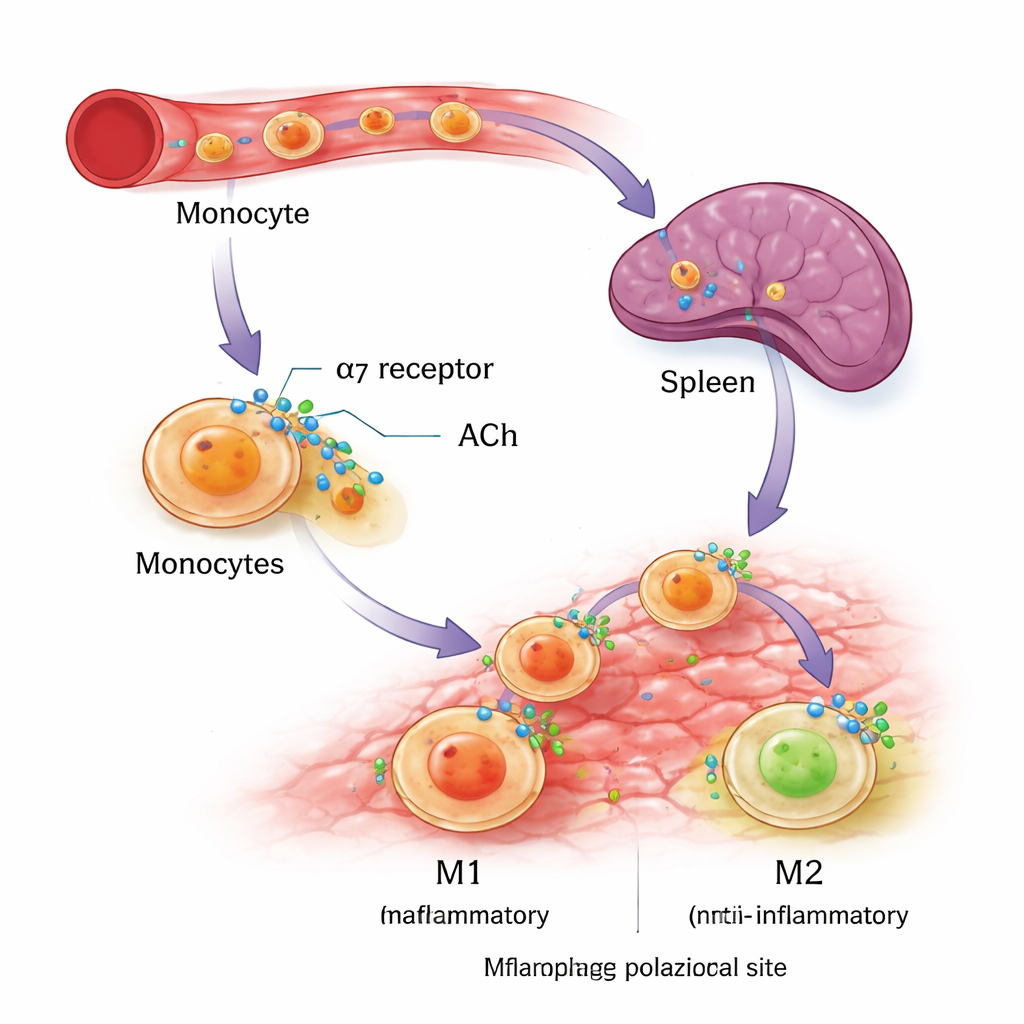
De las pistas sobre la nicotina a futuras terapias
Los hallazgos ayudan a explicar varias observaciones enigmáticas, como por qué la estimulación del nervio vago puede mejorar las enfermedades inflamatorias y por qué los fumadores, a pesar de muchos riesgos para la salud, parecen tener un riesgo algo menor de ciertas afecciones intestinales —la nicotina puede activar α7nAChR. En lugar de limitarse a bloquear químicos inflamatorios, α7nAChR parece ayudar al cuerpo a convertir sus equipos de limpieza inmunitarios en células M2 más enfocadas en la reparación, particularmente mediante el entrenamiento de monocitos en el bazo. Para un lector no especialista, esto significa que nuestro sistema nervioso hace más que detectar el dolor o controlar los músculos; también orienta silenciosamente a las células inmunitarias sobre cuándo luchar y cuándo curar. Aprender a activar de forma segura este interruptor inherente con fármacos o estimulación nerviosa dirigida podría abrir nuevas vías para calmar la inflamación nociva sin sacrificar la capacidad del cuerpo para defenderse.
Cita: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Palabras clave: polarización de macrófagos, inflamación, nervio vago, receptor nicotínico de acetilcolina, regulación inmune