Clear Sky Science · es
Formas fisiológicamente relevantes de los trazadores radiactivos Tc- y Re-pirofosfato y la base de su sensibilidad al amiloide de transtiretina
Por qué importa esta historia sobre la imagen cardíaca
Muchas personas desarrollan depósitos silenciosos de proteínas mal plegadas, llamados amiloides, en el corazón a medida que envejecen. Algunos de estos depósitos, en especial los formados por una proteína sanguínea llamada transtiretina, pueden endurecer el corazón y provocar una enfermedad grave. Los médicos confían cada vez más en un trazador radiactivo conocido como pirofosfato de tecnecio‑99m (99mTc‑PYP) para visualizar estos depósitos en las exploraciones. Sin embargo, sorprendentemente, la forma exacta de este trazador en el organismo y por qué parece “preferir” ciertos tipos de amiloide no estaba clara. Este artículo combina teoría y experimento para descubrir cómo es realmente el trazador en condiciones fisiológicas y cómo esa forma puede permitirle localizar los fibrilos dañinos de transtiretina.
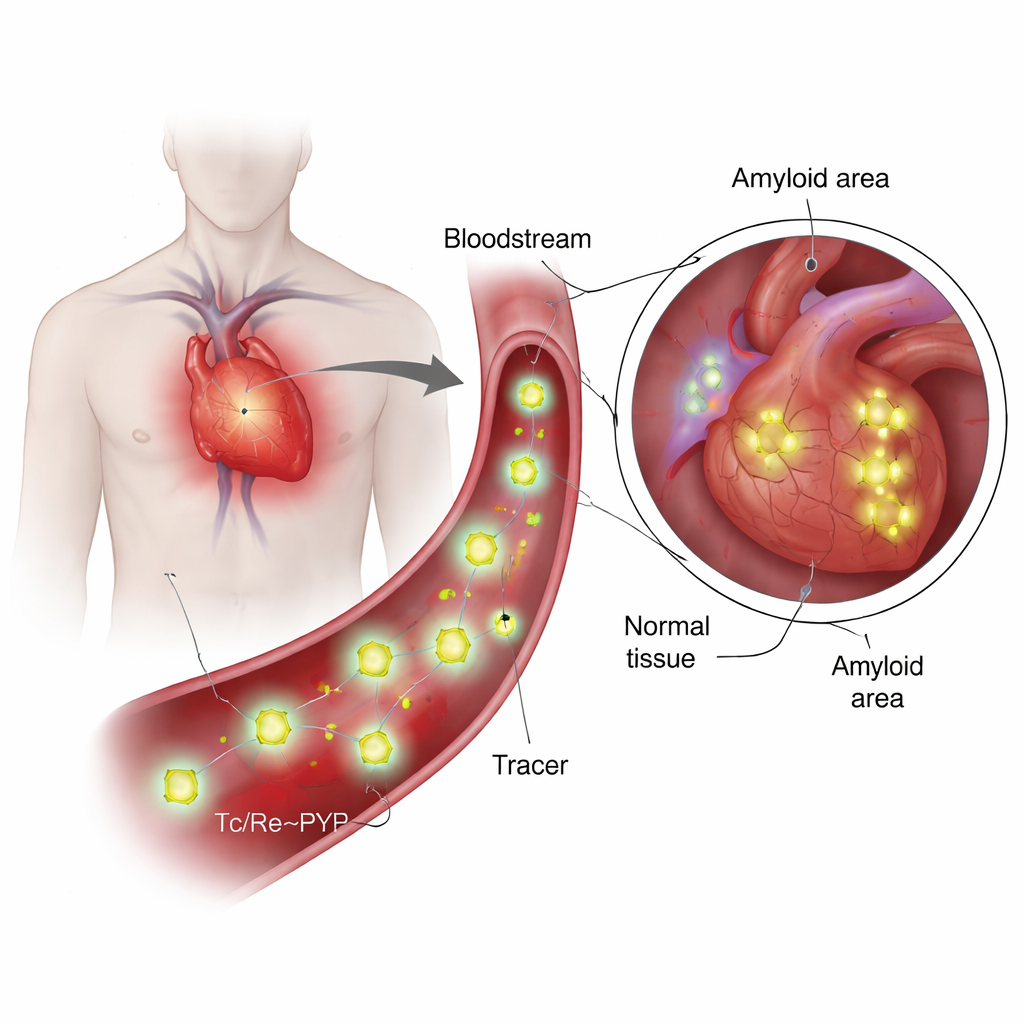
¿Qué son estos trazadores y por qué son especiales?
El 99mTc‑PYP se ha usado durante décadas para imagear el hueso, porque tiende a acumularse donde el calcio y la renovación mineral son elevados. Más recientemente, los médicos descubrieron que también puede distinguir entre dos tipos principales de amiloidosis cardíaca: una formada por cadenas ligeras de anticuerpos (AL) y otra por transtiretina (ATTR). En ATTR, el corazón suele iluminarse fuertemente en las exploraciones con PYP, mientras que los casos AL tienden a permanecer tenues, incluso cuando la acumulación de calcio parece similar. Esta discrepancia planteó una cuestión clave: ¿se adhiere el trazador solo al calcio, o interactúa directamente con la proteína amiloide? Responder eso requiere conocer la estructura química verdadera del trazador en condiciones semejantes a la sangre, algo que trabajos anteriores solo habían bosquejado de forma general.
Usar un sustituto más seguro para ver lo invisible
Puesto que el tecnecio es radiactivo y está presente solo en cantidades ínfimas en las preparaciones médicas, resulta difícil estudiarlo directamente con muchas técnicas de laboratorio. Los autores usaron por tanto rutenio, un elemento estrechamente relacionado con tamaño y preferencias de enlace casi idénticas pero con una química más manejable, como sustituto. Prepararon mezclas de rutenio‑pirofosfato en condiciones que imitan los kits clínicos de PYP y las examinaron con una batería de herramientas: cálculos cuánticos de alto nivel, absorción en el rango UV‑visible, diversas espectroscopías vibracionales (infrarrojo y Raman), resonancia magnética nuclear, espectrometría de masas y espectroscopía Mössbauer del estaño. En conjunto, estos métodos les permitieron testar muchas estructuras candidatas y acotar cuáles especies son probables en pH neutro, como el de la sangre.
Una forma molecular flexible pero reconocible
La evidencia combinada apunta a una “estructura núcleo” común: un complejo octaédrico en el que un átomo de tecnecio o rutenio en estado de oxidación +4 está unido a dos grupos pirofosfato y a dos moléculas de agua. En términos simples, el metal se sitúa en el centro de una jaula casi octaédrica formada por átomos de oxígeno, con los pirofosfatos actuando como anclajes multifuncionales y las aguas ocupando las posiciones restantes. Esta unidad básica diaqua dipirofosfato no es rígida. Dado que los brazos del pirofosfato pueden girar y formar puentes de hidrógeno internos con las aguas ligadas, la molécula explora muchas formas ligeramente diferentes en solución. Los cálculos y los espectros sugieren que estas variaciones desplazan sus huellas de absorción de luz y vibracionales, lo que explica por qué las bandas experimentales son anchas y por qué estudios anteriores tuvieron dificultades para identificar una única estructura nítida.
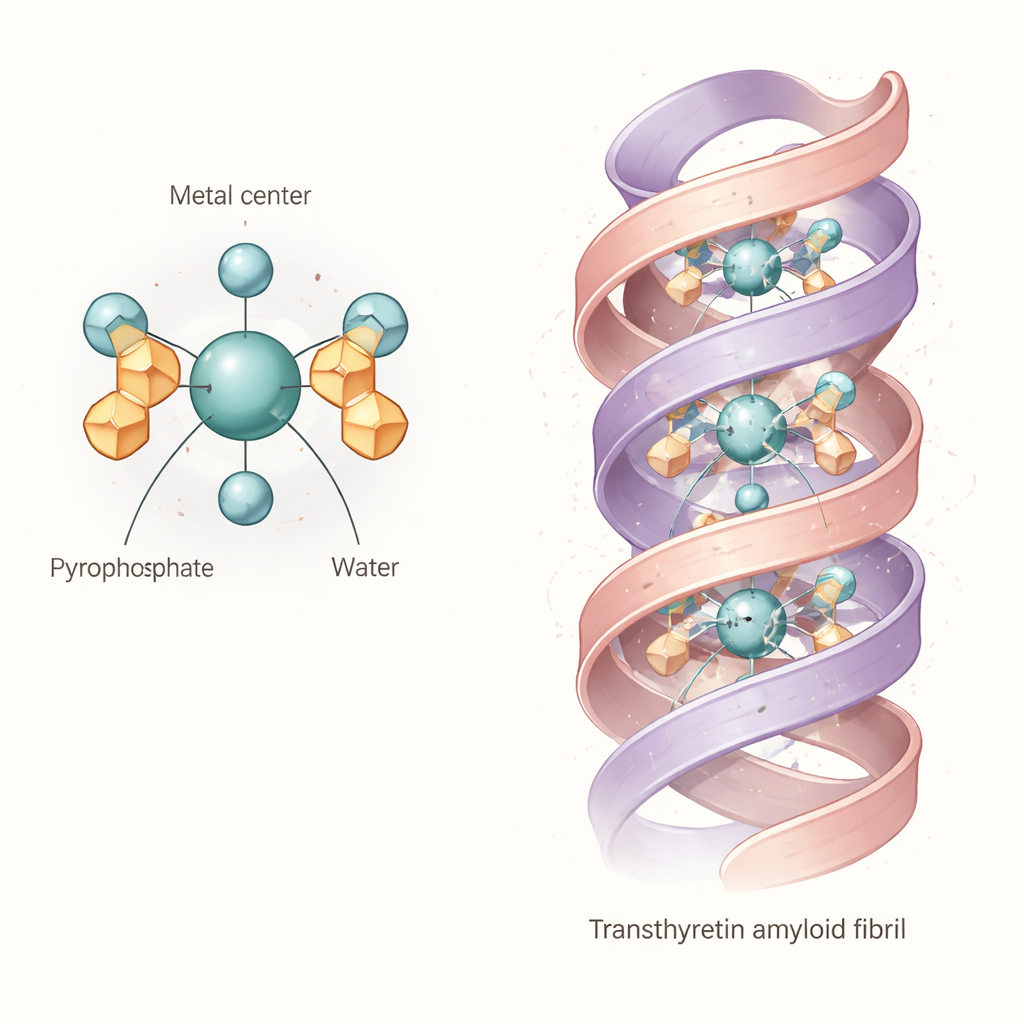
Qué significa esto para la unión al amiloide cardíaco
Los autores se preguntaron luego si este complejo flexible podría razonablemente encajar directamente en los fibrilos de transtiretina. Usando una estructura detallada de criomicroscopía electrónica de un fibrilo humano de transtiretina, realizaron búsquedas de acoplamiento por ordenador con el complejo modelado de tecnecio‑pirofosfato. Los resultados muestran que la unidad diaqua dipirofosfato puede acomodarse en un canal central que recorre el fibrilo, formando múltiples puentes de hidrógeno y puentes salinos con cadenas laterales cargadas que recubren la cavidad. Esto sugiere que, al menos para algunas conformaciones de fibrilos de transtiretina, el trazador no se limita a marcar depósitos minerales cercanos; puede ser sujetado directamente por el andamiaje proteico. La «flexibilidad» estructural del trazador probablemente le ayuda a adaptarse a huecos y patrones de carga ligeramente distintos en fibrilos reales de pacientes.
Implicaciones para el diagnóstico y futuros trazadores
Para un lector no especializado, la conclusión es que la exploración cardíaca con PYP ampliamente utilizada se basa en un trazador más sutil y consciente de la proteína de lo que se pensaba. En condiciones fisiológicas, es mejor considerarlo como una pequeña jaula metálica‑pirofosfato que porta agua, capaz de flexionar y formar múltiples puntos de contacto con canales amiloides de transtiretina. Esta idea ayuda a explicar por qué el trazador muestra señales fuertes en algunas enfermedades amiloides pero no en otras, y por qué cambios minúsculos en la proteína o en su entorno pueden provocar pérdidas de sensibilidad desconcertantes. Al aclarar la forma funcional y el patrón de carga del trazador, el estudio sienta las bases para diseñar agentes de imagen o terapéuticos de próxima generación que reconozcan con mayor selectividad los fibrilos causantes de enfermedad en el corazón y más allá.
Cita: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Palabras clave: amiloidosis cardíaca, transtiretina, pirofosfato de tecnecio, imagen molecular, química de radiotrazores