Clear Sky Science · es
Detección visual rápida de Treponema pallidum mediante el sistema RPA-CRISPR/Cas12a
Por qué esto importa para la salud diaria
La sífilis, una infección de transmisión sexual que se creía controlada, vuelve a aumentar en todo el mundo. Puede dañar silenciosamente el corazón, el cerebro y a los fetos si no se detecta. Sin embargo, las pruebas de laboratorio actuales no son ideales para cribados rápidos en consultas, áreas rurales o urgencias concurridas. Este artículo describe una nueva prueba de ADN de fácil lectura y de una hora de duración para el germen de la sífilis, Treponema pallidum, que pretende acercar el diagnóstico preciso al lado del paciente y a entornos con recursos limitados.
Un problema en crecimiento que es difícil de detectar
La sífilis es causada por una bacteria en forma de sacacorchos que se transmite principalmente por contacto sexual y de madre a hijo durante el embarazo. Los informes globales contabilizaron alrededor de 8 millones de casos nuevos en 2022 y 1,5 millones de casos de sífilis congénita en 2023, cifras que señalan importantes lagunas en el cribado y el tratamiento. La mayoría de las pruebas actuales no buscan el germen en sí; en su lugar, detectan anticuerpos, la respuesta del organismo a la infección. Estas pruebas sanguíneas se usan ampliamente porque son baratas y sencillas, pero pueden pasar por alto infecciones muy tempranas, dar falsos positivos en condiciones como el embarazo o enfermedades autoinmunes, y a menudo permanecen positivas de por vida. Eso significa que no pueden indicar fácilmente a los médicos si un paciente tiene una infección activa o una que fue curada hace tiempo.
Construyendo una prueba de ADN más rápida
Para resolver estos problemas, los investigadores crearon una prueba que detecta directamente el ADN de la sífilis. Se centraron en un gen llamado tp47, un marcador estable y ampliamente utilizado para esta bacteria. La prueba combina dos herramientas modernas. La primera es la amplificación por polimerasa mediada por recombinasa (RPA), que copia rápidamente el ADN a una temperatura constante, parecida a la corporal, en lugar de alternar temperaturas altas y bajas como las máquinas PCR tradicionales. La segunda es CRISPR/Cas12a, un sistema enzimático conocido por la edición genética, pero aquí reconvertido en un sensor altamente selectivo. Cuando Cas12a es guiada hacia la secuencia de ADN tp47 coincidente, se activa y corta rápidamente fragmentos cortos de ADN “reportero” cercanos, liberando una fuerte señal fluorescente o provocando la aparición de una línea en una tira tipo inmunocromatográfica.
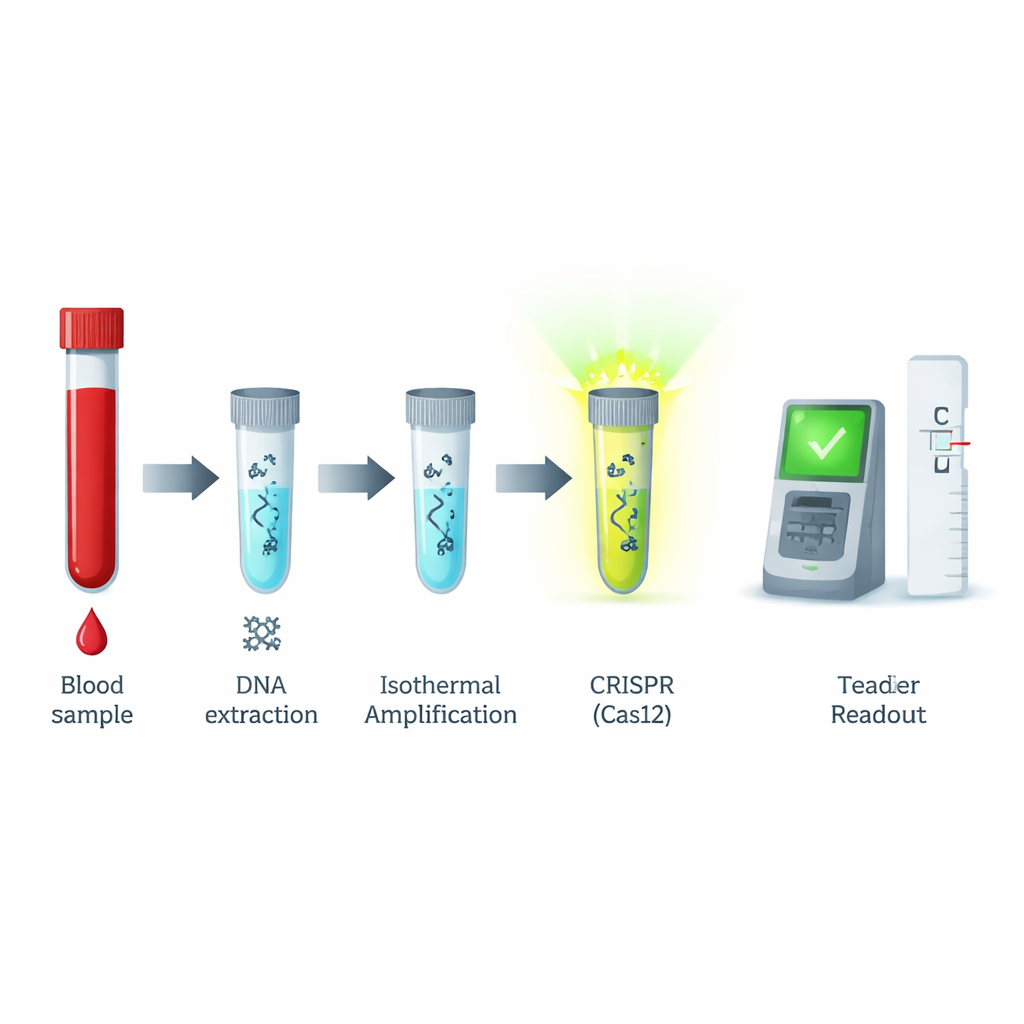
Cómo funciona la nueva prueba en la práctica
En el laboratorio, el equipo optimizó cada paso: el mejor par de cebadores para copiar el gen tp47, los tiempos de reacción ideales y las cantidades de la proteína Cas12a, su ARN guía y el reportero que genera la señal. Bajo estas condiciones afinadas, todo el proceso —desde añadir el ADN de la muestra del paciente hasta leer el resultado— lleva cerca de una hora. La versión por fluorescencia de la prueba pudo detectar de manera fiable tan solo unas 11 copias del ADN objetivo por microlitro, un nivel extremadamente bajo. También distinguió el ADN de la sífilis del material genético de varios otros virus transmitidos por la sangre que pueden causar síntomas similares, incluidos VIH, hepatitis B y C y dengue, sin reacciones cruzadas.
Del laboratorio de alta tecnología a la tira sencilla
Conscientes de que muchas consultas carecen de instrumentos especializados, los investigadores convirtieron su método en un ensayo de flujo lateral —el mismo formato básico usado en pruebas de embarazo domésticas y en muchas pruebas rápidas de COVID-19. Tras los pasos de RPA y CRISPR, la mezcla de reacción se aplica a una pequeña tira. Si el ADN tp47 está presente, aparece una línea de prueba junto a una línea de control. Esta versión en tira tuvo un límite de detección de aproximadamente 5,56 × 10² copias de ADN por microlitro, algo menos sensible que la lectura por fluorescencia pero aún adecuada para una prueba de campo. En ensayos con 30 muestras de sangre de pacientes, la prueba de fluorescencia coincidió con los diagnósticos hospitalarios estándar en el 96,6 % de los casos, mientras que la prueba en tira detectó correctamente los casos positivos pero necesita más ajustes para alcanzar el mismo rendimiento.
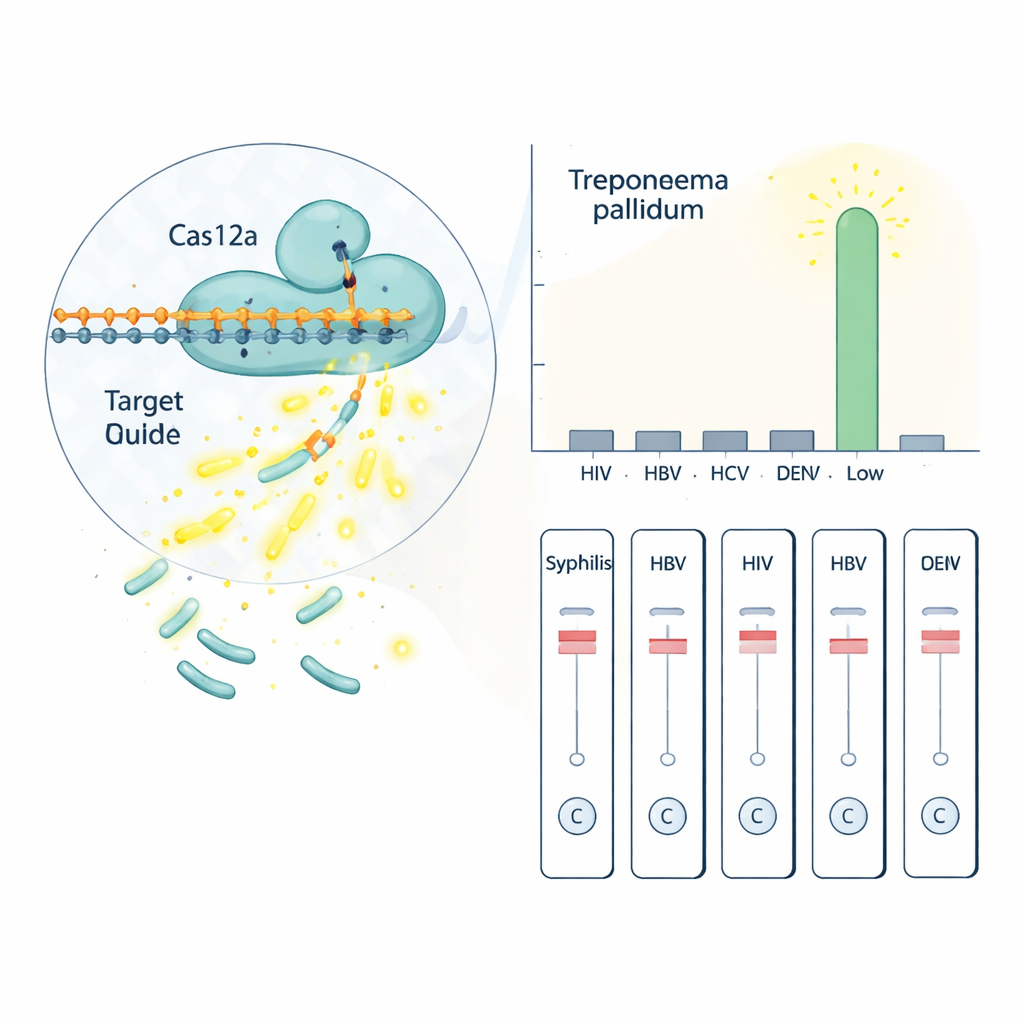
Qué podría significar esto para los pacientes
Para quienes no son especialistas, el mensaje clave es que esta nueva prueba busca directamente el ADN del germen de la sífilis, funciona rápidamente a temperaturas sencillas y puede ofrecer tanto una señal fluorescente intensa en un pequeño lector como una línea positiva clara en una tira desechable. Esa combinación de rapidez, sensibilidad y simplicidad podría ayudar a los médicos a detectar infecciones antes, especialmente en consultas con equipo limitado o en programas de atención comunitaria. Aunque se necesita más trabajo para mejorar la versión en tira y evaluar grupos de pacientes más grandes y diversos, la plataforma ofrece un modelo prometedor para el diagnóstico rápido de la sífilis en el punto de atención y, potencialmente, para pruebas similares dirigidas a muchos otros microbios infecciosos.
Cita: Li, W., Sun, Y., Ye, M. et al. Rapid visual detection of Treponema pallidum using the RPA-CRISPR/Cas12a system. Sci Rep 16, 5120 (2026). https://doi.org/10.1038/s41598-026-35745-6
Palabras clave: sífilis, Treponema pallidum, diagnóstico CRISPR, pruebas en el punto de atención, ensayo RPA-Cas12a