Clear Sky Science · es
Correlaciones de los ARNm relacionados con la metilación m6A y el cáncer de tiroides
Por qué pequeñas modificaciones en el ARN importan en el cáncer de tiroides
El cáncer de tiroides suele ser curable, pero algunos pacientes aún enfrentan recidivas o enfermedad diseminada. Este estudio analiza una capa emergente de la biología llamada «marcado» del ARN, en la que pequeñas etiquetas químicas se añaden a las moléculas de ARN dentro de nuestras células. Los investigadores plantearon una pregunta concreta: en personas con cáncer papilar de tiroides que no presentan enfermedad tiroidea autoinmune, ¿cambian estas marcas en el ARN de una forma que pueda contribuir al cáncer, y podrían esos cambios señalar nuevas vías para diagnosticarlo o tratarlo?
Acercándose a los tumores tiroideos sin enfermedad inmune
Mucha gente con cáncer de tiroides también presenta enfermedad tiroidea autoinmune, un ataque inmunitario contra la glándula que puede enturbiar el panorama biológico. Para evitar esto, el equipo estudió a 26 pacientes cuyos cánceres papilares de tiroides surgieron sin signos de autoinmunidad. De cada paciente recogieron un fragmento del tumor y un fragmento cercano de tejido tiroideo no canceroso. En un subconjunto de tres pacientes realizaron análisis amplios de qué genes estaban activados o silenciados y de cuánto llevaban una etiqueta química específica llamada m6A, la modificación interna más común en el ARN de las células humanas.
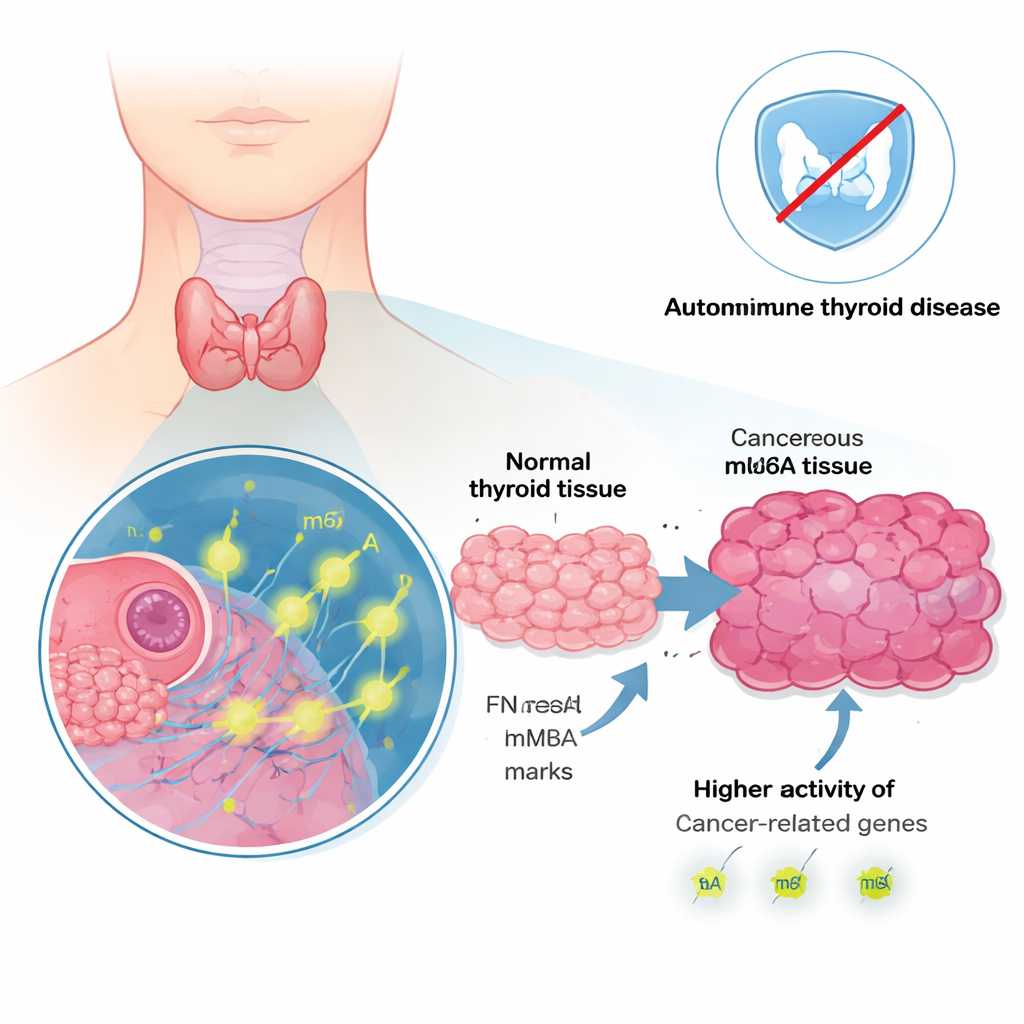
Un auge de genes y vías asociados al cáncer
Al comparar el tejido tumoral con el tejido sano circundante, los investigadores hallaron 486 genes con mayor actividad y 39 con menor actividad en el cáncer. Muchos de los genes más aumentados ya se han implicado en el crecimiento tumoral, la diseminación o la resistencia a tratamientos. Entre ellos están genes como LAMB3, FN1 y NMU, que ayudan a las células a interactuar con su estructura de soporte y con las células vecinas. El análisis informático mostró que los genes potenciados se agruparon en vías ya conocidas por alimentar el cáncer, incluidas redes de señalización relacionadas con la división celular, respuestas al estrés y comunicación entre células y el sistema inmunitario. En otras palabras, los tumores habían reprogramado claramente su actividad génica hacia el crecimiento y la invasión.
Las etiquetas en el ARN y un «lector» clave están aumentadas
La siguiente pregunta fue si la etiqueta m6A en el ARN estaba alterada en estos cánceres. Mediante un ensayo bioquímico, el equipo halló que los niveles globales de m6A eran más altos en el tejido tumoral que en el tejido normal emparejado. Luego examinaron los genes que controlan este sistema de marcado: “escritores” que añaden m6A, “borradores” que la eliminan y “lectores” que se unen al ARN marcado y determinan lo que ocurre después. Solo uno destacó en los tumores: una proteína lectora llamada IGF2BP2 se produjo a niveles significativamente más altos. Trabajos anteriores han mostrado que IGF2BP2 puede unirse a ARNs marcados con m6A y hacerlos más estables y más propensos a traducirse en proteína. En el cáncer papilar de tiroides, IGF2BP2 ya se ha asociado con un comportamiento más agresivo, peores resultados y mayor capacidad de diseminarse a los ganglios linfáticos.
Qué ARNs llevan etiquetas extra — y por qué importa
Al combinar el mapeo de m6A con las mediciones de actividad génica en las mismas muestras, los investigadores identificaron 367 ARNs con más marcado en los tumores y 12 con menos marcado. De manera llamativa, la mayoría de los ARNs más hipermarcados pertenecían a la misma lista de genes que impulsan el cáncer y que mostraban mayor actividad global. En 147 genes, los tumores presentaron tanto niveles más altos de m6A como mayor expresión, incluidos FN1, LAMB3, NMU y CDKN2B. El análisis de redes sugirió que estos genes ocupan el centro de sistemas que controlan cómo las células tumorales se adhieren a su entorno, responden a señales inflamatorias y remodelan el tejido circundante—pasos clave para la invasión y la metástasis. El equipo también encontró docenas de ARN largos no codificantes marcados, incluidos algunos vinculados a vías tumorales conocidas, lo que apunta a que el marcado del ARN puede influir no solo en los mensajes que codifican proteínas sino también en ARNs regulatorios que afinan el comportamiento génico.
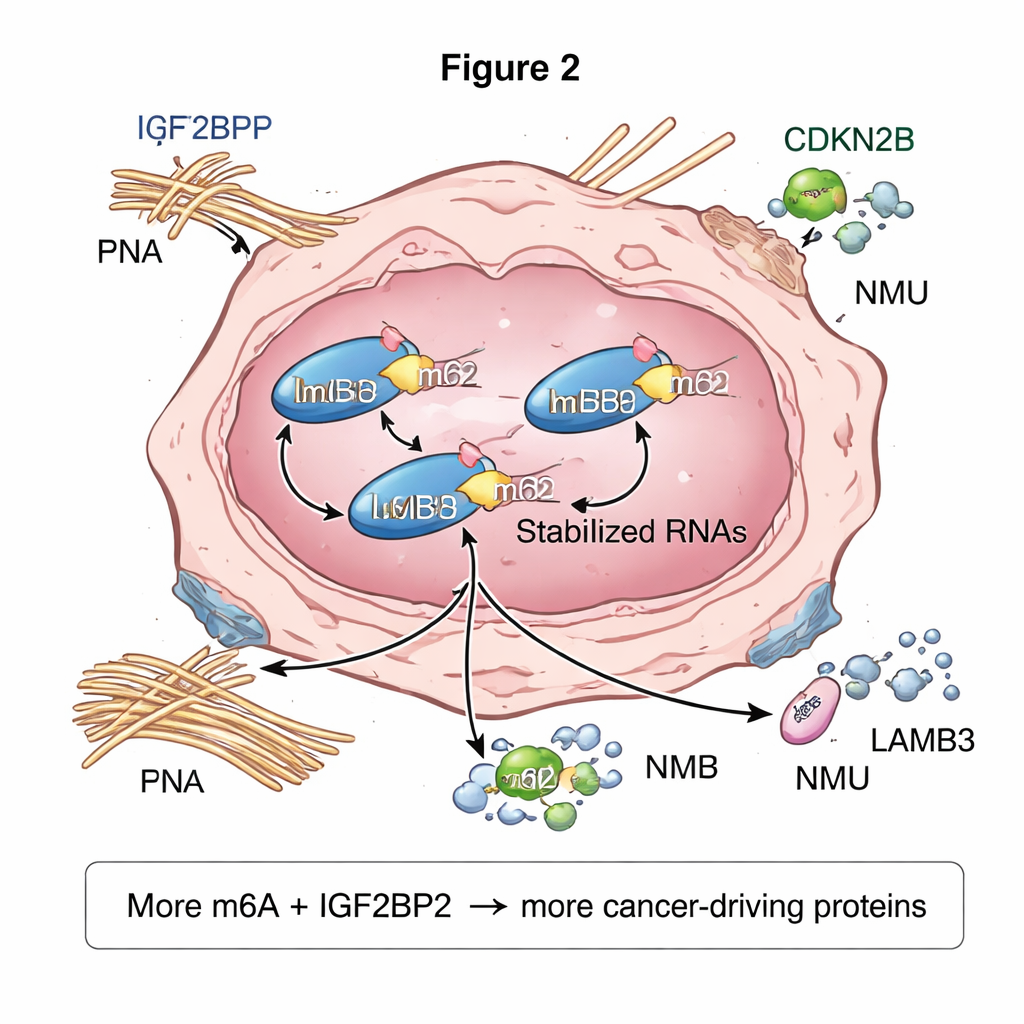
Qué podría significar esto para los pacientes
Para el público general, el mensaje central es que los cánceres papilares de tiroides—incluso en pacientes sin enfermedad tiroidea autoinmune—parecen explotar un sistema químico de marcado del ARN para amplificar redes que impulsan el cáncer. Las células tumorales muestran niveles globales más altos de m6A y mayores cantidades de la proteína lectora IGF2BP2, que en conjunto estabilizan y aumentan la producción de genes clave implicados en el crecimiento y la diseminación. Aunque este trabajo se basa principalmente en análisis computacionales y de laboratorio avanzados en un grupo pequeño de pacientes, destaca actores específicos—como IGF2BP2 y los genes marcados con m6A FN1, LAMB3 y NMU—como candidatos prometedores para nuevas pruebas o terapias dirigidas. Estudios futuros deberán confirmar estos hallazgos en cohortes más grandes y en modelos experimentales, pero los resultados sugieren que las marcas “epigenéticas” en el ARN constituyen una capa importante, y potencialmente abordable con fármacos, de la biología del cáncer de tiroides.
Cita: Jiang, Z., Luo, S., Lin, Y. et al. Correlations of m6A methylation-related mRNAs with thyroid cancer. Sci Rep 16, 5688 (2026). https://doi.org/10.1038/s41598-026-35712-1
Palabras clave: cáncer papilar de tiroides, metilación del ARN, modificación m6A, IGF2BP2, biomarcadores del cáncer