Clear Sky Science · es
Vpr del VIH induce la desmetilación del promotor antisentido de SNCA, conduciendo a deterioro neurocognitivo
Por qué el VIH todavía puede afectar al cerebro
Las personas que viven con VIH disfrutan de vidas más largas y saludables gracias a los fármacos antirretrovirales modernos. Sin embargo, muchas siguen sufriendo problemas de memoria, concentración y movimiento, incluso cuando el virus en su sangre está bien controlado. Este estudio explora por qué ocurre esto al centrarse en una pequeña proteína viral, llamada Vpr, y en una proteína cerebral, la alfa‑sinucleína, que también es central en la enfermedad de Parkinson. Comprender cómo interactúan estas dos moléculas puede revelar por qué el VIH acelera el envejecimiento cerebral y sugerir nuevas formas de proteger el cerebro.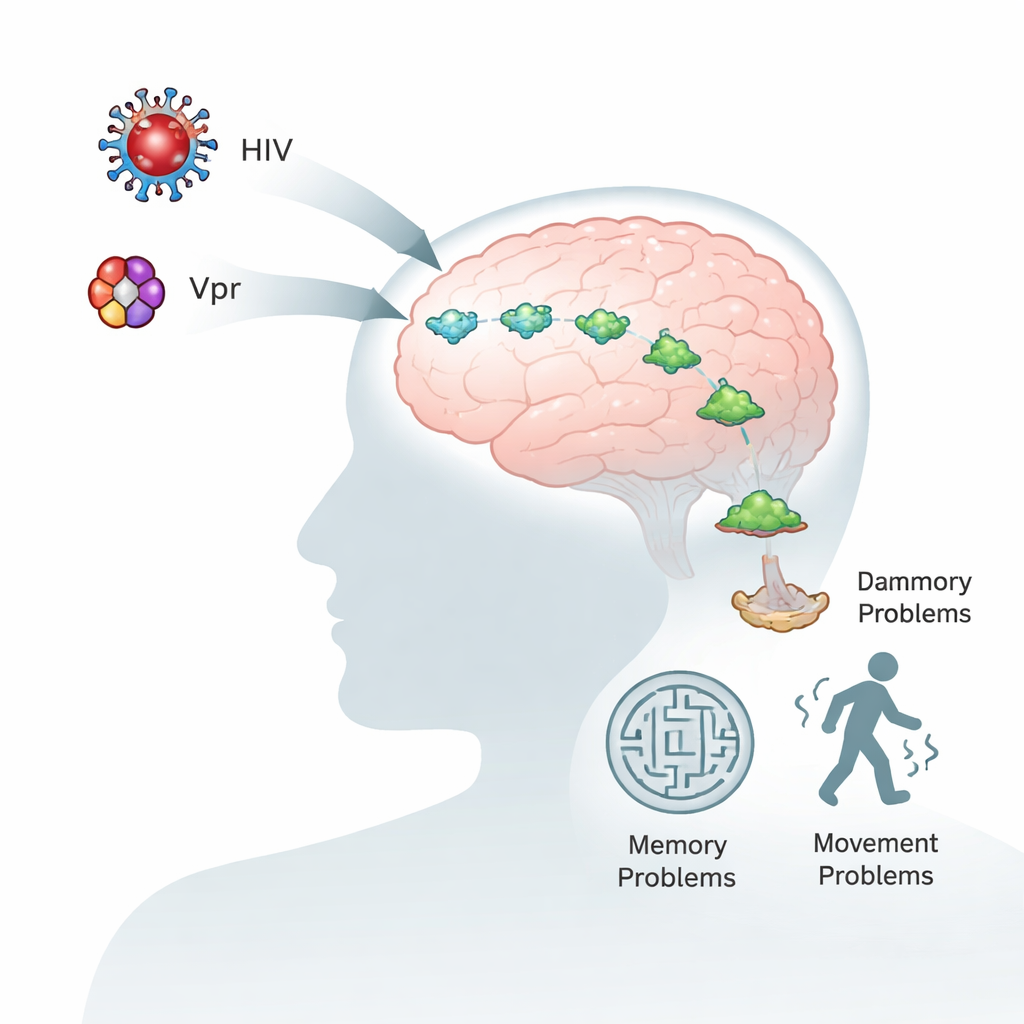
Una proteína cerebral en la encrucijada del VIH y el Parkinson
La alfa‑sinucleína es una proteína que ayuda a las neuronas a comunicarse, especialmente en regiones cerebrales que controlan el movimiento y la memoria. Cuando se acumula demasiada alfa‑sinucleína, se agrupa en agregados que dañan las sinapsis, tensionan las mitocondrias productoras de energía y alimentan la inflamación. Tales agregados son una característica de la enfermedad de Parkinson. Los autores muestran que la alfa‑sinucleína también se acumula con el envejecimiento normal en ratones, y que la proteína Vpr del VIH eleva sus niveles aún más en células con aspecto neuronal. Esto sitúa a la alfa‑sinucleína en la intersección entre los problemas cognitivos relacionados con el VIH y los trastornos clásicos del movimiento.
Cómo una proteína viral reescribe la “puntuación” celular
Cada célula usa etiquetas químicas en el ADN—descritas a menudo como marcas de puntuación molecular—para encender o apagar genes. En este trabajo, el equipo se centró en un interruptor de control poco conocido dentro del gen de la alfa‑sinucleína llamado promotor antisentido. En células sanas, este interruptor está fuertemente marcado con grupos metilo, manteniéndolo relativamente silencioso. Los investigadores encontraron que Vpr elimina estas marcas en sitios específicos de esta región, un proceso conocido como desmetilación. Una vez que se retiran esas marcas, el promotor antisentido se vuelve más activo y conduce a una producción adicional de alfa‑sinucleína, preparando el terreno para la agregación perjudicial.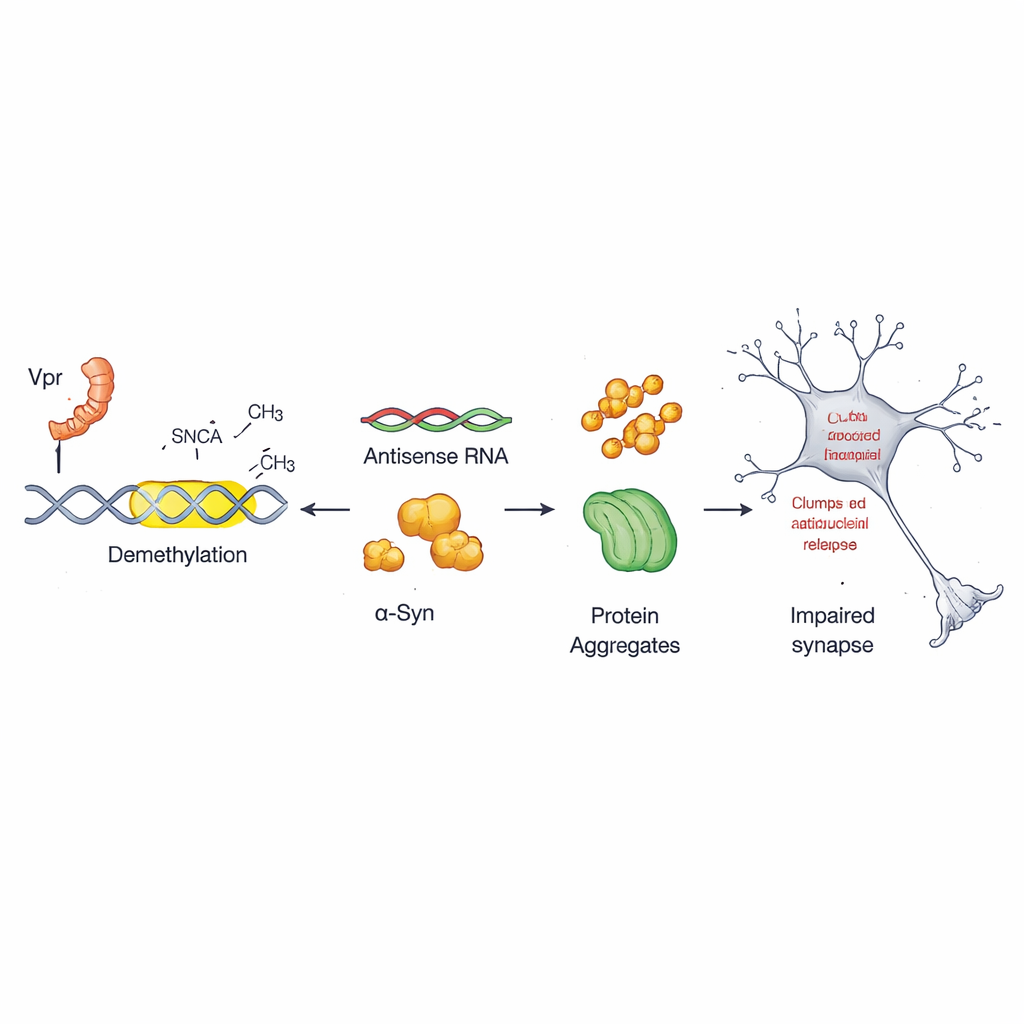
Pruebas en células, ratones y cerebros humanos
Usando células humanas con aspecto neuronal en cultivo y neuronas primarias de ratón, los autores demostraron que añadir Vpr aumenta con el tiempo los niveles del mensajero y de la proteína alfa‑sinucleína. Un fármaco que promueve de forma amplia la desmetilación del ADN mimetizó algunos de estos efectos, subrayando el papel del control epigenético. En contraste, un compuesto llamado DMOG, que bloquea las enzimas desmetilantes, impidió que Vpr activara plenamente el promotor antisentido. El equipo analizó entonces muestras cerebrales humanas de personas con y sin VIH. Los cerebros de donantes VIH‑positivos—tanto antes como después del tratamiento antirretroviral—tenían menos marcas de metilo en la misma región del ADN y niveles más altos de alfa‑sinucleína y de su transcrito antisentido, especialmente en donantes con demencia relacionada con el VIH. Esto sugiere que el virus deja una cicatriz epigenética duradera en el cerebro.
De los cambios moleculares a los problemas de memoria
Para vincular estos cambios moleculares con el comportamiento, los investigadores examinaron cómo Vpr afecta los circuitos cerebrales en ratones. Cuando aplicaron Vpr a cortes del hipocampo de ratón, una región vital para la memoria, la fuerza básica de la señal entre neuronas no cambió, pero se redujo la capacidad de fortalecer las conexiones—un proceso llamado potenciación a largo plazo. En ratones vivos, inyecciones dirigidas de Vpr en el hipocampo provocaron un peor rendimiento en una tarea de memoria espacial en la que los animales deben recordar la ubicación de objetos. En conjunto, estos experimentos sugieren que los cambios inducidos por Vpr en la alfa‑sinucleína no son meras curiosidades bioquímicas; se traducen en sinapsis debilitadas y déficits de memoria medibles.
Qué significa esto para las personas que viven con VIH
Este estudio propone una cadena clara de eventos: el VIH libera Vpr, Vpr reprograma un interruptor clave del ADN que controla la alfa‑sinucleína, la proteína se acumula y forma agregados, y las neuronas pierden gradualmente su capacidad de comunicarse y mantener la memoria. Dado que problemas similares de alfa‑sinucleína subyacen en la enfermedad de Parkinson, el trabajo sugiere que el VIH y las enfermedades neurodegenerativas clásicas comparten mecanismos solapados. De forma importante, los hallazgos destacan posibles estrategias nuevas—como fármacos que estabilicen la metilación del ADN en el promotor antisentido o que limiten la acumulación de alfa‑sinucleína—para frenar o prevenir el deterioro cognitivo y los problemas de movimiento relacionados con el VIH.
Cita: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Palabras clave: Trastornos neurocognitivos asociados al VIH, alfa-sinucleína, epigenética, metilación del ADN, Síntomas tipo Parkinson