Clear Sky Science · es
Rediseño racional de una DNAasa G-cuádruplex de alta actividad mediante bases flanqueantes y de bucle
Pequeñas máquinas de ADN con gran potencial
Imagínese sustituir enzimas proteicas frágiles por minúsculas hebras de ADN que resisten el calor, los productos químicos y el manejo brusco, y aun así realizan química útil. Este estudio explora exactamente esa idea. Los investigadores modifican estructuras especiales de ADN para que se comporten como pequeñas enzimas limpiadoras, capaces de usar peróxido de hidrógeno para generar una señal intensa. Estas “máquinas” de ADN, más resistentes y rápidas, podrían abaratar y hacer más fiables las pruebas médicas, los sensores ambientales y los diagnósticos portátiles, además de facilitar su uso fuera del laboratorio.
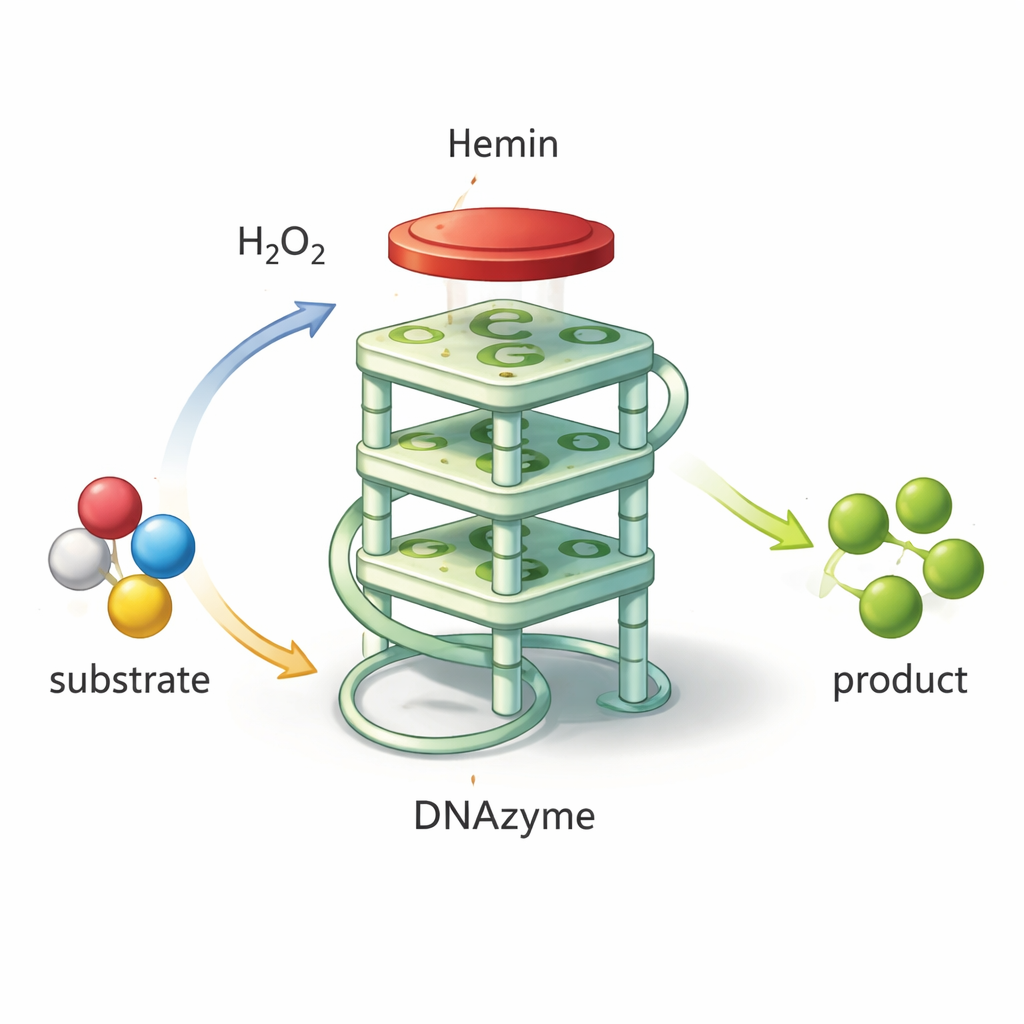
Convertir el ADN en una herramienta química diminuta
No todo el ADN es únicamente un portador pasivo de información genética. Ciertas secuencias cortas pueden plegarse en formas inusuales que atrapan moléculas específicas o incluso aceleran reacciones químicas. Una de esas formas es el G‑cuádruplex, en el que el ADN rico en guaninas se pliega en una pila compacta de cuatro capas. Cuando una pequeña molécula que contiene hierro llamada hemina se apoya sobre esta pila, el conjunto actúa como una “DNAasa”: un catalizador basado en ADN que imita a las peroxidasas naturales. Puede usar peróxido de hidrógeno para oxidar un reactivo que forma color, produciendo una señal verde intensa fácil de medir. Debido a que estas DNAzas son baratas de fabricar, muy estables y sencillas de rediseñar, son elementos prometedores para biosensores que detecten patógenos, toxinas o marcadores de enfermedad.
Por qué las DNAzas actuales necesitan una mejora
A pesar de su potencial, la mayoría de las DNAzas siguen siendo más lentas y menos eficientes que las enzimas proteicas naturales. Los biosensores existentes a menudo deben amplificar la diana mediante técnicas como la PCR o añadir reactivos auxiliares, lo que aumenta el coste y la complejidad. Intentos previos para mejorar las DNAzas han incluido enlazar dos unidades de ADN, fijar la hemina de forma permanente o rodear el sitio reactivo con grupos químicos adicionales. Estos trucos a veces ayudan, pero también pueden introducir volumen que estorba o exigir una química elaborada. Una cuestión clave ha sido cómo cambios sencillos en las bases de ADN cercanas—especialmente los que no rompen la forma central del G‑cuádruplex—podrían ajustar la actividad de manera predecible y “diseñable”.
Rediseñando una DNAasa de alto rendimiento
El equipo se centró en una DNAasa particularmente activa conocida como B730, que ya figura entre los mejores catalizadores de G‑cuádruplex no modificados. Alteraron sistemáticamente el ADN justo fuera de su núcleo, añadiendo o reposicionando bases comunes como adenina, timina y citosina en las regiones de bucle y cola. Una versión rediseñada, llamada B730‑1.2, combinó adeninas añadidas en los bucles con un par timina–citosina corto en un extremo de la hebra. En condiciones moderadas de peróxido de hidrógeno, esta variante triplicó la velocidad inicial de la reacción y aumentó aproximadamente cuatro veces la cantidad total de producto coloreado en comparación con la B730 original. Además, superó claramente a otras dos DNAzas bien conocidas, AS1411 y CatG4, cuando se probaron lado a lado.
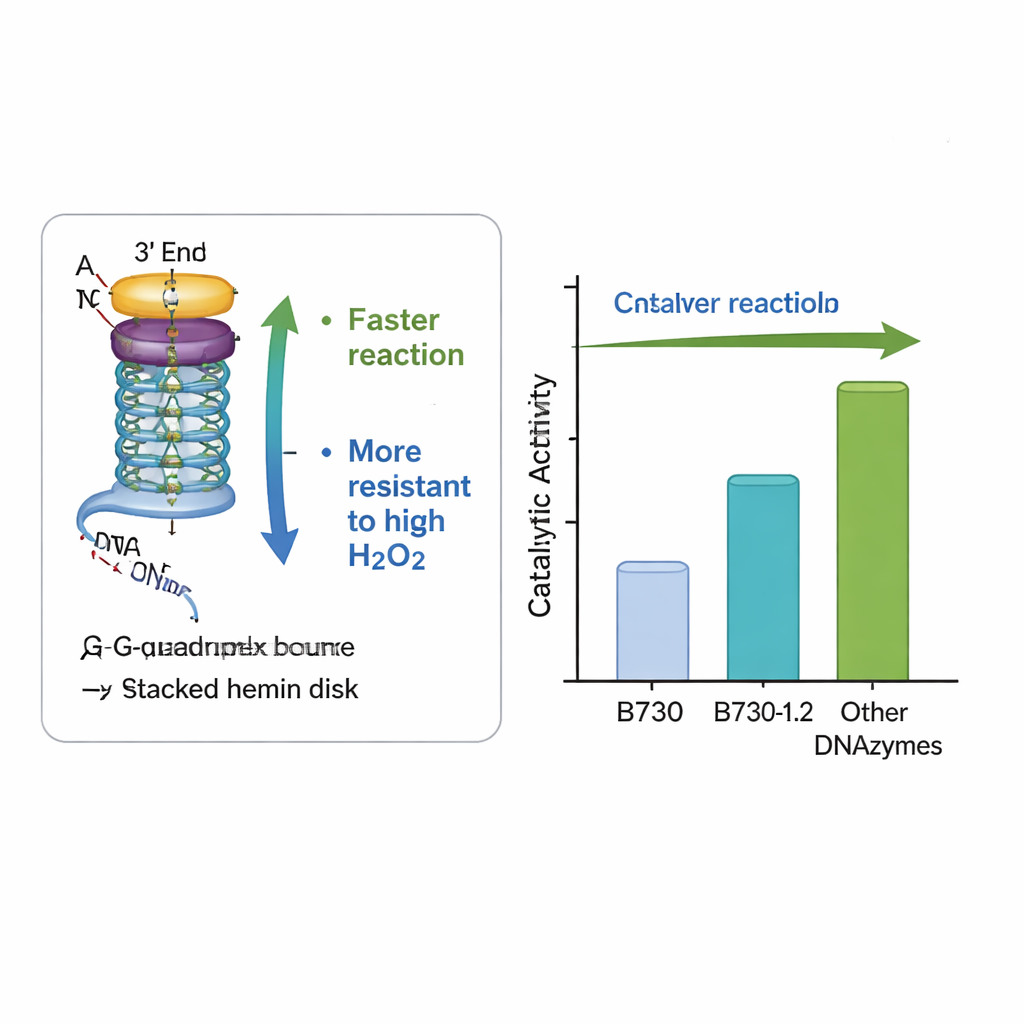
Diseñada para soportar condiciones adversas
Un obstáculo práctico importante para peroxidasas naturales y artificiales es que niveles altos de peróxido de hidrógeno, el ingrediente que impulsa la reacción, pueden destruir la enzima y detener el proceso. La DNAasa rediseñada B730‑1.2 mostró una notable resistencia: mantuvo e incluso incrementó su actividad a niveles de peróxido que normalmente inactivan sistemas similares. Mediciones de absorción de luz confirmaron que el ADN modificado ayudó a formar más rápidamente el intermedio reactivo clave—el denominado Compuesto I—sin alterar la forma general del G‑cuádruplex. En otras palabras, cambios sutiles en las bases circundantes crearon un entorno local más favorable para la química, acelerando los pasos útiles mientras ayudaban a proteger el centro catalítico de la autodestrucción.
Qué significa esto para sensores futuros
Para un lector no especialista, el mensaje es sencillo: ajustando cuidadosamente apenas unas pocas “letras” a ambos lados de una DNAasa ya buena, los autores obtuvieron una versión que funciona más rápido y sigue operativa en condiciones más duras. Su estrategia de modificar las bases flanqueantes y de bucle ofrece una receta simple y de bajo coste para construir catalizadores basados en ADN más potentes sin recurrir a modificaciones químicas complejas. Estas DNAzas robustas y eficientes podrían convertirse en el corazón de las próximas tiras reactivas y dispositivos portátiles que conviertan rápidamente señales biológicas invisibles—como trazas de virus o contaminantes—en cambios de color fáciles de leer.
Cita: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Palabras clave: DNAasa G-cuádruplex, mímico de peroxidasa, biosensores, ingeniería de aptámeros, catálisis con peróxido de hidrógeno