Clear Sky Science · es
Investigación de líquidos iónicos basados en Acoramidis como posibles estabilizadores de transtiretina mediante cálculos DFT, acoplamiento molecular y estudios ADMET
Por qué es tan difícil crear una pastilla para una enfermedad cardíaca rara
La amiloidosis por transtiretina (ATTR) es una enfermedad grave en la que una proteína sanguínea se acumula en el corazón y en los nervios, dañándolos lentamente. Un fármaco nuevo, Acoramidis, puede ayudar a detener esta acumulación, pero existe un problema práctico: el fármaco no se disuelve bien en agua, lo que dificulta su absorción cuando se administra en forma de pastilla. Este estudio explora una estrategia ingeniosa para rediseñar Acoramidis en nuevas formas tipo sal, llamadas líquidos iónicos, que podrían hacer el medicamento más fácil de tragar y más eficaz.
Convertir un fármaco prometedor en una forma bebible
Para que una pastilla funcione, primero debe disolverse en los fluidos acuosos del estómago e intestinos, y luego atravesar la pared intestinal hacia el torrente sanguíneo. Acoramidis es eficaz estabilizando la proteína transtiretina (TTR), lo que ayuda a prevenir los agregados proteicos perjudiciales relacionados con la ATTR, pero presenta baja solubilidad y escasa biodisponibilidad oral. Los investigadores se propusieron abordar esto emparejando químicamente Acoramidis con distintas moléculas compañeras cargadas, creando tres nuevas versiones de líquido iónico (IL1, IL2 e IL3). Estas versiones están diseñadas para comportarse más como sales fluidas que como cristales rígidos, lo que podría mejorar la disolución del fármaco y su distribución en el organismo. 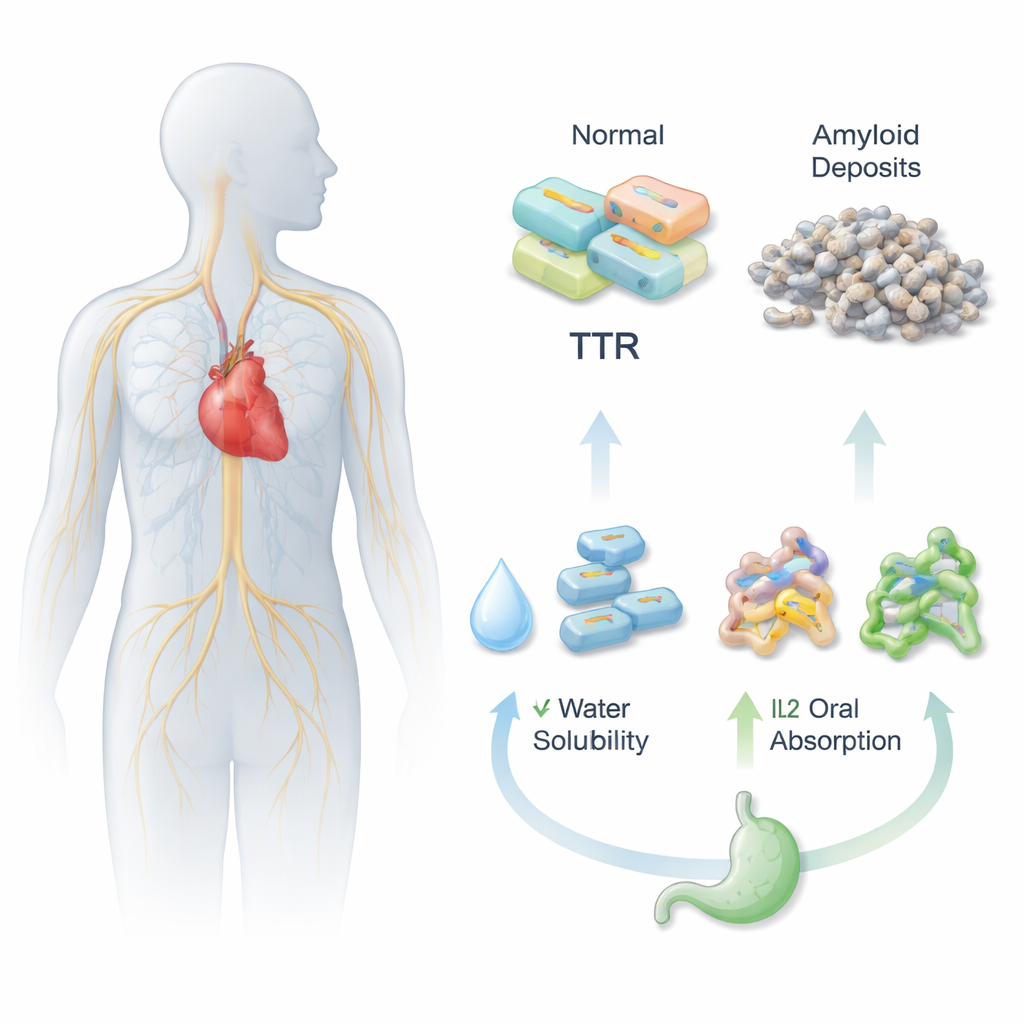
Explorando las nuevas moléculas por ordenador
En lugar de recurrir directamente a pruebas en animales o humanos, el equipo usó métodos computacionales avanzados para predecir el comportamiento de estas nuevas formas. Cálculos de química cuántica estimaron cuán polar es cada molécula —un predictor clave de la solubilidad en agua— y cuán fácilmente se desplazan sus electrones, lo que se relaciona con cómo podrían interactuar con proteínas. IL1 destacó por tener el momento dipolar más alto y la mayor respuesta electrónica, lo que indica que debería disolverse mejor en agua y formar contactos más fuertes y flexibles con sus dianas. Los cálculos de energía también sugirieron que IL1 es más estable térmicamente que el fármaco original y que los otros dos líquidos iónicos, lo que significa que sería menos propenso a descomponerse antes de alcanzar su destino.
Qué tan fuerte puede sujetar el fármaco a su diana
A continuación, los investigadores emplearon acoplamiento molecular, una prueba virtual de “cerradura y llave”, para ver qué tan bien encajan Acoramidis y sus tres formas iónicas en el canal de unión de la proteína TTR. Las cuatro moléculas se acoplaron en la región correcta de TTR, pero IL1 formó la unión más estrecha, con la energía de unión más favorable y varios contactos estabilizadores —particularmente enlaces de hidrógeno— con aminoácidos clave de la proteína. Esta unión más fuerte sugiere que IL1 podría ser incluso mejor que el fármaco parental para mantener a la TTR en su estructura segura de cuatro subunidades, ayudando a prevenir la ruptura y el mal plegamiento que conducen a los depósitos amiloides.
¿El organismo absorberá y eliminará estas nuevas formas?
Finalmente, el equipo utilizó herramientas farmacológicas en línea para sondear cómo podría manejar el organismo estos compuestos: qué tan bien se disuelven, atraviesan la pared intestinal, circulan en la sangre y se eliminan. Las tres formas iónicas se predijeron más solubles en agua que Acoramidis, siendo IL3 la que mostró la mayor solubilidad bruta. Las medidas de permeabilidad intestinal y la absorción oral global mejoraron para los tres líquidos iónicos, con IL1 e IL2 ofreciendo el mejor equilibrio entre penetración intestinal y biodisponibilidad predicha. La unión a proteínas en sangre, las tasas de eliminación y las semividas también cambiaron en sentidos que sugieren que las formas de líquido iónico podrían ofrecer una exposición más confiable tras la administración oral, con IL1 presentando de nuevo un perfil particularmente favorable. 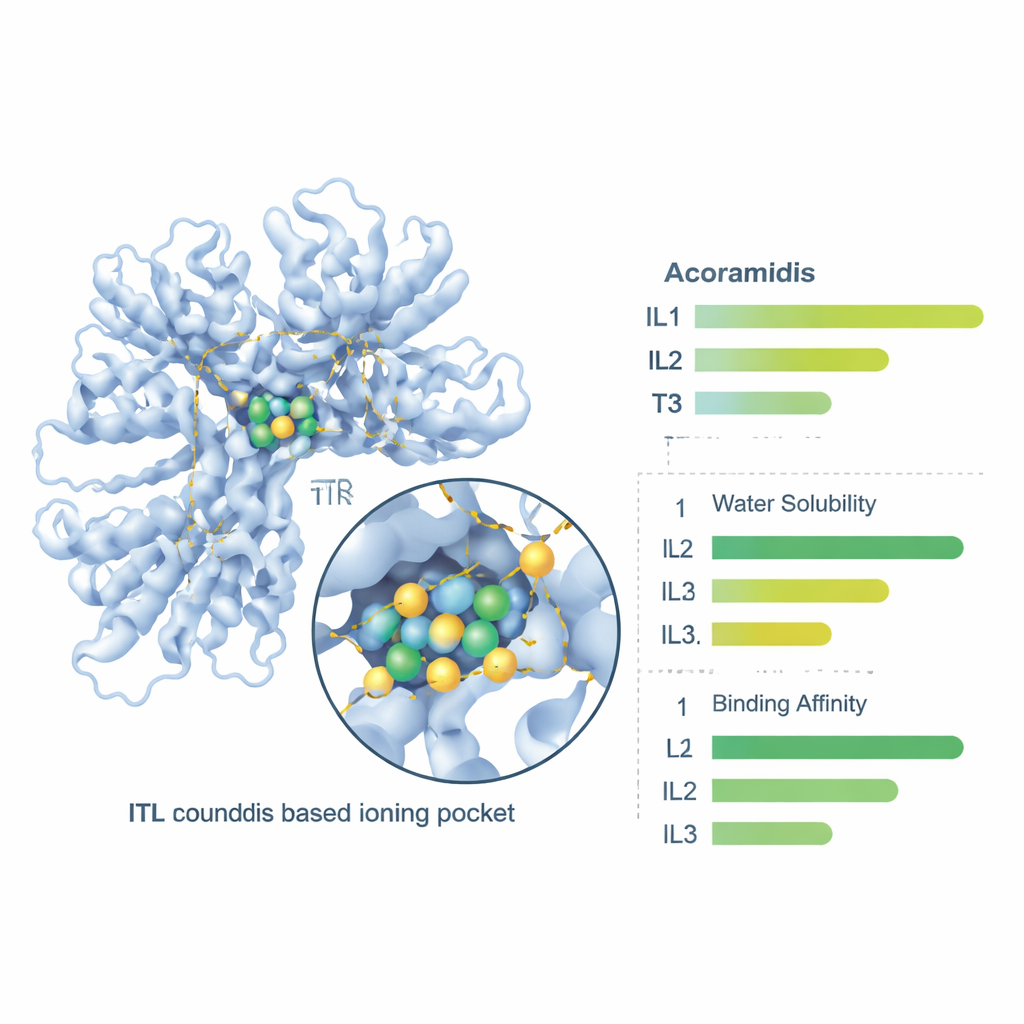
Qué podría significar esto para futuros tratamientos de la ATTR
Para un lector no especializado, el mensaje principal es que el fármaco Acoramidis ya parece prometedor para una enfermedad cardíaca y nerviosa rara pero grave, aunque su baja solubilidad limita su eficacia por vía oral. Al convertir Acoramidis en líquidos iónicos especialmente diseñados, este estudio muestra —totalmente mediante pruebas computacionales— que podría ser posible crear versiones que se disuelvan mejor, se unan con mayor fuerza a su proteína diana y se absorban de forma más eficiente. Entre los tres candidatos, IL1 parece alcanzar el mejor equilibrio entre estabilidad, afinidad de unión, solubilidad y absorción oral predicha, lo que lo sitúa como un sólido candidato para futuros desarrollos en laboratorio y ensayos clínicos orientados a ofrecer tratamientos más eficaces y fáciles de tomar para la ATTR.
Cita: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Palabras clave: amiloidosis por transtiretina, Acoramidis, líquidos iónicos, desplegamiento proteico, administración oral de fármacos