Clear Sky Science · es
Diseño in silico de una vacuna multi‑epítopo dirigida a DENV‑1 y DENV‑3
Por qué las vacunas contra el dengue siguen siendo importantes
La fiebre del dengue ya no es una enfermedad tropical rara; hoy amenaza a miles de millones de personas en más de 100 países y desborda regularmente los hospitales en partes de Asia, América Latina y otras regiones. Sin embargo, aun con dos vacunas autorizadas en el mercado, la protección es desigual, especialmente en personas que nunca han tenido dengue y en regiones donde circulan varios serotipos al mismo tiempo. Este estudio plantea una pregunta vigente: ¿puede el diseño guiado por ordenador ayudarnos a construir una vacuna más segura y precisa, dirigida específicamente a co‑infecciones peligrosas con dos serotipos de dengue que suelen presentarse juntos?
Dos serotipos escurridizos y por qué son problemáticos
El virus del dengue existe en cuatro versiones, llamadas serotipos DENV‑1 a DENV‑4. La infección con cualquiera de ellos puede causar fiebre alta, dolor intenso y, en algunos casos, hemorragias o shock potencialmente mortales. Preocupantemente, enfermarse por segunda vez con un serotipo distinto puede a veces empeorar la enfermedad en lugar de mejorarla, porque anticuerpos existentes pueden facilitar la entrada del nuevo virus en las células, un proceso llamado potenciación dependiente de anticuerpos. En brotes recientes, los médicos han reportado pacientes infectados simultáneamente con DENV‑1 y DENV‑3, una combinación asociada a enfermedad más grave y a resultados de pruebas confusos. Las vacunas actuales no protegen de forma fiable a todos los grupos de edad y frente a todos los serotipos, especialmente en personas sin exposición previa, lo que deja una brecha peligrosa en la defensa.
Diseñar una vacuna desde la molécula
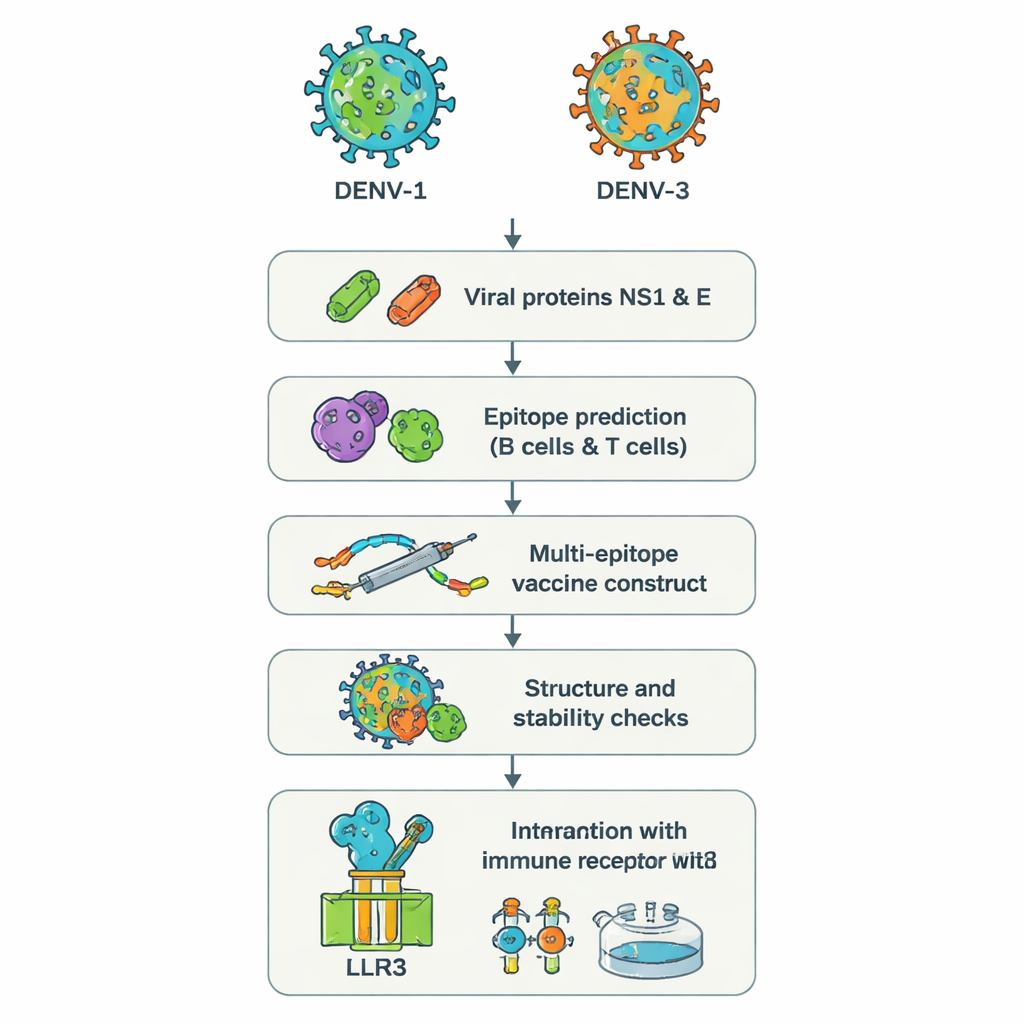
En lugar de cultivar virus enteros en el laboratorio, los investigadores emplearon un enfoque a veces llamado “vacunología inversa”. Partieron de las secuencias genéticas de dos proteínas del dengue, NS1 y E, de DENV‑1 y DENV‑3. Estas proteínas son clave para la invasión celular del virus y la forma en que el sistema inmunitario lo reconoce. Potentes herramientas en línea escanearon las secuencias proteicas para localizar fragmentos cortos —epítopos— que tienen mayor probabilidad de ser reconocidos por células B humanas (que producen anticuerpos) y células T (que eliminan células infectadas y coordinan respuestas). De cientos de candidatos, el equipo seleccionó un conjunto pequeño predicho como altamente visible para el sistema inmunitario, compartido entre los dos serotipos y capaz de desencadenar señales antivirales útiles como el interferón‑gamma.
Construir una única molécula vacuna multifuncional
Los epítopos elegidos se ensamblaron digitalmente en una larga proteína artificial, una vacuna “multi‑epítopo”. Cortos enlazadores de aminoácidos actúan como espaciadores flexibles para que cada epítopo mantenga su conformación y siga siendo accesible a las células inmunitarias. Se añadió una pieza extra, basada en un péptido antimicrobiano humano natural denominado beta‑defensina, como adyuvante para potenciar la respuesta global. El análisis computacional predijo que el constructo final, con 575 aminoácidos, sería estable, hidrófilo (y por tanto más fácil de disolver) y poco probable que actúe como alergeno. Herramientas adicionales de predicción de estructura generaron un modelo tridimensional y verificaron que la mayoría de los bloques estructurales ocupaban posiciones realistas, similares a las observadas en proteínas conocidas.
Probar el candidato dentro de un cuerpo virtual
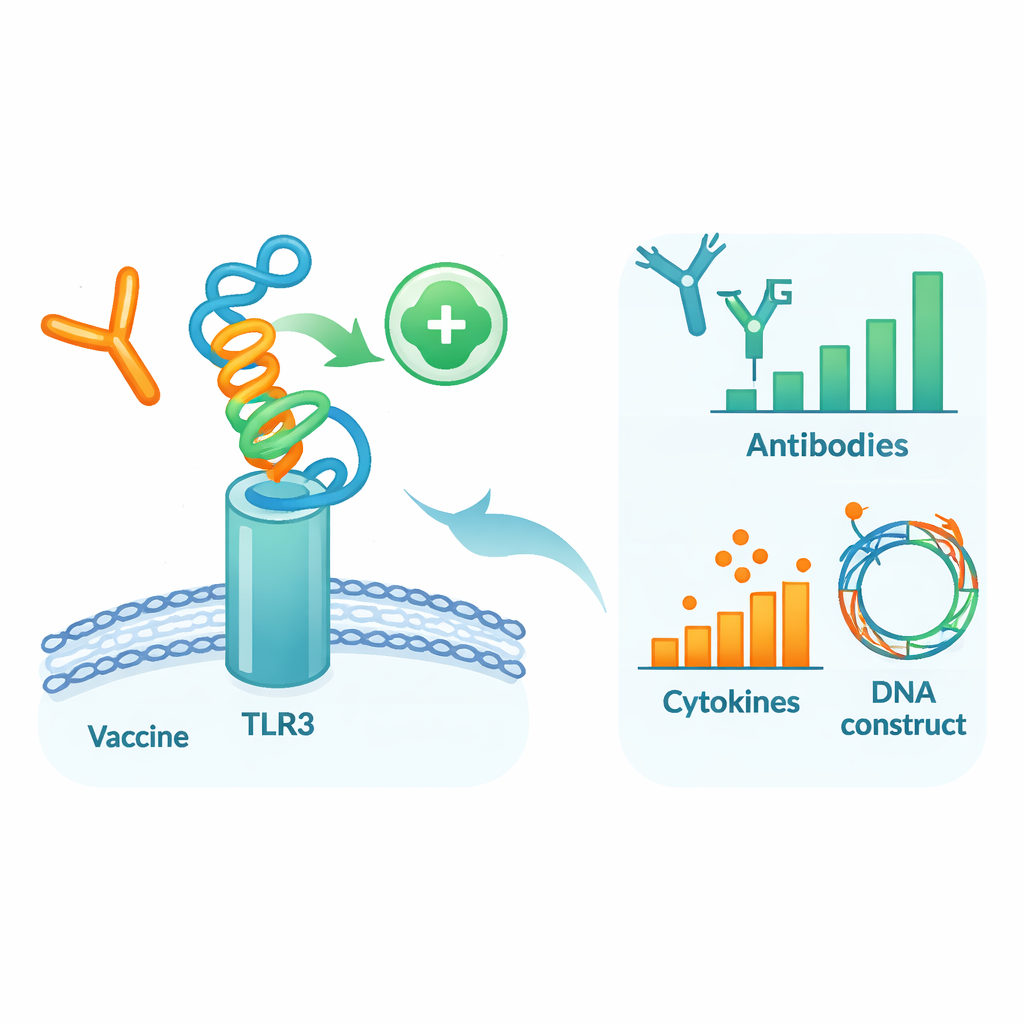
Para evaluar cómo podría comportarse esta proteína diseñada en un entorno similar al humano, los autores realizaron una serie de simulaciones computacionales detalladas. Primero, acoplaron el modelo de la vacuna al TLR3, una proteína sensora en células inmunitarias que detecta material viral y ayuda a lanzar las defensas tempranas. Las simulaciones de dinámica molecular —películas virtuales de átomos en movimiento— sugirieron que la vacuna y el TLR3 forman un complejo estable, respaldado por energías de unión favorables y numerosas interacciones por puente de hidrógeno. Análisis adicionales de movimiento y energía señalaron regiones específicas de ambas moléculas que actúan como “puntos calientes” de contacto. A continuación, se usó un simulador del sistema inmunitario para imitar tres dosis de vacuna a lo largo de varios meses. El sistema inmunitario virtual produjo fuertes oleadas de anticuerpos IgG protectores, memoria duradera de células B y T, y moléculas de señalización coherentes con una respuesta antiviral robusta.
Del modelo computacional al plano listo para el laboratorio
Finalmente, los investigadores adaptaron el código genético de la vacuna para una producción eficiente en microbios de laboratorio comunes e insertaron con éxito esta secuencia de ADN optimizada en un plásmido de expresión estándar, listo para futuras pruebas experimentales. En términos sencillos, su trabajo entrega un plano detallado para una nueva vacuna contra el dengue que apunta a fragmentos cuidadosamente seleccionados de DENV‑1 y DENV‑3, que se predice será estable y segura y debería implicar fuertemente a ambos brazos del sistema inmunitario. Aunque estos resultados son puramente computacionales y deben confirmarse en células, animales y, finalmente, en personas, muestran cómo la bioinformática moderna puede generar con rapidez candidatos vacunales diseñados para problemas complejos como la co‑infección por dengue.
Cita: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Palabras clave: vacuna contra el dengue, multi‑epítopo, DENV‑1, DENV‑3, inmunoinformática