Clear Sky Science · es
Análisis integrador de proteómica y metabolómica revela un trastorno del metabolismo de aminoácidos en células de leucemia mieloide aguda resistentes a la adriamicina
Por qué algunos fármacos contra la leucemia dejan de funcionar
La quimioterapia ha transformado el tratamiento de la leucemia mieloide aguda (LMA), un cáncer de la sangre de crecimiento rápido. Sin embargo, muchos pacientes ven que su enfermedad reaparece porque las células cancerosas aprenden a sobrevivir a los mismos fármacos diseñados para matarlas. Este estudio plantea una pregunta sencilla pero crucial: ¿qué cambia dentro de las células leucémicas cuando se vuelven resistentes a la adriamicina, uno de los fármacos quimioterápicos estándar, y podrían esos cambios señalar nuevas maneras de restaurar la eficacia del tratamiento?
Espiando dentro de las células leucémicas
Para explorar esto, los investigadores compararon una línea celular humana de LMA común, llamada HL60, con una línea hermana que se había vuelto resistente a la adriamicina (HL60/R). En lugar de mirar un solo gen o proteína a la vez, usaron dos enfoques amplios y complementarios. La proteómica midió miles de proteínas diferentes: las moléculas ejecutoras que realizan la mayoría de las tareas en la célula. La metabolómica midió cientos de pequeñas moléculas que conforman el metabolismo celular, incluidos lípidos, azúcares y aminoácidos. Al combinar estas capas "ómicas", el equipo construyó un panorama detallado de cómo las células resistentes difieren de sus contrapartes aún sensibles.
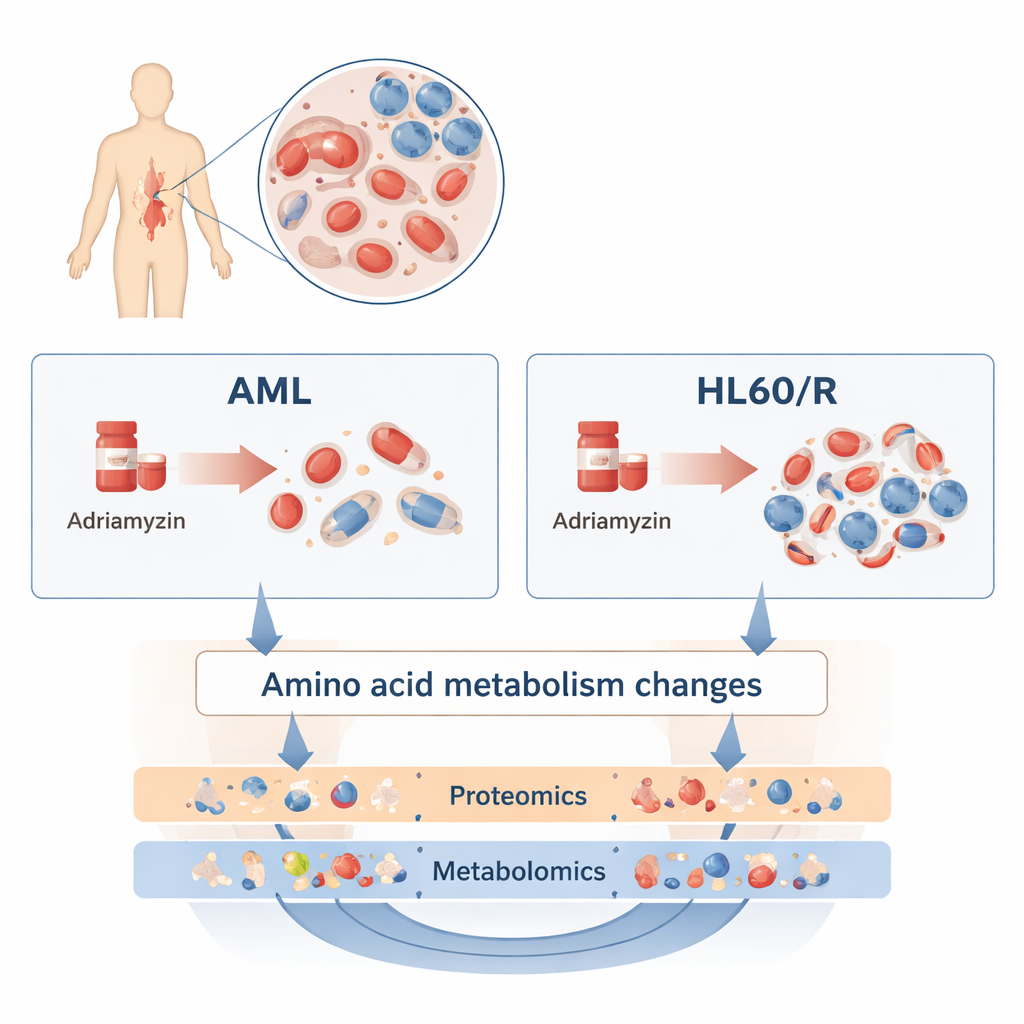
Reconfiguración masiva de la maquinaria celular
La investigación proteómica reveló cambios de gran alcance: más de 3.200 proteínas estaban presentes en niveles más altos o más bajos en las células resistentes a la adriamicina en comparación con las células HL60 normales. Muchas de estas proteínas se agruparon en vías que controlan cómo las células usan la energía y responden al estrés. En particular, se alteraron proteínas de la vía de señalización cAMP, la vía HIF‑1 (que ayuda a las células a afrontar bajos niveles de oxígeno) y la fosforilación oxidativa (un proceso principal de producción de energía en las mitocondrias). Estos cambios sugieren que las células leucémicas resistentes reprograman cómo respiran, crecen y se comunican entre sí para resistir la quimioterapia.
El metabolismo se orienta hacia los aminoácidos
El análisis metabolómico contó una historia complementaria. De alrededor de 1.400 metabolitos detectados, 260 cambiaron significativamente en las células resistentes. Modelos estadísticos separaron claramente las células resistentes de las no resistentes, lo que indica una firma metabólica consistente de resistencia. Cuando los metabolitos alterados se mapearon en rutas bioquímicas conocidas, destacaron varias vías. Muchas de las rutas más afectadas estaban vinculadas a aminoácidos, los bloques de construcción de las proteínas, especialmente las relacionadas con alanina, aspartato, glutamato, cisteína, metionina y glutatión. Otras redes, como el metabolismo de purinas y pirimidinas (importante para ADN y ARN) y el manejo de ciertos lípidos, también se vieron perturbadas, subrayando que la resistencia está ligada a una amplia remodelación metabólica.
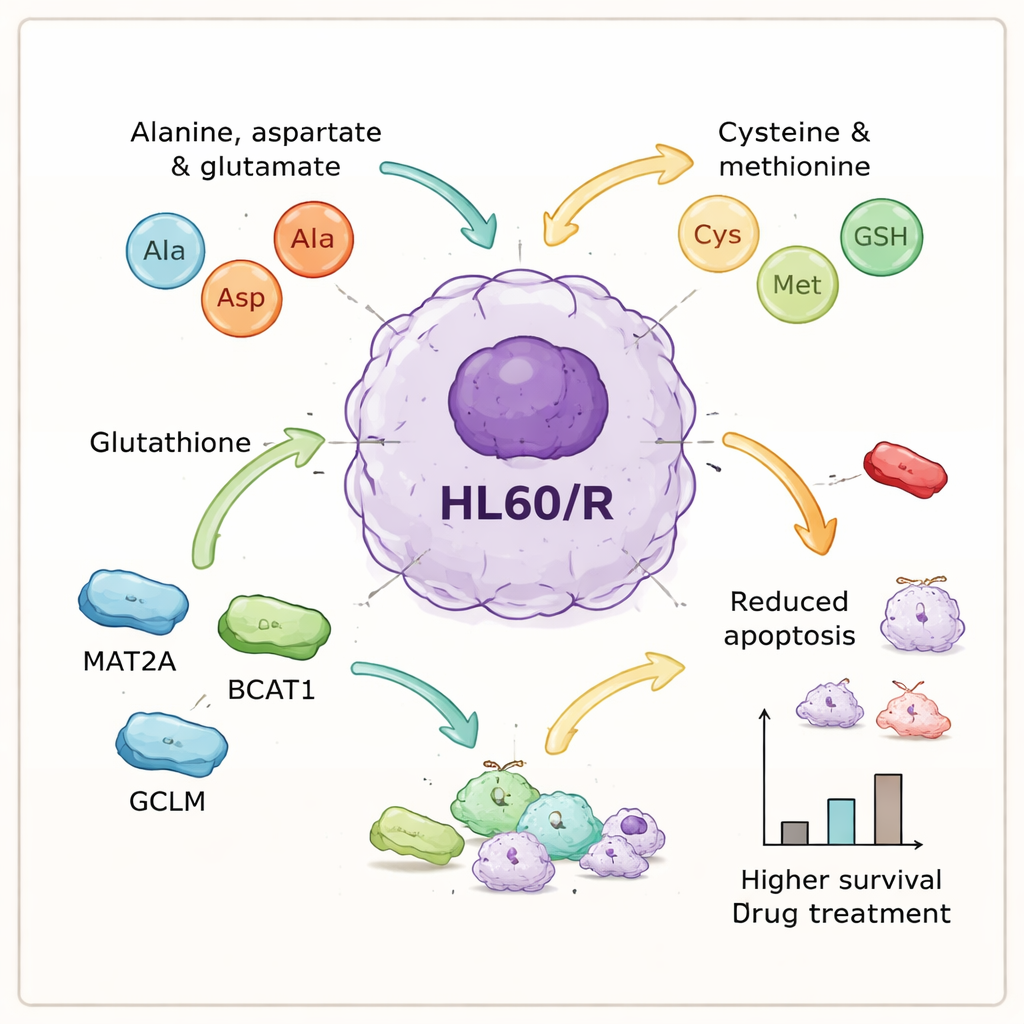
Actores moleculares clave que ayudan a las células cancerosas a perdurar
Al integrar los datos de proteínas y metabolitos, los autores identificaron un conjunto de procesos relacionados con aminoácidos que parecían centrales para la resistencia. Seleccionaron seis proteínas vinculadas a estas vías—GOT1, GPX1, AHCY, MAT2A, BCAT1 y GCLM—para una inspección más detallada. Las pruebas de laboratorio confirmaron que cinco de ellas eran más abundantes en las células resistentes, consistente con la idea de que el procesamiento de aminoácidos está potenciado, mientras que una enzima antioxidante, GPX1, estaba reducida. Para indagar causa y efecto, el equipo utilizó ARN de interferencia pequeño para reducir tres de las proteínas reguladas al alza—MAT2A, BCAT1 y GCLM—en las células resistentes. Cuando se silenciaron estas proteínas, las células experimentaron una muerte celular programada significativamente mayor tras el tratamiento, lo que significa que perdieron gran parte de su protección contra la adriamicina.
Qué implica esto para tratamientos futuros
En conjunto, estos hallazgos sugieren que las células de LMA resistentes a la adriamicina sobreviven no solo por mutaciones individuales, sino porque remodelan su química interna, con el metabolismo de aminoácidos como un centro clave. Al desviar más recursos hacia vías específicas de aminoácidos y glutatión, las células parecen estar mejor preparadas para manejar el estrés, reparar daños y evitar la muerte cuando se exponen a la quimioterapia. Para el público general, el mensaje clave es que la resistencia no es aleatoria: sigue patrones identificables que pueden medirse y, potencialmente, dirigirse. A largo plazo, los fármacos que interfieran con proteínas específicas del procesamiento de aminoácidos como MAT2A, BCAT1 o GCLM podrían combinarse con adriamicina u agentes similares, proporcionando a los clínicos nuevas herramientas para prevenir o superar la resistencia en pacientes con leucemia mieloide aguda.
Cita: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Palabras clave: leucemia mieloide aguda, resistencia a fármacos, adriamicina, metabolismo de aminoácidos, multi-ómica