Clear Sky Science · es
Un modelo celular funcional y robusto para el cribado de alto rendimiento de moduladores de piezo1
Por qué importan los diminutos sensores de presión en nuestras células
Cada vez que la sangre fluye por nuestros vasos o simplemente caminamos por una habitación, nuestras células perciben pequeñas fuerzas mecánicas. Una proteína clave de "sensor de presión" llamada Piezo1 ayuda a las células a transformar esas fuerzas en señales eléctricas y químicas que mantienen los tejidos sanos. Dado que Piezo1 participa en el crecimiento vascular, la resistencia ósea, la inmunidad y enfermedades genéticas raras, los desarrolladores de fármacos están interesados en encontrar moléculas que puedan ajustar su actividad. El artículo descrito aquí presenta una forma nueva y más rápida de buscar esas moléculas usando células diseñadas y lecturas basadas en luz en lugar de técnicas lentas y laboriosas.
Convertir el tacto en una señal luminosa
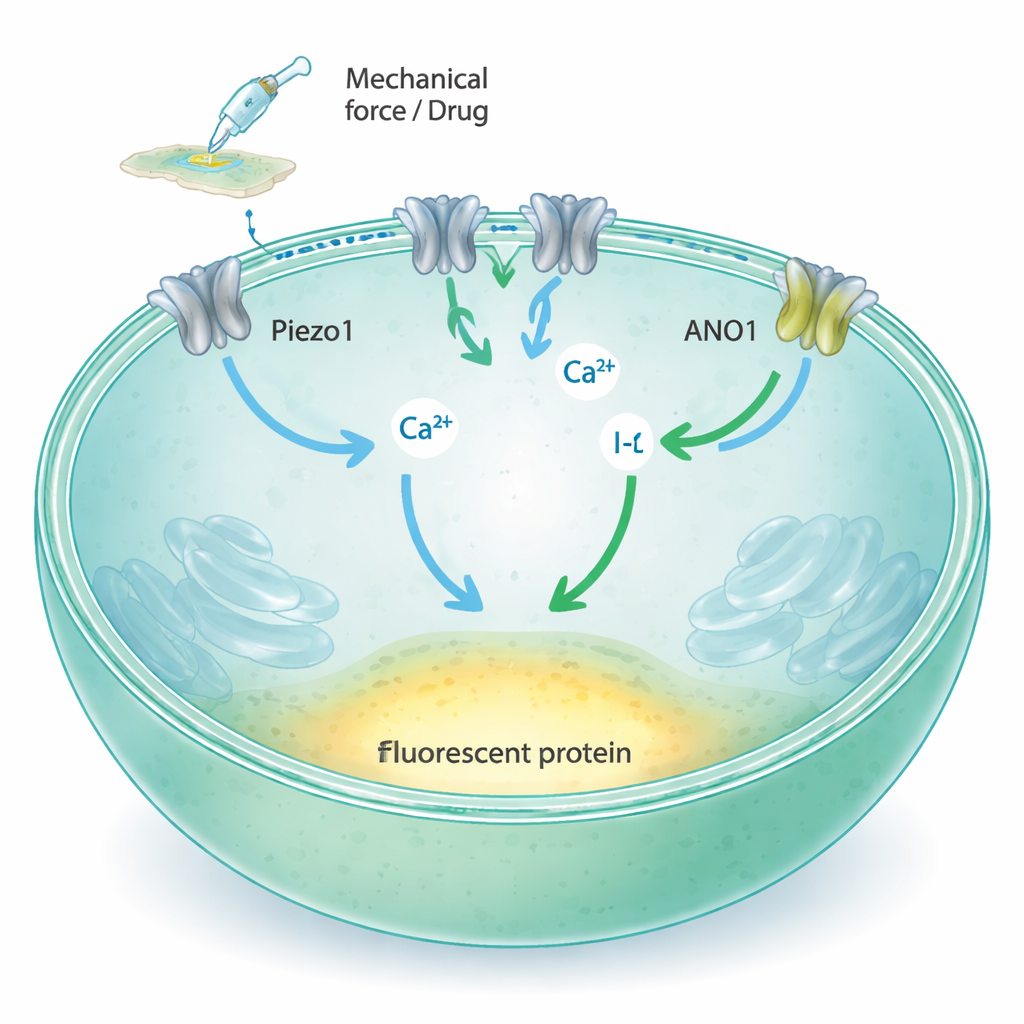
Piezo1 es un canal en la membrana celular que se abre cuando la membrana se estira o se presiona, permitiendo la entrada de calcio y otros iones al interior de la célula. Los métodos tradicionales para estudiar estos canales dependen de electrodos de vidrio finos o de sensores fluorescentes especializados, que son potentes pero difíciles de escalar a las decenas de miles de pruebas necesarias para el descubrimiento moderno de fármacos. Los autores propusieron convertir la actividad de Piezo1 en un cambio simple de luz que un lector de placas pueda medir rápidamente en muchas muestras a la vez. Su idea fue vincular Piezo1 a dos componentes adicionales: ANO1, otro canal iónico que responde al calcio, y una proteína fluorescente amarilla modificada que pierde brillo al exponerse a iones yoduro.
Construir una célula de ensayo sensible
Los investigadores partieron de células Fischer Rat Thyroid (FRT), que producen Piezo1 de forma natural y se adhieren bien a las placas de plástico estándar. Confirmaron que estas células expresan Piezo1 pero no su pariente cercano Piezo2, y demostraron que Piezo1 en estas células responde al flujo de fluido y al sondeo mecánico permitiendo la entrada de calcio. A continuación introdujeron el canal ANO1 y la proteína fluorescente sensible al yoduro (YFP‑H148Q/I152L) en las células. Cuando el calcio aumenta dentro de la célula, ANO1 se abre y permite la entrada de yoduro; la proteína fluorescente se atenúa a medida que el yoduro se acumula a su alrededor. Microscopía, citometría de flujo y registros eléctricos mostraron que tanto ANO1 como el sensor fluorescente estaban presentes en altos niveles y funcionaban según lo previsto.
De la acción del fármaco a un brillo mensurable
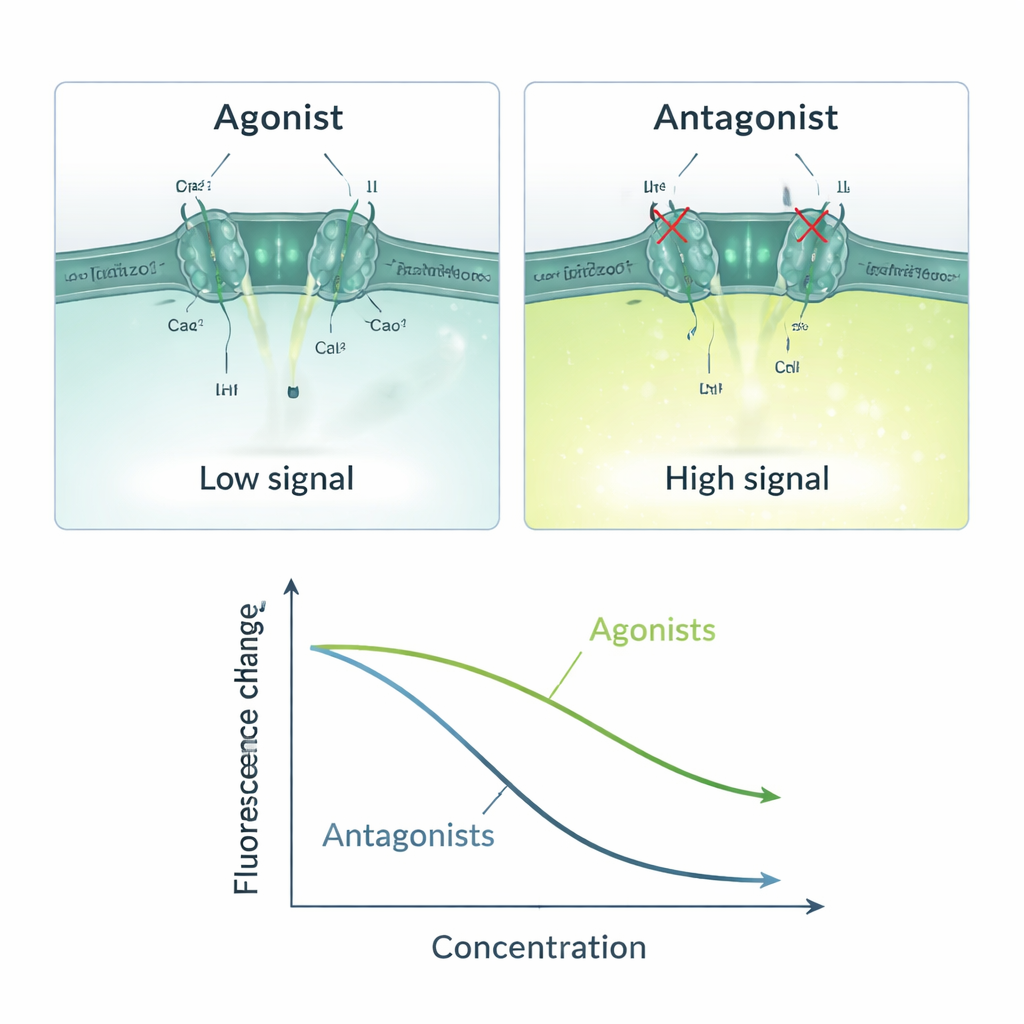
Con este sistema de tres partes en funcionamiento, el equipo creó una cadena simple de causa y efecto: si una molécula de prueba activa Piezo1, entra calcio, ANO1 se abre, entra yoduro y la señal de fluorescencia disminuye; si una molécula bloquea Piezo1, la señal permanece brillante. Validaron esta lógica usando activadores conocidos de Piezo1 (Yoda1, Jedi1, Jedi2) e inhibidores (Ruthenium Red, GsMTx4). Los activadores produjeron disminuciones dependientes de la dosis en la fluorescencia, con valores de sensibilidad acordes con datos previamente publicados. Los bloqueadores causaron el patrón opuesto, reduciendo la respuesta a medida que aumentaba su concentración. El ensayo funcionó solo cuando estaban presentes tanto el calcio como el yoduro, lo que subraya que la señal dependía realmente de la entrada de calcio impulsada por Piezo1 y la posterior entrada de yoduro mediada por ANO1. Medidas estadísticas como el factor Z y la relación señal‑ruido indicaron que el método es lo suficientemente estable y fiable para el cribado a escala industrial.
Pruebas rápidas y escalables con algunas salvedades
El nuevo modelo celular puede completar la medición de un pocillo en aproximadamente 14 segundos y escanear una placa de 96 pocillos en alrededor de 22 minutos, y puede adaptarse a instrumentos que leen cientos de pocillos simultáneamente. Las células diseñadas permanecen estables durante muchas generaciones bajo selección antibiótica, lo que permite repetir experimentos a lo largo del tiempo. Dado que la lectura es óptica y utiliza equipo estándar de microplacas, el enfoque es relativamente económico y accesible. Sin embargo, los autores señalan que su prueba es indirecta: cualquier compuesto que actúe en pasos anteriores o posteriores a Piezo1 en la cadena de señalización —por ejemplo, sobre ANO1 u otras proteínas que manejan el calcio— puede producir un falso positivo. Por esa razón, los compuestos identificados en este cribado aún requieren confirmación con métodos más directos como la electrofisiología.
Qué significa esto para futuros tratamientos
En términos cotidianos, los investigadores han construido una "alarma de humo" de laboratorio que parpadea menos luminosa cada vez que un compuesto empuja a Piezo1 a abrirse, y permanece brillante cuando Piezo1 está bloqueado. Esta alarma es sensible, rápida y fácil de ejecutar en grandes volúmenes, lo que la hace adecuada para la primera pasada en la búsqueda de fármacos que modulen los sensores mecánicos del cuerpo. Aunque no reemplazará las pruebas más detalladas de seguimiento, este modelo celular ofrece un punto de partida potente para descubrir moléculas que podrían, algún día, ayudar a tratar trastornos vasculares, enfermedades óseas, problemas inmunitarios y otras condiciones vinculadas a cómo nuestras células perciben y responden a la fuerza física.
Cita: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Palabras clave: Canal Piezo1, canales iónicos mecanosensibles, cribado de alto rendimiento, ensayo celular, descubrimiento de fármacos