Clear Sky Science · es
Síntesis, caracterización, análisis DFT, acoplamiento molecular e investigaciones anticancerígenas en carcinoma colorrectal de un nuevo complejo de zinc(II) pirozol-hidrazona
Por qué un fármaco basado en metal podría combatir el cáncer de colon con más suavidad
Muchos fármacos anticancerígenos potentes se construyen alrededor de metales pesados como el platino. Pueden ser efectivos, pero a menudo conllevan efectos secundarios severos y resistencia con el tiempo. Este estudio explora un enfoque distinto: un nuevo candidato a fármaco construido alrededor del zinc, un nutriente esencial ya presente en nuestro organismo, combinado con un andamiaje orgánico llamado pirozol–hidrazona. Los investigadores se preguntaron si unir zinc a este andamiaje podría crear un compuesto que ataque con fuerza las células de cáncer colorrectal mientras respeta las células sanas.
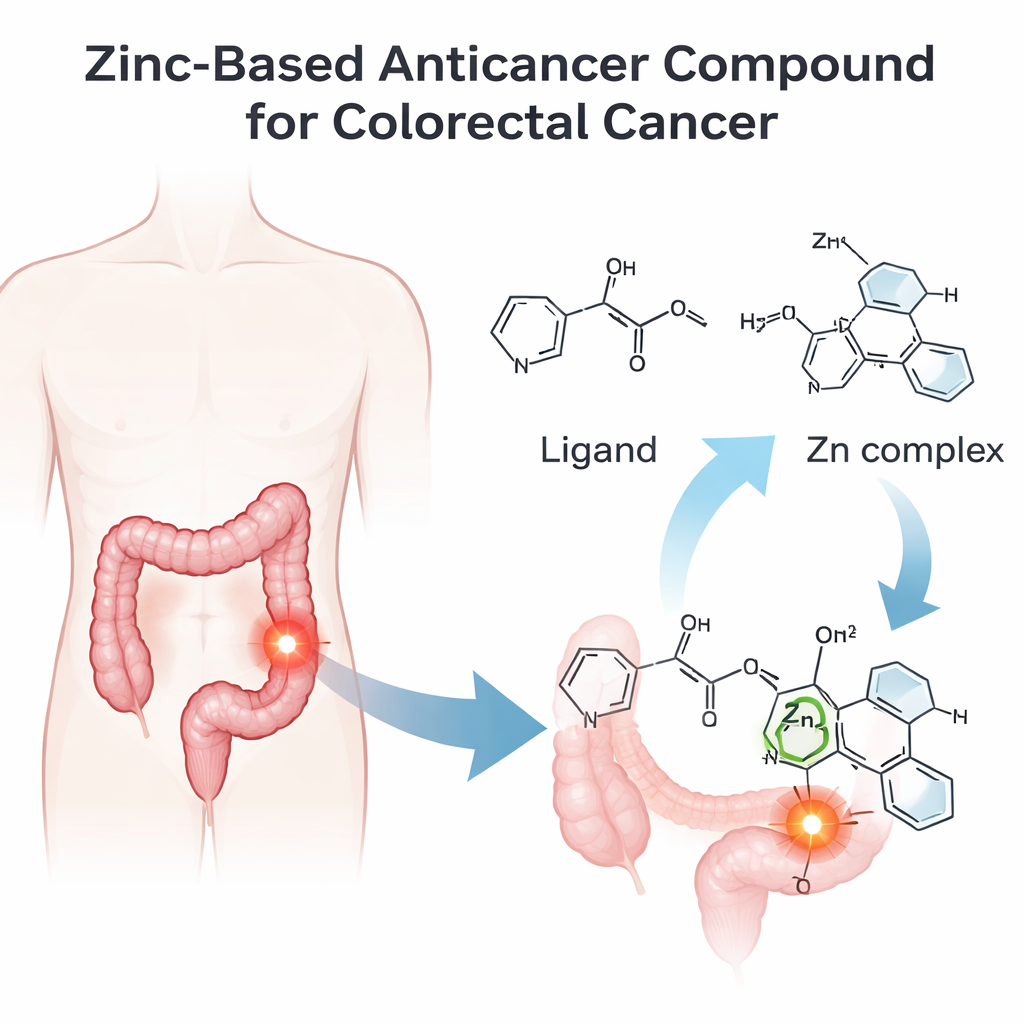
Construyendo una molécula de zinc más inteligente
El equipo diseñó y sintetizó primero una nueva molécula orgánica, denominada IMP, y luego la coordinó a un ion de zinc para obtener un complejo de zinc llamado IMP-Zn. Confirmaron la estructura exacta de ambos mediante una batería de técnicas que, en esencia, "huellan" las moléculas: espectroscopía infrarroja para identificar los enlaces químicos presentes, resonancia magnética nuclear para mapear la posición de los átomos, espectrometría de masas para verificar el peso molecular y espectroscopía ultravioleta–visible para estudiar la interacción de los compuestos con la luz. Estos experimentos, junto con pruebas de conductividad eléctrica, mostraron que el zinc está fuertemente coordinado a tres átomos clave en IMP y a dos iones cloruro, formando un complejo centrado en zinc único y bien definido.
Escrutando la molécula con química virtual
Para complementar las mediciones de laboratorio, los investigadores realizaron detalladas simulaciones por ordenador usando teoría del funcional de la densidad (DFT). Estos cálculos les permitieron predecir cómo se distribuyen los electrones en IMP y en IMP-Zn, qué tan estable es cada forma y con qué facilidad podrían participar las moléculas en reacciones químicas. Los resultados mostraron que, una vez unido el zinc, la brecha energética entre los orbitales "fronterizos" de la molécula se reduce, lo que significa que los electrones pueden moverse con más facilidad dentro de la estructura. Esto suele traducirse en una mayor reactividad química. El complejo de zinc también presentó un índice de electrofilicidad mayor, lo que sugiere que está mejor preparado para interactuar con dianas biológicas que el ligando libre IMP por sí solo.
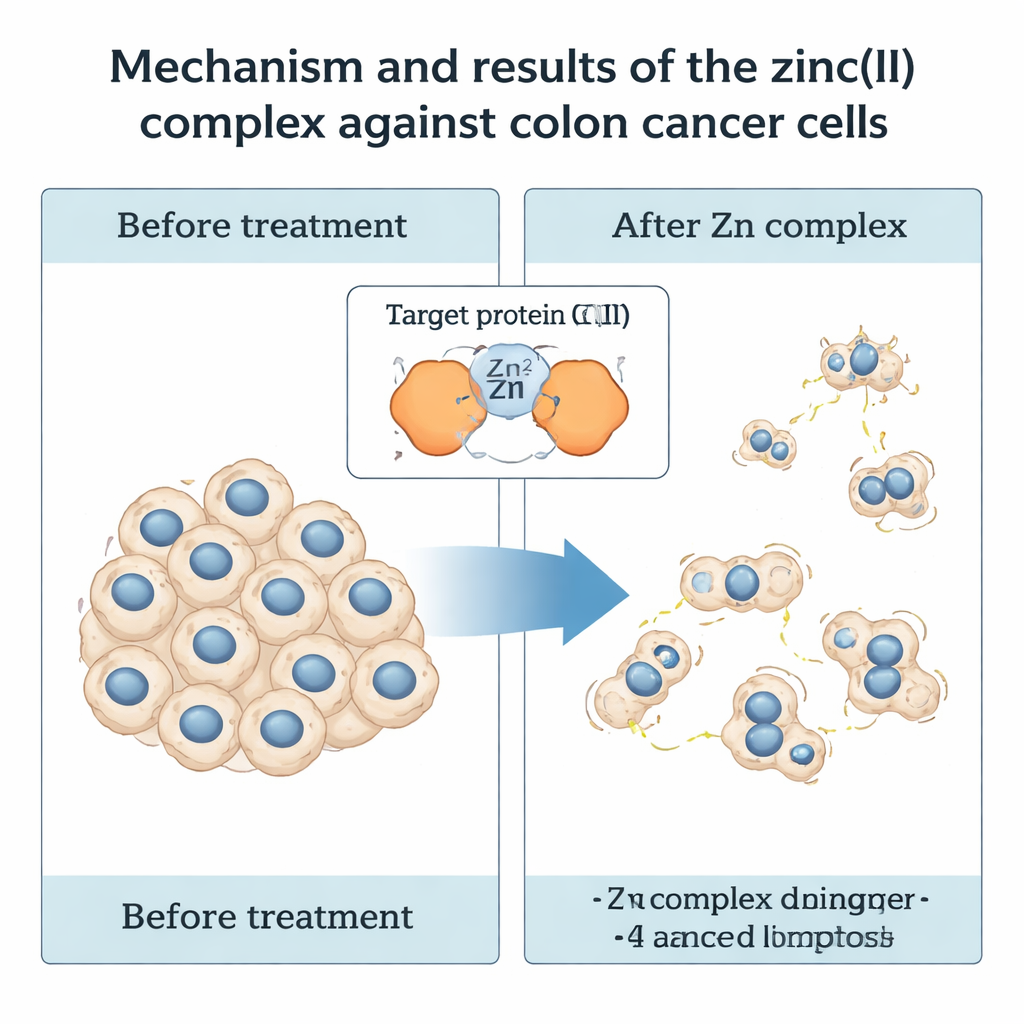
Cómo el complejo de zinc encara las células de cáncer de colon
La prueba real fue biológica. Los investigadores trataron células humanas de cáncer colorrectal (HCT116) con IMP e IMP-Zn a diversas dosis y tiempos, y luego midieron cuántas células sobrevivían. Ambos compuestos ralentizaron el crecimiento de las células cancerosas, pero el complejo de zinc fue claramente más potente: a las 48 horas, IMP-Zn redujo la viabilidad celular a la mitad a unos 25 micromolares, mientras que el ligando solo necesitó una dosis mucho mayor. Igualmente importante, las mismas concentraciones de IMP-Zn no mostraron efecto tóxico detectable sobre una línea celular humana de riñón normal (HEK293), lo que apunta a cierto grado de selectividad hacia las células cancerosas. Cuando el equipo siguió las células cancerosas tratadas durante dos semanas, observaron que IMP-Zn redujo de forma notable tanto el número como el tamaño de las colonias que las células podían formar, lo que indica que interfiere con su capacidad de proliferar a largo plazo.
Pistas de que las células se encaminan hacia la muerte programada
Para entender cómo el complejo de zinc daña las células cancerosas, los científicos examinaron el ciclo celular, la serie de etapas por las que pasan las células al crecer y dividirse. Tras la exposición a IMP-Zn, una fracción mucho mayor de células HCT116 se desplazó a una fase "SubG0", una señal de células con ADN fragmentado. Este patrón se asocia comúnmente con la apoptosis, una forma controlada de muerte celular que suelen buscar los fármacos anticancerígenos. Simulaciones de acoplamiento molecular proporcionaron otra pieza del rompecabezas: los modelos virtuales sugirieron que IMP-Zn se une con mayor fuerza que IMP a varias proteínas relacionadas con el cáncer, incluyendo una quinasa de receptor de factor de crecimiento, una quinasa reguladora del ciclo celular y una enzima metabolizadora de fármacos. Estas interacciones más fuertes apoyan la idea de que la coordinación con zinc ayuda al compuesto a aferrarse a maquinaria celular crítica y a perturbar la supervivencia de las células cancerosas.
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio muestra que "adornar" un andamiaje pirozol–hidrazona con zinc hace algo más que ajustar su química: convierte a IMP en un agente más reactivo, más potente y aparentemente más selectivo contra células de cáncer colorrectal. Aunque IMP-Zn aún está lejos de ser un fármaco terminado —aún debe probarse en animales o en humanos— su capacidad para ralentizar significativamente el crecimiento de células de cáncer de colon, empujar las células hacia la apoptosis y preservar las células normales lo señala como un miembro prometedor de una clase creciente de metalodrogas basadas en zinc. Este trabajo sugiere que complejos de zinc diseñados con cuidado podrían ofrecer alternativas o complementos más selectivos y menos agresivos a la quimioterapia basada en metales tradicional en el futuro.
Cita: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Palabras clave: agentes anticancerígenos basados en zinc, cáncer colorrectal, complejo pirozol-hidrazona, acoplamiento molecular, apoptosis