Clear Sky Science · es
Efectos radiosensibilizadores de nanopartículas de plata dirigidos a la angiogénesis y la señalización de metaloproteinasas de la matriz en líneas celulares de cáncer de mama triple negativo
Hacer más vulnerables a los cánceres de mama más agresivos
El cáncer de mama triple negativo es una de las formas de cáncer de mama más difíciles de tratar. Tiende a crecer con rapidez, a diseminarse temprano y carece de los “puntos de agarre” moleculares habituales a los que se dirigen muchos fármacos modernos. La radiación suele formar parte del tratamiento, pero estos tumores pueden mostrarse obstinadamente resistentes. Este estudio plantea una pregunta simple e intrigante: ¿pueden pequeñas partículas de plata mejorar la efectividad de la radiación, a la vez que frenan la capacidad del tumor para formar nuevos vasos sanguíneos y diseminarse?
Pequeños ayudantes de plata para la radiación
Los investigadores se centraron en nanopartículas de plata: esferas de plata ultrapequeñas medidas en milmillonésimas de metro. Debido a que la plata es densa y interactúa fuertemente con los rayos X, estas partículas pueden concentrar los efectos de la radiación justo donde se acumulan. El equipo trabajó con dos modelos de laboratorio muy usados de cáncer de mama triple negativo, comparándolos con una línea celular mamaria no cancerosa. Primero evaluaron la toxicidad de las nanopartículas de plata por sí solas y encontraron que las células cancerosas morían a dosis mucho más bajas que las células normales, lo que sugiere una ventana terapéutica útil. Usando métodos matemáticos para analizar cómo interactúan las partículas y la radiación, mostraron que la combinación de ambos produjo un efecto claramente mayor de destrucción tumoral que cualquiera de los tratamientos por separado.
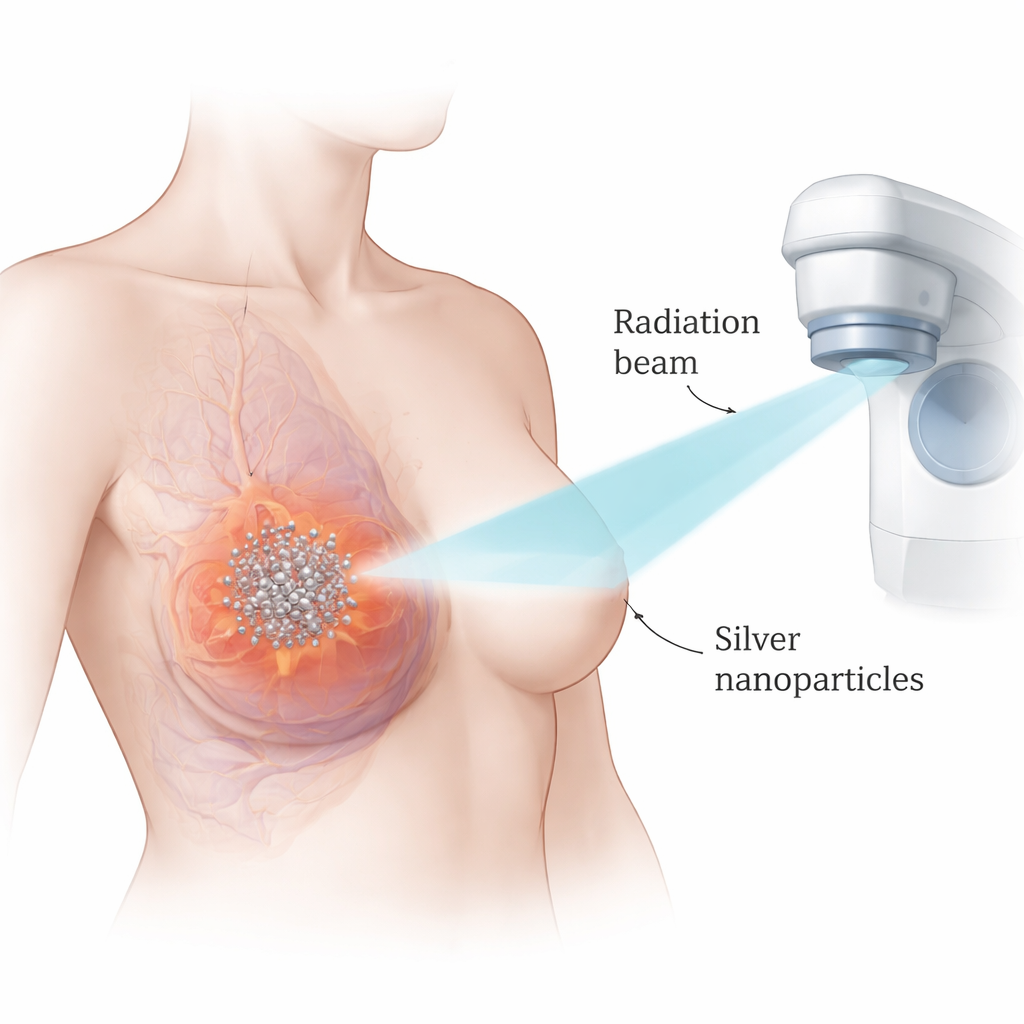
Inducir la autodestrucción de las células cancerosas
A continuación, los científicos examinaron cómo el tratamiento combinado mataba las células. Midieron la apoptosis, una forma de suicidio celular programado, y rastrearon la acumulación de moléculas altamente reactivas conocidas como especies reactivas de oxígeno (ROS). Se sabe que la radiación actúa en parte generando ROS que dañan el ADN. En ambas líneas celulares de cáncer de mama triple negativo, las nanopartículas de plata por sí solas aumentaron la apoptosis y los niveles de ROS, y la radiación sola también lo hizo; pero usarlas juntas elevó ambas medidas de forma dramática. Esto significa que más células cancerosas fueron empujadas hacia un modo ordenado de autodestrucción, en lugar de permanecer en un estado dañado que a veces puede favorecer recaídas o resistencia.
Privar del suministro sanguíneo y frenar la diseminación
Los tumores dependen de los vasos sanguíneos para traer oxígeno y nutrientes, y los cánceres agresivos pueden incluso imitar vasos sanguíneos por sí mismos. El equipo examinó dos interruptores moleculares clave implicados en la formación y estabilización de los vasos tumorales, llamados VEGFR2 y Tie2. En ambas líneas celulares, las nanopartículas de plata redujeron la actividad de estos genes, y la combinación con radiación los apagó aún más. También analizaron dos enzimas, MMP-2 y MMP-9, que ayudan a las células cancerosas a degradar el tejido circundante y migrar. En uno de los modelos celulares, tanto la radiación como las nanopartículas de plata disminuyeron estas enzimas, mientras que el tratamiento combinado tuvo el efecto más pronunciado. Cuando los científicos observaron cómo las células cancerosas se desplazaban para cubrir una “erosión” artificial en una placa de cultivo, y cuando probaron la capacidad de formar tubos similares a vasos en un sistema de cocultivo, el tratamiento combinado fue el que más claramente ralentizó la migración y la formación de tubos.
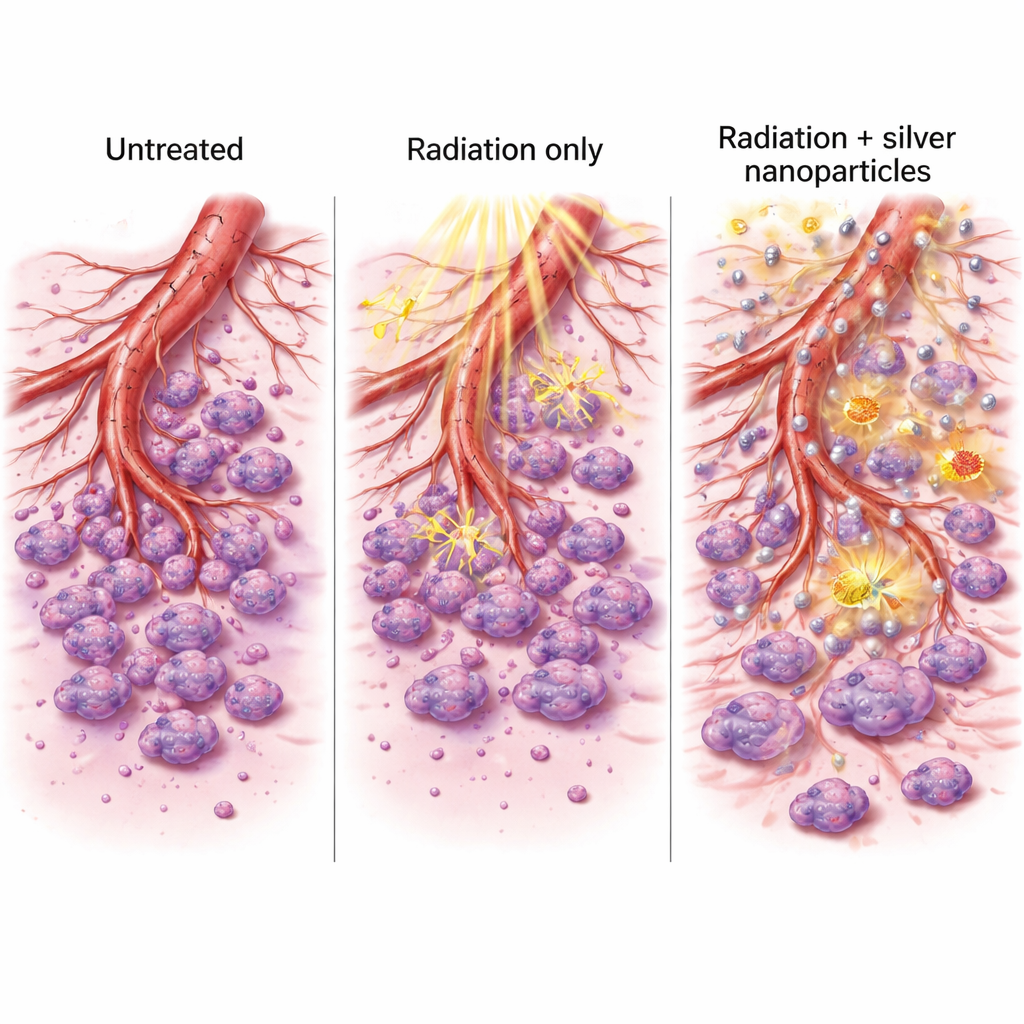
Por qué importan estos cambios
Al reducir genes que promueven el crecimiento de nuevos vasos sanguíneos y enzimas que facilitan la invasión celular, la combinación plata más radiación hizo más que simplemente matar células cancerosas. También alteró los sistemas de apoyo que los tumores usan para expandirse y diseminarse. Las células tratadas tuvieron menos capacidad para cerrar heridas en placas de laboratorio y menos facilidad para organizarse en redes ramificadas que recuerdan a vasos sanguíneos en formación. Junto con el marcado aumento de la muerte celular y la producción de ROS, estos efectos sugieren un beneficio de doble filo: un ataque directo más potente contra el tumor y herramientas reducidas para su crecimiento y metástasis futuros.
Qué podría significar esto para los pacientes
Por ahora, estos resultados proceden de células cancerosas cultivadas en el laboratorio, no de pacientes. Aun así, ofrecen una imagen esperanzadora. Las nanopartículas de plata actuaron como radiosensibilizadores, haciendo que la radioterapia estándar fuera más potente contra las células de cáncer de mama triple negativo. Al mismo tiempo, parecieron impedir la capacidad del tumor para construir líneas de suministro sanguíneo e invadir el tejido circundante. Si futuros estudios en animales y ensayos clínicos confirman que estas partículas pueden administrarse con seguridad y selectividad a los tumores, podrían ayudar a los médicos a usar dosis de radiación más bajas obteniendo mejores resultados, ofreciendo una nueva forma de abordar una de las variantes de cáncer de mama más desafiantes.
Cita: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Palabras clave: cáncer de mama triple negativo, nanopartículas de plata, radioterapia, angiogénesis, metástasis