Clear Sky Science · es
Respuesta quimiosensorial a quimioterapéuticos basados en Pt vía receptores gustativos amargos in vitro revela un nuevo mecanismo de los trastornos del gusto amargo
Por qué los fármacos contra el cáncer pueden hacer que todo tenga un sabor horrible de repente
Los pacientes con cáncer suelen informar que los alimentos empiezan a saber extrañamente amargos o metálicos poco después de iniciar la quimioterapia. Esto no solo estropea las comidas: puede reducir el apetito, promover la pérdida de peso y minar la calidad de vida justo cuando los pacientes necesitan fuerza. Este estudio plantea una pregunta aparentemente simple con grandes consecuencias prácticas: ¿cómo interfieren exactamente los fármacos quimioterapéuticos comunes a base de platino con nuestro sentido del gusto, y se puede atenuar ese efecto de forma segura sin debilitar el tratamiento?
El papel oculto de los “sensores de amargor” en el intestino y la boca
Nuestras lenguas y el tracto digestivo están salpicados de receptores del gusto amargo, diseñados para advertirnos sobre sustancias potencialmente dañinas. Estos sensores, conocidos como TAS2R, no se limitan a las papilas gustativas; también se encuentran en células del estómago. Los investigadores emplearon una línea celular gástrica humana (HGT-1) que actúa como un detector de amargor in vitro: cuando se activan los receptores amargos, las células expulsan más protones (ácido), lo que puede medirse como un cambio en una señal llamada índice de protones intracelulares. Al exponer estas células a dos fármacos contra el cáncer basados en platino ampliamente usados —carboplatino y cisplatino—, el equipo pudo sondear de forma segura cuán “amargos” resultan estos fármacos para células humanas sin pedirle nunca a una persona que pruebe un compuesto tóxico. 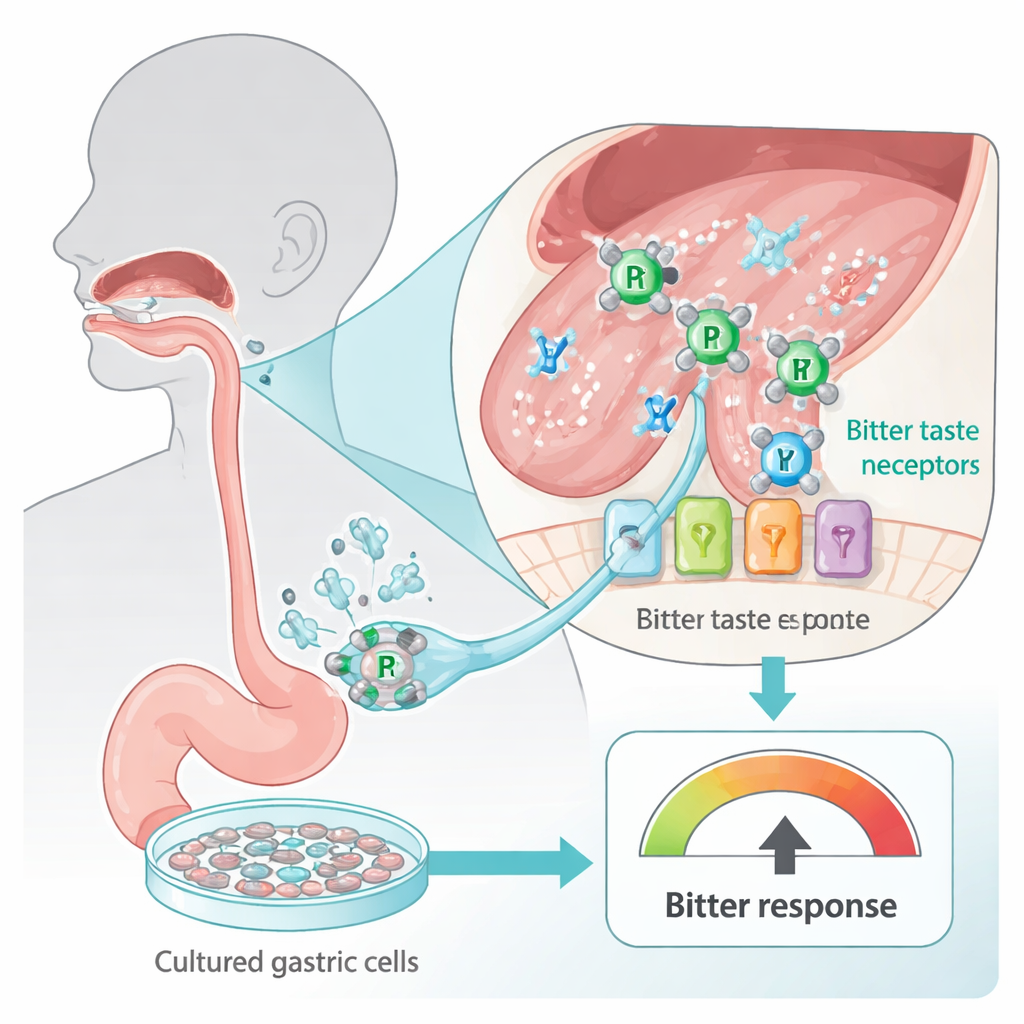
Fármacos quimioterapéuticos que saben amargos para las células
Cuando las células gástricas se trataron con concentraciones clínicamente relevantes de carboplatino y cisplatino, ambos fármacos desencadenaron una clara respuesta de tipo amargo dependiente de la dosis: cuanto mayor era la dosis, más intensa era la reacción celular. Sin embargo, el cisplatino produjo una respuesta más intensa que el carboplatino cuando se tuvo en cuenta su ratio terapéutica habitual (aproximadamente 1:4), lo que sugiere que puede contribuir más a los problemas de sabor amargo en los pacientes. A nivel genético, la exposición a estos fármacos cambió la actividad de múltiples genes de receptores amargos en las células, lo que indica que los fármacos de platino no actúan sobre un único “interruptor del amargor”, sino que remodelan de forma amplia el sistema de detección del amargor. Entre estos receptores, TAS2R4 y TAS2R5 destacaron por estar ambos muy activos y verse fuertemente afectados por el tratamiento.
Apagar las señales amargas y probar un bloqueador amargo natural
Para precisar qué receptores importan más, el equipo desactivó selectivamente receptores amargos específicos. Eliminar TAS2R4 o reducir la expresión de TAS2R5 redujo cada uno la respuesta de tipo amargo al carboplatino y al cisplatino, confirmando que estos receptores contribuyen a la detección de los fármacos. Los científicos probaron luego una contramedida prometedora: la sal sódica del homoeriodictiol (Na-HED), una flavanona aislada originalmente de la planta norteamericana Herba Santa y ya conocida por enmascarar el amargor de otros compuestos. Cuando se añadió Na-HED junto con los fármacos de platino, atenuó notablemente la respuesta celular de tipo amargo —aproximadamente en tres cuartas partes tanto para el carboplatino como para el cisplatino— sin dañar las células por sí sola. Esto demuestra que Na-HED puede actuar directamente sobre los receptores amargos para mitigar la señal desencadenada por los fármacos quimioterapéuticos.
Cuando la detección del amargor y la captación del fármaco se cruzan
Además de explicar por qué la quimioterapia con platino puede saber amarga, el estudio revela un giro inesperado: los mismos receptores de amargor también parecen influir en cuánto de estos fármacos entra en las células. Empleando espectrometría de masas altamente sensible, los investigadores midieron el contenido de platino dentro de las células tras el tratamiento. Las células que carecían de ciertos receptores, como TAS2R4 o TAS2R43, acumularon más platino que las células normales, lo que sugiere que los receptores intactos ayudan a limitar la captación o retención celular de estos agentes tóxicos. Na-HED no cambió la captación de carboplatino, pero sí redujo cuánto cisplatino entró en las células y mostró interacción molecular directa con cisplatino en solución. Esto sugiere que un compuesto enmascarante del amargor podría, en algunos casos, también modular la intensidad con la que un fármaco afecta a tejidos locales, como las células del gusto o las glándulas salivales. 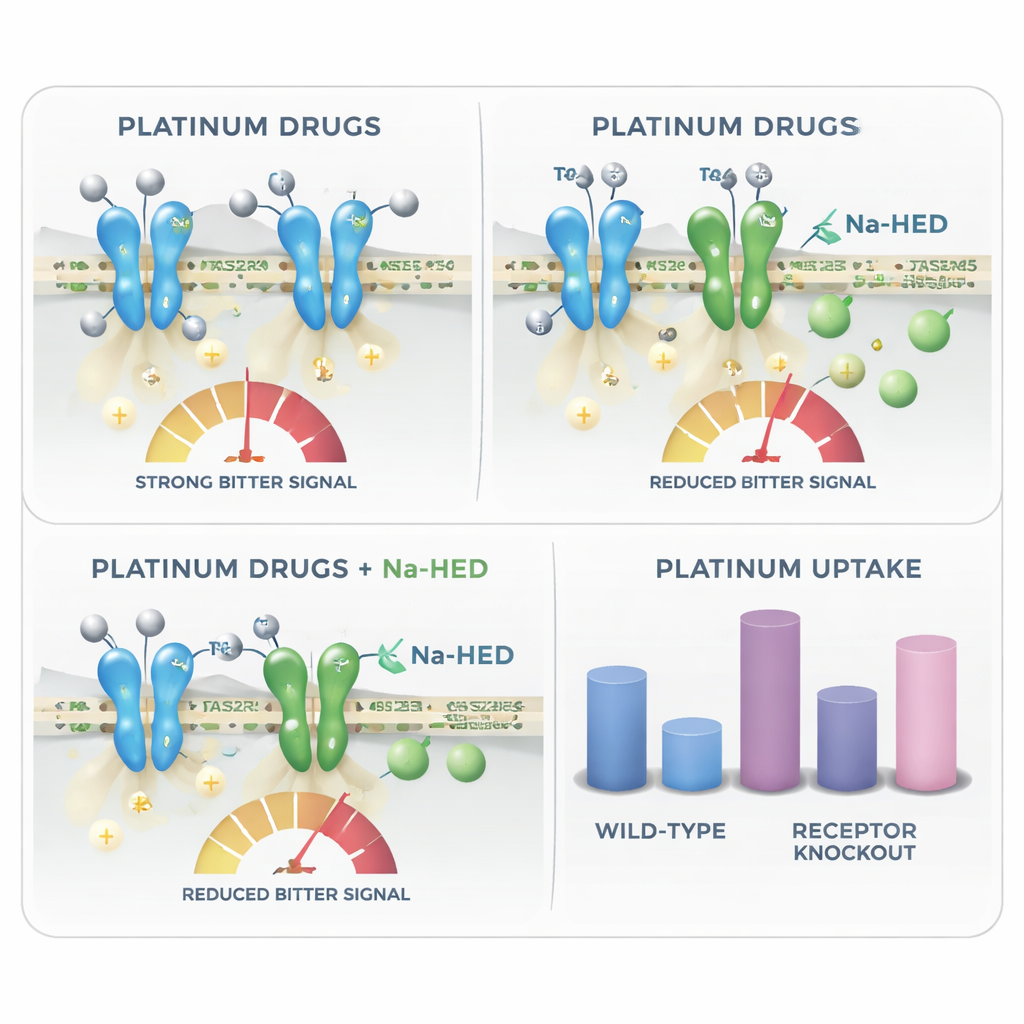
Hacia experiencias de sabor más suaves durante la quimioterapia
Para los pacientes, la conclusión principal es esperanzadora: la quimioterapia basada en platino parece desencadenar problemas de sabor amargo al activar directamente receptores amargos que existen no solo en la lengua sino también en células de tipo intestinal. El cisplatino parece particularmente potente en este sentido. El estudio muestra que Na-HED puede atenuar sustancialmente esta señal amarga en un sistema celular controlado y que podría también limitar la captación local de cisplatino. Aunque estos hallazgos necesitan confirmación en humanos, apuntan hacia futuros tratamientos bucales de tipo enjuague y escupir que contengan Na-HED y que podrían suavizar las sensaciones amargas y metálicas sin interferir con la acción anticancerígena de los fármacos en todo el cuerpo.
Cita: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Palabras clave: cambios del gusto por quimioterapia, receptores del gusto amargo, cisplatino y carboplatino, compuestos enmascarantes del amargor, nutrición de pacientes con cáncer