Clear Sky Science · es
Cálculo DFT de la complejación de Ac3+ y Bi3+ con el quelante híbrido 3p-C-DEPA para la terapia alfa dirigida
Por qué esta investigación importa para el tratamiento del cáncer
La medicina oncológica moderna depende cada vez más de fármacos radiactivos capaces de localizar tumores célula por célula. Un enfoque potente, denominado terapia alfa dirigida, utiliza partículas de gran energía que pueden eliminar células cancerosas individuales con notable precisión. Pero para administrar estas partículas con seguridad, el metal radiactivo debe quedar encerrado en una pequeña «jaula» molecular para que no se desplace a tejidos sanos. Este estudio explora una nueva molécula jaula, 3p‑C‑DEPA, diseñada para retener metales particularmente difíciles como el actinio‑225 y el bismuto‑213, y plantea la pregunta: ¿puede unirse a ellos con más seguridad que el quelante estándar actual, DOTA?
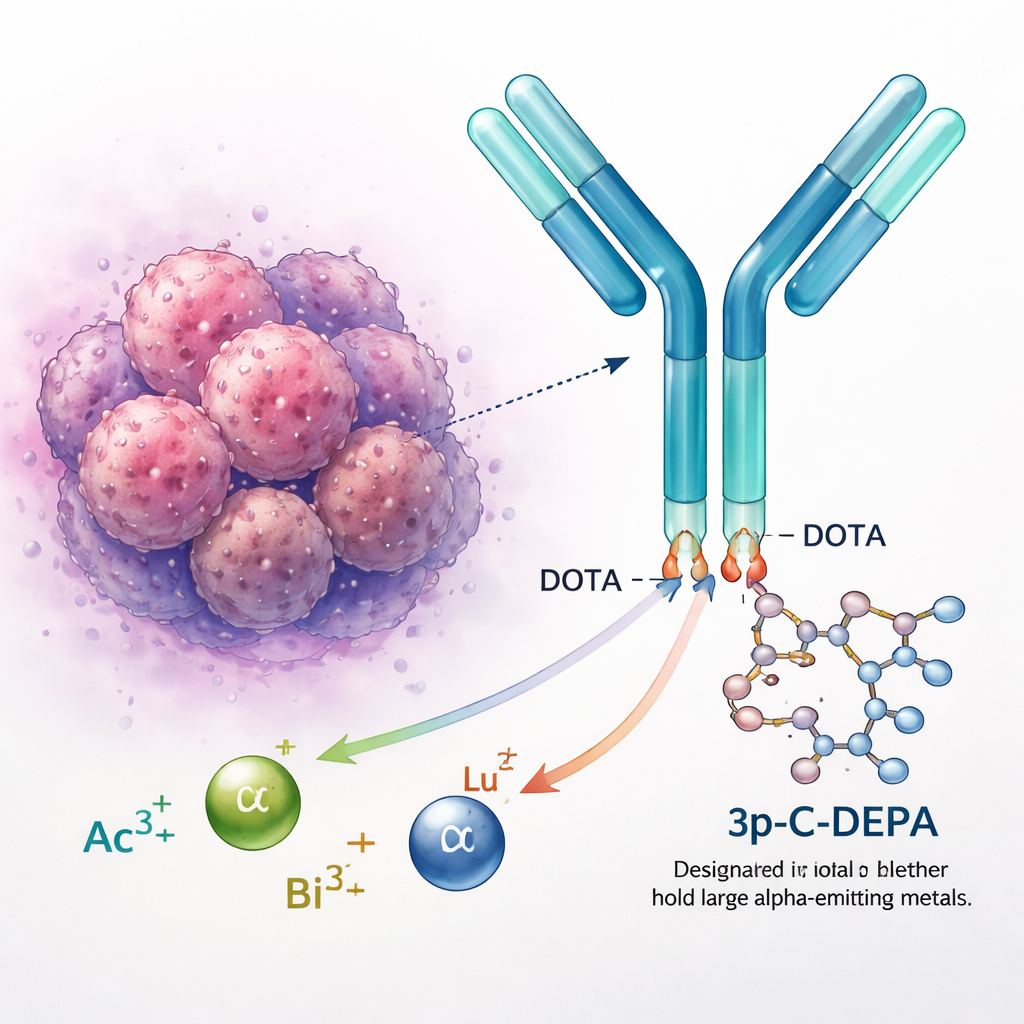
Fijando los metales radiactivos de forma segura
Metales radiactivos como el actinio, el bismuto y el lutecio se emplean para diagnosticar y tratar el cáncer. Por sí solos, sin embargo, estos iones metálicos cargados positivamente interactuarían libremente en el organismo, potencialmente dañando órganos saludables. Por eso los químicos los enlazan a «quelantes», moléculas en forma de anillo que rodean el metal y lo mantienen en su sitio. El quelante de referencia DOTA se usa en varios fármacos aprobados, pero tiene dificultades con iones más grandes y difusos como el actinio‑225. Estos metales pueden escapar con el tiempo, lo que plantea dudas sobre la seguridad a largo plazo y limita la aplicabilidad de la terapia alfa dirigida.
Una jaula híbrida diseñada para átomos más grandes
El nuevo quelante, 3p‑C‑DEPA, combina rasgos de dos diseños establecidos: el armazón rígido y anular de DOTA y la estructura más flexible y abierta de otro quelante llamado DTPA. Esta arquitectura híbrida dota a 3p‑C‑DEPA de diez fuertes «manos» de unión (átomos de nitrógeno y oxígeno) frente a las ocho de DOTA, y de una cavidad más espaciosa que puede acomodar mejor iones metálicos de gran tamaño. Trabajos de laboratorio previos sugerían que 3p‑C‑DEPA puede marcar anticuerpos rápidamente a temperaturas suaves y mantener radionúclidos a base de bismuto estables en suero sanguíneo. El estudio actual da el siguiente paso, utilizando cálculos a nivel cuántico para comparar sistemáticamente cómo se unen 3p‑C‑DEPA y DOTA al lutecio‑177, bismuto‑213 y actinio‑225.
Escudriñando el apretón molecular
Dado que trabajar directamente con emisores alfa de vida corta es difícil, los investigadores recurrieron a la teoría del funcional de la densidad (DFT), un método computacional potente que estima cómo se distribuyen los electrones en las moléculas y cuán fuertemente se atraen los átomos entre sí. Modelaron cada ion metálico en agua, luego su complejo con DOTA o con 3p‑C‑DEPA, y calcularon el cambio de energía libre cuando el metal pasa del agua a la jaula del quelante. Este cambio de energía se traduce en una «constante de estabilidad»: cuanto mayor es el valor, más firmemente sujeta el quelante al metal. Se emplearon dos enfoques DFT diferentes y dos modelos de solvatación para imitar condiciones de solución realistas y comprobar que las tendencias fueran robustas y no artefactos de un único montaje computacional.
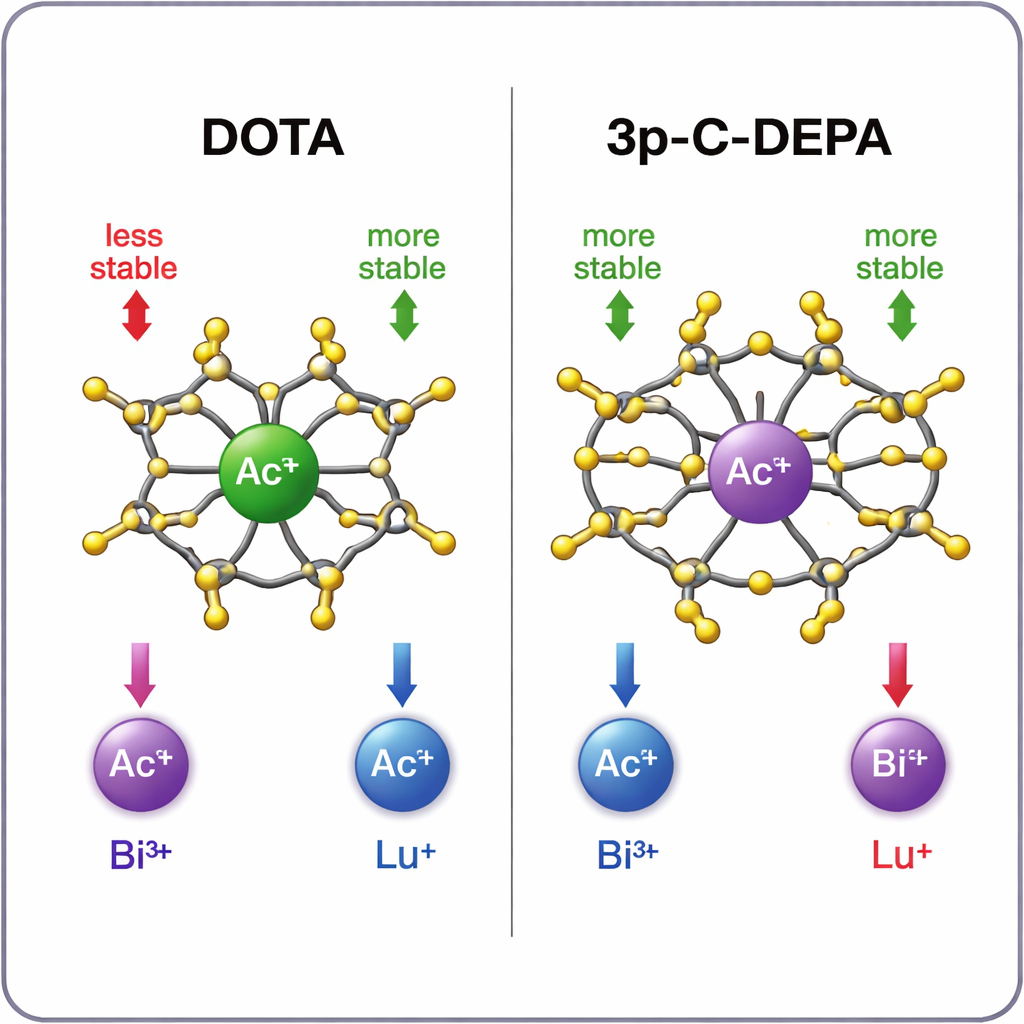
¿Qué jaula sujeta mejor a cada metal?
Las simulaciones muestran un patrón claro. Para el gran ion de actinio, 3p‑C‑DEPA forma un complejo marcadamente más estable que DOTA, gracias a su cavidad mayor y a un mayor número de donantes oxígeno que pueden agarrar el metal. El bismuto‑213 también encaja bien en 3p‑C‑DEPA, beneficiándose tanto de su tamaño como de su carácter aceptor de electrones, que combina con los grupos donantes de electrones del quelante. En cambio, el más pequeño lutecio‑177 se acomoda mejor en el entorno más ceñido y de ocho brazos de DOTA. En 3p‑C‑DEPA, los donantes en exceso se apiñan alrededor del ion pequeño, generando interacciones repulsivas que parecen ralentizar el marcado y debilitar ligeramente el complejo final. Las tendencias de estabilidad calculadas concuerdan bien con los datos experimentales y los rendimientos de radiomarcado disponibles, lo que da credibilidad a las predicciones teóricas.
Qué significa esto para futuras terapias contra el cáncer
En términos prácticos, el estudio sugiere que DOTA no es una jaula única para todo: funciona muy bien con metales más pequeños como el lutecio, pero es subóptima para emisores alfa más voluminosos como el actinio‑225. 3p‑C‑DEPA, en cambio, actúa como un soporte a medida para estos iones mayores, sujetándolos con más fuerza y bajo condiciones más suaves que convienen a moléculas de direccionamiento delicadas como los anticuerpos. Aunque hacen falta más trabajos experimentales y clínicos, los cálculos señalan a 3p‑C‑DEPA como una columna vertebral prometedora para terapias alfa dirigidas más seguras y eficaces, que podrían ampliar el acceso a tratamientos contra el cáncer altamente potentes capaces de erradicar tumores preservando el tejido sano circundante.
Cita: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Palabras clave: terapia alfa dirigida, radiofármacos, diseño de quelantes, actinio-225, teoría del funcional de la densidad