Clear Sky Science · es
Investigación experimental y correlación termodinámica de la solubilidad del clordiazepóxido en CO₂ supercrítico
Por qué disolver un fármaco conocido de una forma nueva importa
Muchos medicamentos modernos funcionan bien pero son difíciles de formular de manera eficiente: pueden no disolverse con facilidad, degradarse durante la fabricación o requerir grandes cantidades de disolventes orgánicos. Este estudio analiza el clordiazepóxido, un fármaco para la ansiedad usado desde hace tiempo, y plantea una pregunta práctica de amplio alcance: ¿qué tan bien se disuelve en dióxido de carbono supercrítico, un disolvente más limpio y ajustable que podría ayudar a fabricar partículas de fármaco más seguras y eficaces?
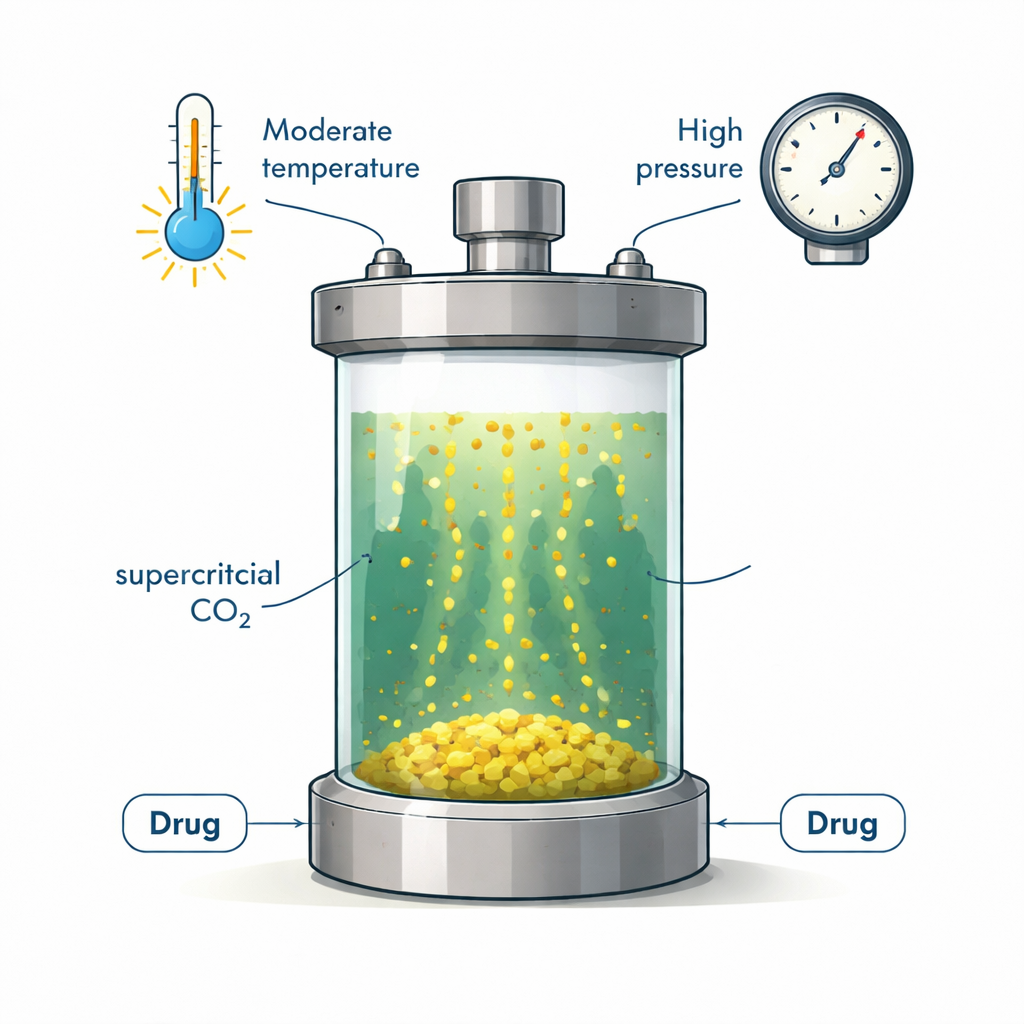
Un fluido verde que se comporta como gas y como líquido
El dióxido de carbono supercrítico es CO₂ presurizado y calentado por encima de ciertos límites, hasta alcanzar un estado que no es ni un gas típico ni un líquido convencional. En ese estado fluye como un gas pero tiene una densidad parecida a la de un líquido que puede disolver muchas sustancias. La industria ya lo usa para descafeinar café y extraer aromas y aceites. Para la farmacia, el CO₂ supercrítico resulta atractivo porque es no tóxico, aceptado por reguladores, barato y fácil de reciclar. Puede ayudar a crear partículas de fármaco pequeñas y uniformes y reducir la necesidad de disolventes orgánicos agresivos, siempre que—y solo si—el fármaco realmente se disuelva en él en una medida útil.
Midiendo cómo se comporta un fármaco contra la ansiedad bajo presión
Los autores se propusieron medir, por primera vez, cuánto clordiazepóxido se disuelve en CO₂ supercrítico puro dentro de una ventana de procesamiento práctica. Colocaron polvo sólido del fármaco en una celda de alta presión y hicieron fluir CO₂ a través de ella a presiones entre 12 y 30 megapascales y temperaturas entre 308 y 338 kelvin (aproximadamente 35–65 °C). Tras permitir que el sistema alcanzara el equilibrio, muestrearon la fase de CO₂, la expandieron rápidamente en un disolvente y usaron absorción en el ultravioleta visible para determinar cuánto fármaco se había disuelto. La solubilidad global varió desde aproximadamente 20 hasta 576 partes por millón, lo que corresponde a fracciones molares entre 0,0198×10⁻³ y 0,576×10⁻³, valores coherentes con muchos otros fármacos moderadamente solubles en CO₂ supercrítico.
Cómo la presión y la temperatura moldean la solubilidad
Las mediciones revelaron patrones claros e intuitivos. A temperatura fija, aumentar la presión siempre incrementó la solubilidad. Una mayor presión comprime las moléculas de CO₂, haciendo la fase supercrítica más densa y mejor capaz de rodear y transportar las moléculas del fármaco. La temperatura tuvo un efecto más sutil. A presiones bajas, calentar el sistema tendía a reducir la solubilidad porque diluye el CO₂ y disminuye su poder disolvente. Por encima de una presión de cruce de aproximadamente 19 megapascales, la tendencia se invirtió: temperaturas más altas aumentaron la solubilidad porque favorecían la tendencia del fármaco a escapar del estado sólido hacia el fluido. Este equilibrio entre la densidad del fluido y la volatilidad del fármaco es característico de los sistemas supercríticos y es importante para elegir condiciones operativas prácticas.
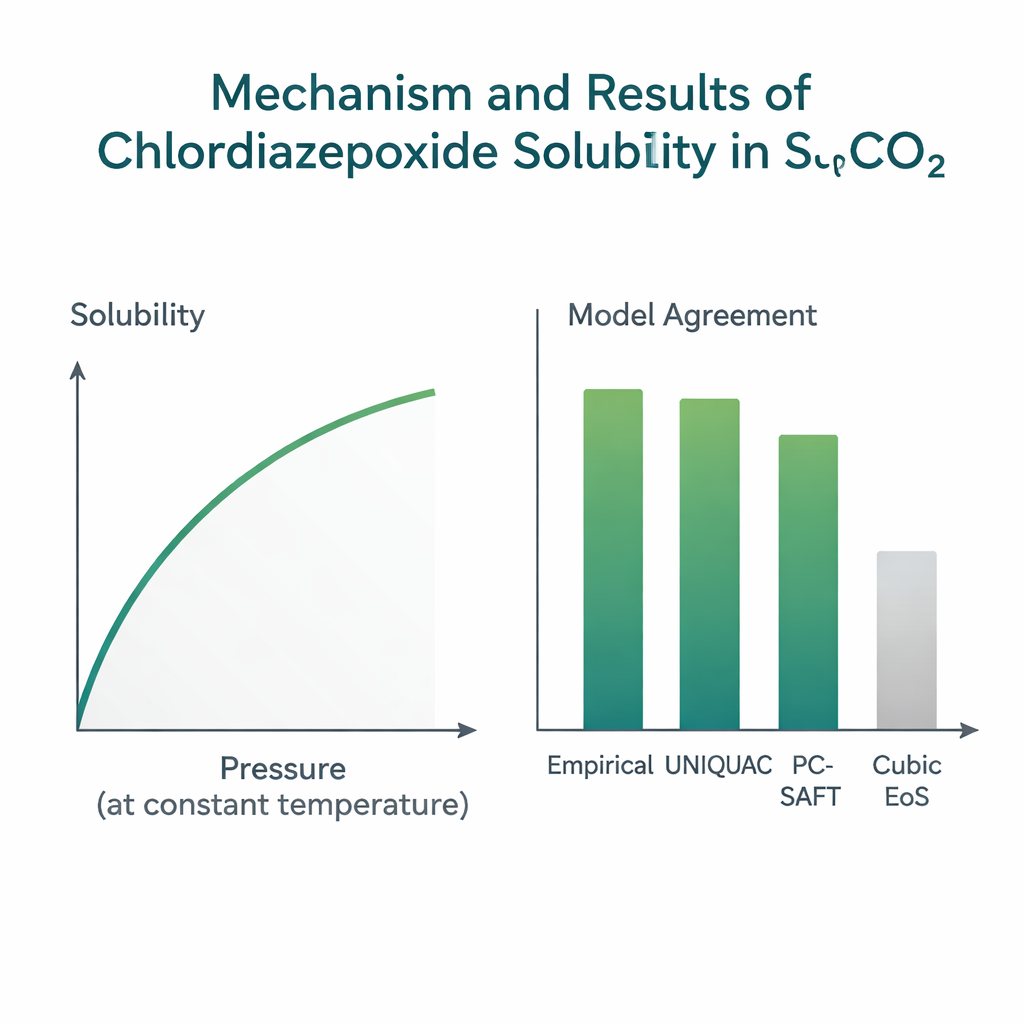
Enseñar a los modelos a predecir lo que ve el laboratorio
Dado que ejecutar experimentos a alta presión es lento y costoso, los ingenieros dependen de modelos matemáticos para predecir la solubilidad bajo condiciones nuevas o para fármacos relacionados. El equipo probó varias familias de modelos usando su nuevo conjunto de datos. Las fórmulas empíricas simples «basadas en la densidad», que vinculan la solubilidad directamente con la densidad del CO₂ y la temperatura usando solo unas pocas constantes de ajuste, fueron las que mejor funcionaron. En particular, la correlación establecida de Chrastil ajustó los datos con una desviación media de alrededor del 5%, y otras fórmulas similares también rindieron bien. Un enfoque más físicamente detallado llamado UNIQUAC para líquidos expandidos, que tiene en cuenta el tamaño y la forma molecular y las energías de interacción, alcanzó una precisión comparable, en torno al 6% de desviación. En contraste, las ecuaciones de estado cúbicas de uso común—fórmulas de propósito general para el comportamiento de fluidos—mostraron desviaciones cercanas al 20%, fallando en captar detalles más finos de cómo este fármaco específico interactúa con el CO₂.
Qué significa esto para la fabricación futura de fármacos
En términos simples, el estudio muestra que el clordiazepóxido se disuelve en CO₂ supercrítico en condiciones de relevancia tecnológica, y que su comportamiento puede describirse muy bien con modelos relativamente simples y bien elegidos. Esto proporciona un mapa fiable para diseñar procesos más ecológicos destinados a obtener nuevas formas sólidas o nanopartículas del fármaco, lo que puede mejorar su estabilidad o absorción en el organismo. En un sentido más amplio, el trabajo aporta un conjunto de datos raro y cuidadosamente medido para un medicamento de uso generalizado y demuestra qué herramientas de modelado son más confiables al planear procesos con CO₂ supercrítico, información que puede guiar una fabricación más limpia y eficiente de muchos otros fármacos.
Cita: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Palabras clave: dióxido de carbono supercrítico, solubilidad de fármacos, clordiazepóxido, procesamiento farmacéutico ecológico, modelado termodinámico