Clear Sky Science · es
Un enfoque de proteómica y proteómica redox para comprender la heterogeneidad del SDRA
Por qué esto importa para las personas en la unidad de cuidados intensivos
El síndrome de distrés respiratorio agudo (SDRA) es una forma potencialmente mortal de insuficiencia pulmonar que puede afectar a personas con infecciones graves, traumatismos u otras enfermedades críticas. Muchos pacientes con SDRA se parecen en la cabecera del enfermo, pero algunos se recuperan y otros no, y no existe ningún fármaco que haya demostrado revertir específicamente el síndrome. Este estudio plantea una pregunta sencilla pero importante: si examinamos con detalle las proteínas y las reacciones químicas dentro de los pulmones y la sangre de pacientes con SDRA, ¿podremos descubrir «tipos» biológicos ocultos de la enfermedad que expliquen por qué los pacientes evolucionan de forma tan distinta?
Mirar dentro de los pulmones, no solo en el torrente sanguíneo
Para explorar esto, los investigadores siguieron a 16 adultos en una unidad de cuidados intensivos con SDRA que estaban conectados a ventilación mecánica. En los primeros tres días tras el diagnóstico, recogieron sangre y una muestra especial llamada líquido de lavado broncoalveolar (LBA), que es un lavado suave de los alvéolos pulmonares. Repitieron estas recogidas durante varios días cuando fue posible. Con espectrometría de masas de alta gama midieron cientos de proteínas en cada muestra (proteómica) y, de forma crucial, también examinaron cuánto estaban oxidadas algunas de esas proteínas (proteómica redox), lo que refleja cuánto han sido dañadas o reguladas por especies reactivas de oxígeno, subproductos químicamente agresivos de la inflamación.
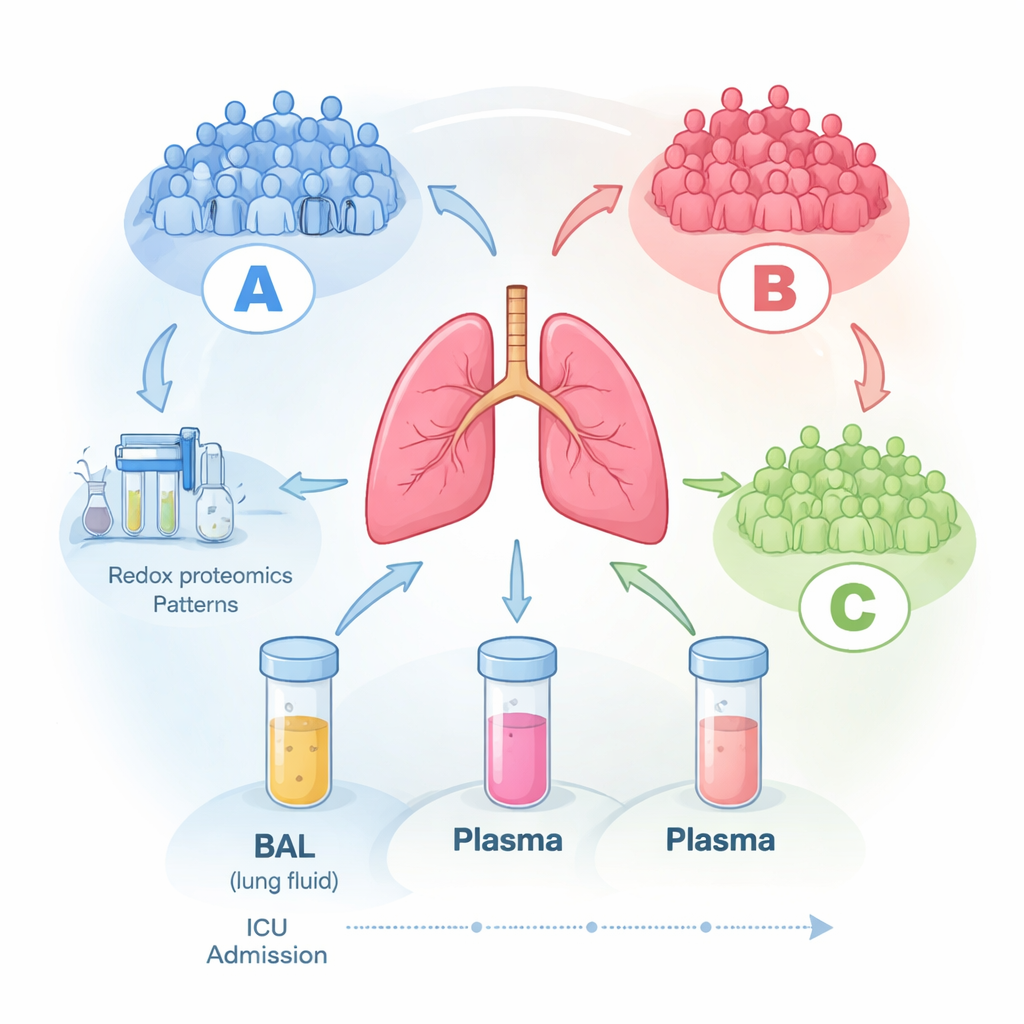
Emergen tres grupos de pacientes ocultos
Cuando el equipo dejó que los datos se agruparan por sí mismos sin decirle nada al ordenador sobre los pacientes, surgió un patrón claro en las muestras de líquido pulmonar: tres grupos moleculares distintos, etiquetados A, B y C. Los pacientes del grupo A tendían a estar más graves al ingreso, mientras que los grupos B y C presentaban una enfermedad más leve. De forma llamativa, estas firmas moleculares se mantuvieron en gran medida estables durante hasta seis días en la UCI, lo que sugiere que cada paciente pertenece a un patrón biológico relativamente consistente y no fluctúa de forma aleatoria día a día. Las medidas clínicas estándar en la cabecera —como los niveles de oxígeno, la duración de la estancia o las puntuaciones generales de gravedad— no se correlacionaron bien con estos agrupamientos moleculares, lo que insinúa que las herramientas clínicas habituales pasan por alto biología clave que ocurre dentro de los pulmones.
Estrés oxidativo y las defensas del organismo
Un tema principal en los datos fue el equilibrio entre las dañinas especies reactivas de oxígeno y las defensas antioxidantes del organismo. En el grupo A, el más grave, muchas proteínas pulmonares implicadas en la producción de energía y el mantenimiento celular estaban presentes en niveles más bajos. Aún más revelador, enzimas antioxidantes importantes como las peroxiredoxinas, proteínas relacionadas con el glutatión, la tioredoxina y la catalasa estaban significativamente reducidas. En contraste, los grupos B y especialmente C mostraron niveles más altos de estas proteínas protectoras, lo que sugiere que sus pulmones estaban mejor equipados para detoxificar oxidantes dañinos y limitar el daño colateral de la inflamación. Los patrones en el estado de oxidación de las proteínas añadieron otra capa, mostrando subconjuntos diferentes de proteínas oxidadas enriquecidas en los grupos más y menos severos.
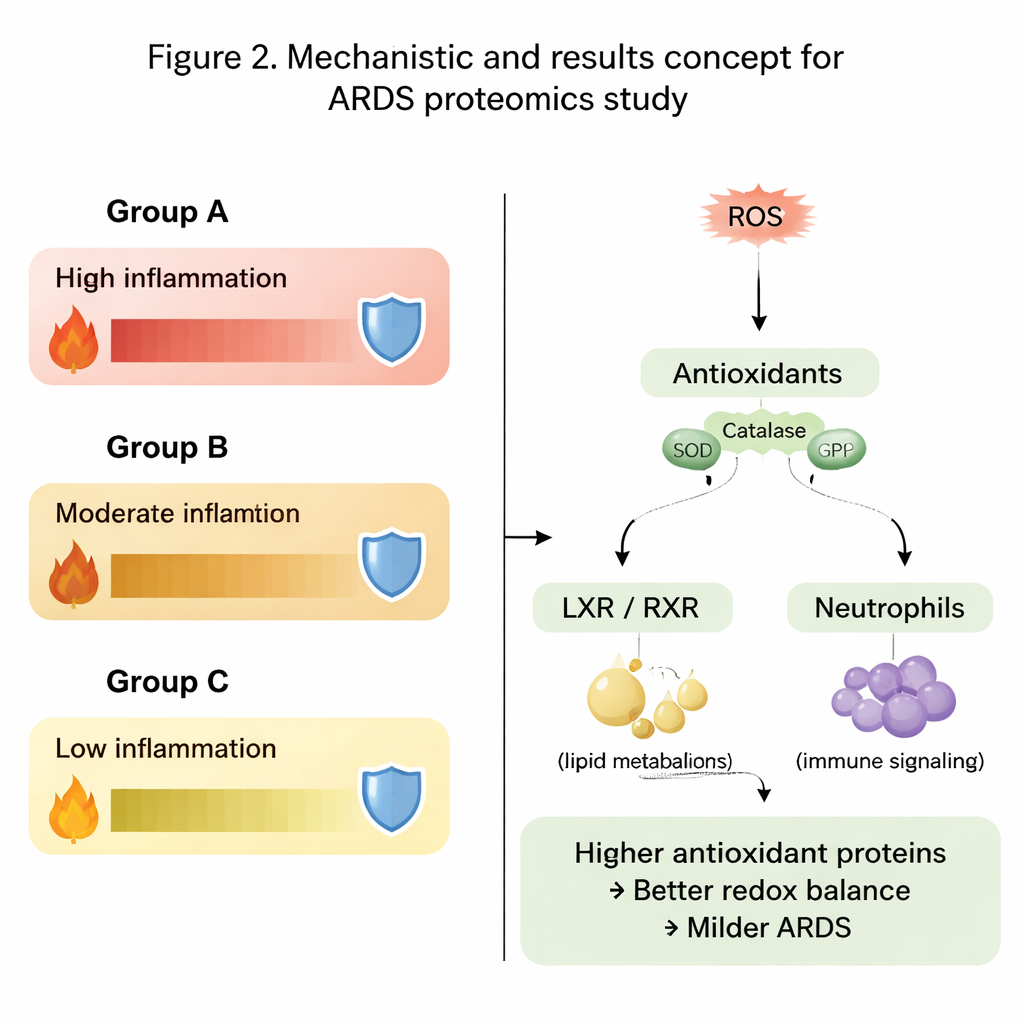
Vías de señalización que moldean la inflamación
Más allá de proteínas individuales, los autores examinaron vías biológicas completas. Encontraron que las vías asociadas con la inflamación, el manejo del colesterol y los lípidos, y la actividad de las células inmunitarias se comportaban de forma distinta entre los tres grupos. Señales vinculadas a la vía receptor X del retinoide–receptor X del hígado (LXR/RXR) y a una enzima llamada DHCR24, que en conjunto ayudan a regular el metabolismo de lípidos y las respuestas inmunes, fueron especialmente notables. En el grupo más severo, se predijo que estas vías estaban más activas, junto con una señalización reducida de la citocina inmune interleucina-12. Al mismo tiempo, las vías que implican especies reactivas de oxígeno, su detoxificación y la actividad de neutrófilos mostraron patrones contrastantes entre el líquido pulmonar y la sangre, subrayando que lo que ocurre localmente en el pulmón puede diferir de lo que se observa en la circulación.
Qué podría significar esto para la atención futura
Este estudio pequeño y exploratorio no cambia el tratamiento hoy, y sus hallazgos deben confirmarse en grupos de pacientes mucho mayores. Sin embargo, demuestra que al perfilar detenidamente las proteínas y su estado redox directamente en el líquido pulmonar —en lugar de confiar solo en pruebas sanguíneas o en puntuaciones clínicas— podemos distinguir subtipos biológicamente relevantes de SDRA. Estos subtipos difieren en estrés oxidativo, capacidad antioxidante, metabolismo y señalización inmune, y permanecen relativamente estables durante los primeros días críticos de la enfermedad. En el futuro, estas huellas moleculares podrían ayudar a los médicos a clasificar a los pacientes con SDRA en grupos más precisos, elegir terapias dirigidas adaptadas a cada patrón y diseñar ensayos clínicos más inteligentes con mayor probabilidad de encontrar tratamientos realmente eficaces.
Cita: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Palabras clave: síndrome de distrés respiratorio agudo, proteómica, estrés oxidativo, lavado broncoalveolar, cuidados críticos