Clear Sky Science · es
Agulillas de Co3O4 crecidas sobre óxido de grafeno como electrocatalizador eficiente para la electrólisis hídrica híbrida mediante reacciones anódicas alternativas de oxidación
Convertir residuos de fruta en combustible del futuro
El hidrógeno suele presentarse como un combustible limpio del futuro, pero su obtención normalmente exige mucha electricidad. Este estudio muestra cómo algo tan corriente como las pieles de naranja desechadas puede ayudar a cambiar eso. Al transformar este residuo en un material de carbono especial y combinarlo con un compuesto a base de cobalto, los investigadores crearon un catalizador de bajo coste que puede producir hidrógeno usando mucha menos energía que los métodos convencionales de separación del agua. Además, sustituyen un paso ineficiente en la electrólisis por reacciones más suaves que convierten compuestos problemáticos en gases inofensivos.
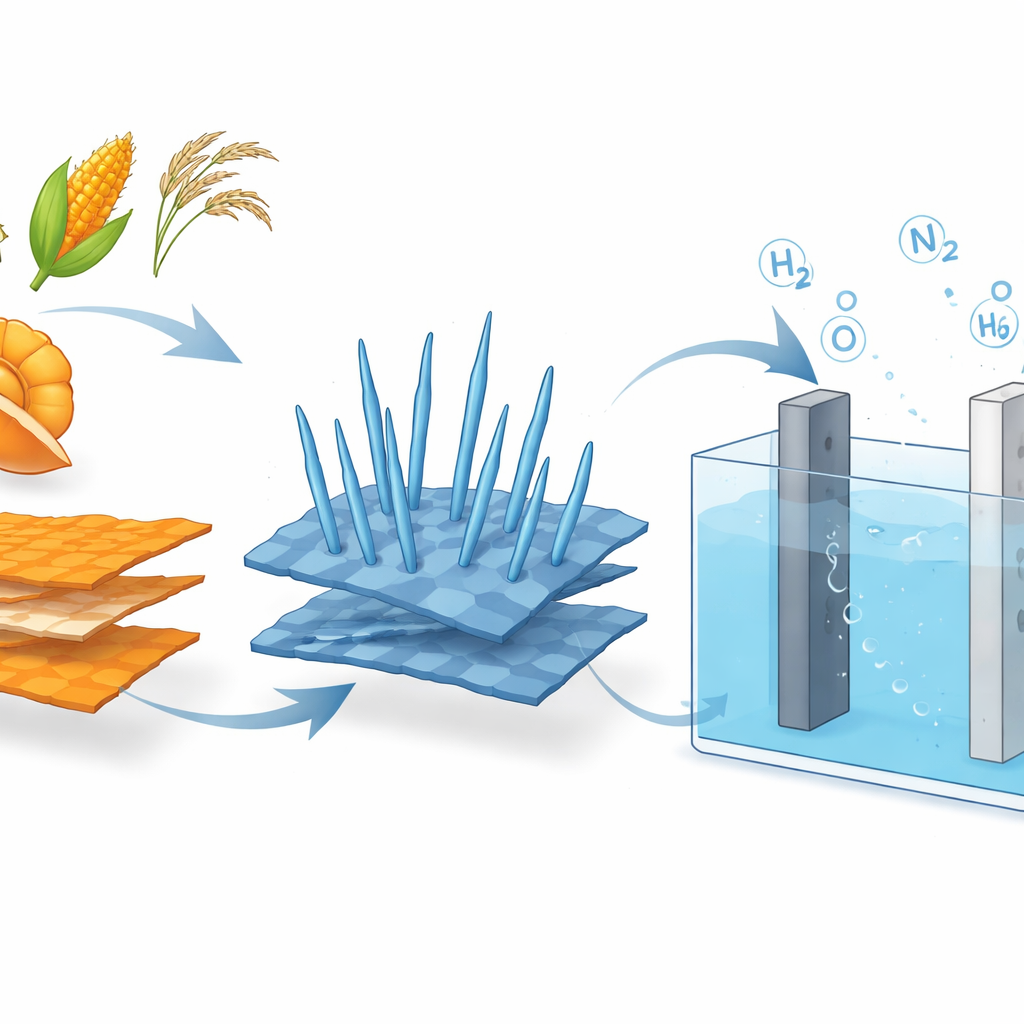
Por qué la separación tradicional del agua desperdicia energía
Para dividir el agua en hidrógeno y oxígeno, un electrolizador hace pasar corriente eléctrica por agua que contiene una sal o una base disuelta. En un lado se forma el gas hidrógeno con relativa facilidad. En el otro, se produce oxígeno en una reacción lenta y exigente, porque debe mover cuatro electrones en pasos muy coordinados. Este paso de producción de oxígeno, llamado reacción anódica, es lo que obliga a los ingenieros a aumentar el voltaje, elevando los costes energéticos. Peor aún, el oxígeno suele ventearse y no aprovecharse, lo que significa que gran parte de la energía eléctrica suministrada no genera un valor práctico equivalente.
Cambiar un consumidor de energía por reacciones más suaves
El equipo abordó este cuello de botella rediseñando lo que ocurre en el lado de la celda que consume más energía. En lugar de generar oxígeno a partir del agua, se plantearon: ¿y si el sistema oxidara otros químicos más fáciles de manejar mientras sigue produciendo hidrógeno en el lado opuesto? Eligieron dos compuestos ricos en nitrógeno, la urea y la hidrazina, que son comunes en corrientes de aguas residuales y procesos industriales. Cuando estas moléculas se oxidan en solución alcalina, se descomponen en gas nitrógeno, agua y, en el caso de la urea, dióxido de carbono. De forma crucial, estas reacciones comienzan a voltajes mucho más bajos que la producción de oxígeno, lo que significa que se puede generar la misma cantidad de hidrógeno con mucha menos energía eléctrica.
De las pieles de naranja a electrodos inteligentes
Para que este enfoque fuera práctico, los investigadores necesitaron un catalizador barato, robusto y activo para tres tareas distintas: la producción convencional de oxígeno, la oxidación de urea y la oxidación de hidrazina. Comenzaron convirtiendo pieles de naranja secas en óxido de grafeno, un material de carbono fino y conductor, mediante un proceso de calentamiento simple en lugar de tratamientos químicos agresivos. Sobre estas láminas crecieron diminutas «agulillas» de óxido de cobalto en un vaso de presión. El híbrido resultante—agulillas de óxido de cobalto sobre óxido de grafeno—forma una superficie rugosa y esponjosa con muchos sitios reactivos expuestos y un camino fácil para que circulen los electrones. Las mediciones mostraron que el soporte de grafeno evita que las partículas de cobalto se agrupen y aumenta dramáticamente el área superficial efectiva y la conductividad eléctrica.
Cómo el nuevo catalizador reduce la factura eléctrica
Cuando se probó en solución alcalina, el nuevo electrodo alcanzó una corriente de referencia estándar a voltajes significativamente más bajos que el óxido de cobalto puro. Para la producción convencional de oxígeno, su rendimiento fue comparable al de algunos catalizadores comerciales de metales nobles. Al añadir urea, el voltaje requerido bajó aún más, y con hidrazina la mejora fue notable: el electrodo necesitó solo un pequeño sobrepotencial por encima del nivel de referencia para mantener la misma corriente. En una celda completa de dos electrodos emparejada con un electrodo hidrofílico estándar a base de platino para producir hidrógeno, la electrólisis asistida por hidrazina generó hidrógeno a solo 0,33 voltios—unos 1,3 voltios menos que la separación del agua tradicional en las mismas condiciones. El sistema también se mantuvo estable durante muchas horas, con la estructura y la composición del catalizador esencialmente sin cambios.
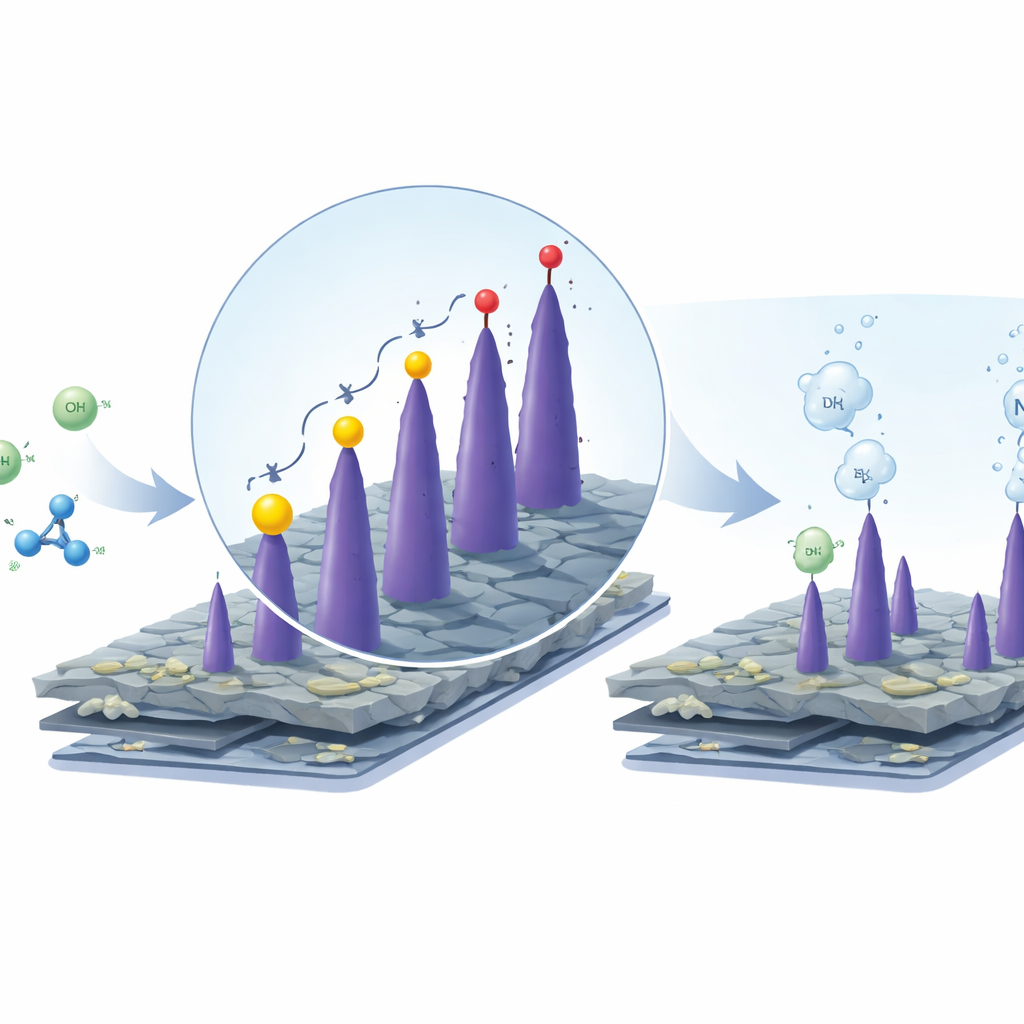
Qué significa esto para el hidrógeno limpio
Para un público no especializado, la conclusión es simple: al repensar tanto el material del electrodo como la reacción que tiene lugar en él, los investigadores demostraron que se puede producir hidrógeno usando mucha menos electricidad y con ingredientes económicos. Los residuos de fruta se convierten en un andamiaje de carbono de alto rendimiento; las agulillas de óxido de cobalto proporcionan sitios activos; y reemplazar la formación de oxígeno por la oxidación de urea o hidrazina reduce drásticamente el voltaje necesario. En el caso de la hidrazina, los subproductos son principalmente nitrógeno y agua, evitando emisiones carbonadas adicionales. Aunque se necesita más trabajo para gestionar el suministro químico y la seguridad a escala, esta estrategia de electrólisis híbrida apunta hacia una producción de hidrógeno más limpia y barata que además valoriza corrientes de residuos y biomasa renovable.
Cita: Rahamathulla, N., Murthy, A.P. Co3O4 nanoneedles grown on graphene oxide as an efficient electrocatalyst for hybrid water electrolysis through alternative anodic oxidation reactions. Sci Rep 16, 8452 (2026). https://doi.org/10.1038/s41598-026-35522-5
Palabras clave: producción de hidrógeno, electrólisis del agua, óxido de grafeno, oxidación de hidrazina, catalizadores derivados de biomasa