Clear Sky Science · es
Desarrollo estructural y computacional respaldado de análogos 2,5-disustituidos de 1,3,4-oxadiazol como inhibidores activos de LOX, ureasa y α-glucosidasa
Nuevas herramientas químicas para abordar enfermedades comunes
Muchos problemas de salud cotidianos —desde úlceras y cálculos renales hasta la diabetes y la inflamación crónica— están impulsados por enzimas hiperactivas en nuestro organismo. Este estudio explora una familia de pequeñas moléculas recientemente diseñadas que actúan como diminutos frenos para tres de esas enzimas. Al ajustar sus estructuras y evaluarlas en el laboratorio y mediante simulaciones por ordenador, los investigadores pretenden sentar las bases para fármacos futuros más eficaces y seguros. 
Por qué importan estas enzimas
El equipo se centró en tres dianas enzimáticas que desempeñan roles muy distintos pero igualmente importantes en la salud. La ureasa ayuda a descomponer la urea; cuando se vuelve hiperactiva en ciertas bacterias o tejidos, puede contribuir a úlceras gástricas y del tracto urinario, cálculos renales e incluso a un aumento de la presión arterial. La alfa-glucosidasa se encuentra en la superficie de las células intestinales y corta los carbohidratos complejos en glucosa; bloquearla es una estrategia bien establecida para controlar la glucemia en la diabetes tipo 2. La lipoxigenasa (LOX) convierte lípidos en moléculas señal que impulsan la inflamación, el asma y algunos procesos relacionados con el cáncer. Por ello, se buscan fármacos que atenúen estas enzimas sin dañar otros sistemas.
Construyendo una biblioteca de moléculas candidatas
Para buscar estos fármacos, los investigadores construyeron una serie de 15 compuestos relacionados basados en un sistema de anillo llamado 1,3,4-oxadiazol enlazado a una unidad piperidina. Este andamiaje químico ya aparece en varios medicamentos modernos y es conocido por interactuar bien con dianas biológicas. El equipo varió las “decoraciones” unidas a este núcleo —grupos pequeños como metilo, etilo, metoxi, bencilo y ciclohexilo— en diferentes posiciones, creando una pequeña biblioteca de candidatos etiquetados 7a a 7o. Confirmaron cada estructura mediante herramientas analíticas estándar como espectroscopía infrarroja y resonancia magnética nuclear, asegurando que lo sintetizado coincidía con sus diseños.
Probando la capacidad de las moléculas para bloquear enzimas
Cada compuesto se probó luego frente a LOX, ureasa y alfa-glucosidasa purificadas para evaluar cuánto podían ralentizar la actividad enzimática. Varios compuestos destacaron. Frente a la alfa-glucosidasa, los compuestos 7a y 7n fueron particularmente efectivos, superando al fármaco estándar para la diabetes acarbosa en las pruebas de laboratorio al lograr altos porcentajes de inhibición a concentraciones micromolares bajas. Para LOX, los compuestos 7a, 7h y 7n mostraron una actividad muy fuerte, en algunos casos mejor que el inhibidor de referencia natural quercetina. En los ensayos de ureasa, los compuestos 7a y en especial 7l rivalizaron o incluso superaron ligeramente al inhibidor estándar tio urea, lo que sugiere que podrían, en el futuro, servir como candidatos para terapias anti-úlcera o anti-cálculos. 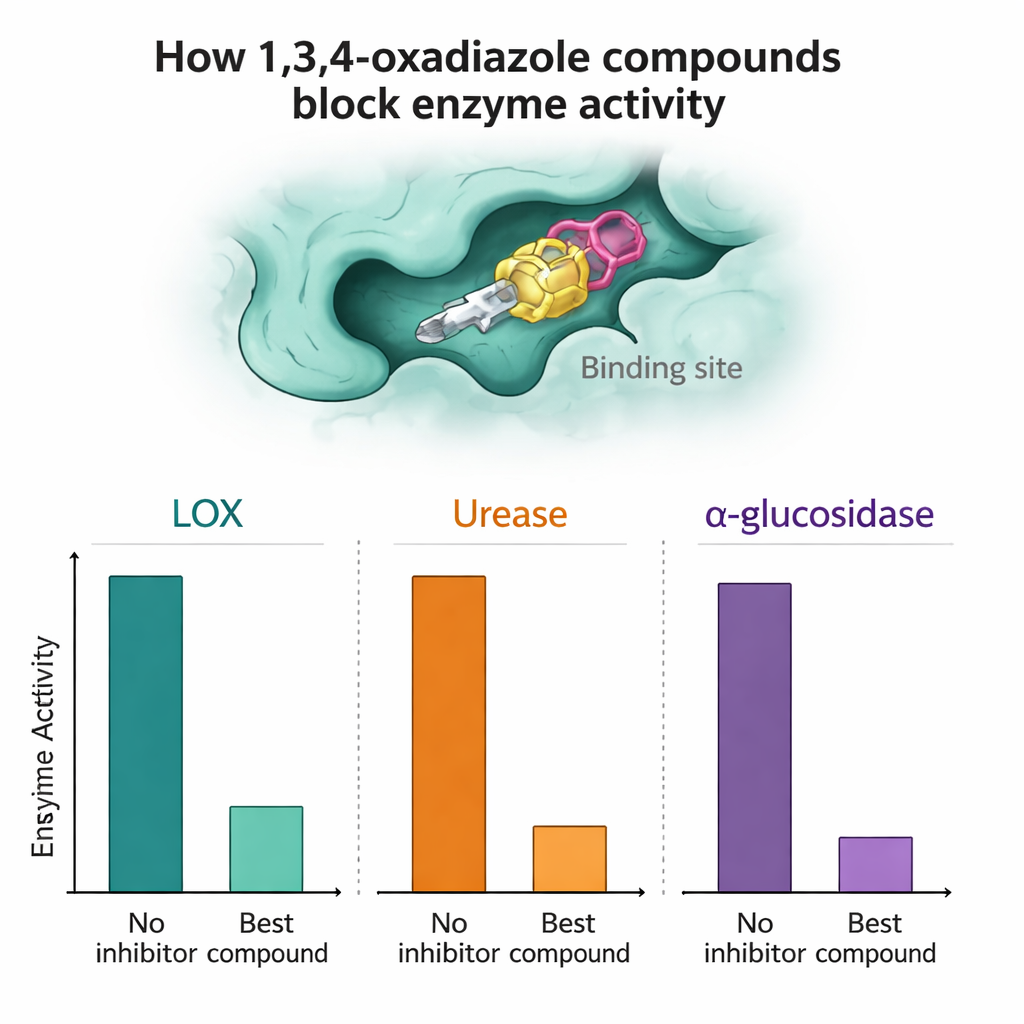
Relacionando la estructura con el rendimiento
Dado que las únicas diferencias entre los compuestos 7a–7o son pequeños cambios alrededor del sistema de anillo central, los investigadores pudieron comenzar a trazar relaciones sencillas entre estructura y actividad. Por ejemplo, añadir pequeños grupos ricos en carbono en ciertas posiciones “orto” de un anillo adjunto a menudo aumentaba la capacidad de bloquear la alfa-glucosidasa o la LOX. Otras sustituciones, como determinados grupos metoxi o éster colocados en posiciones menos favorables, tendían a debilitar la actividad. Para entender por qué, el equipo empleó simulaciones computacionales. Cálculos cuántico-químicos mostraron que todas las moléculas eran termodinámicamente estables y lo bastante flexibles para adaptarse a las cavidades enzimáticas. Estudios de acoplamiento (docking) —ajuste virtual de cada molécula en modelos tridimensionales de las enzimas— revelaron que los compuestos más activos establecían contactos más estrechos mediante una combinación de enlaces de hidrógeno e interacciones hidrofóbicas en puntos clave de los sitios activos, mientras que los candidatos más débiles encajaban peor o no establecían contactos críticos.
Qué significa esto para futuros fármacos
En términos cotidianos, el estudio identifica un puñado de “llaves” prometedoras que encajan bien en tres “cerraduras” relacionadas con enfermedades y comienza a explicar, a nivel atómico, por qué unas llaves giran mejor que otras. Ninguna de estas moléculas está aún lista para ser un fármaco: todavía requieren pruebas de seguridad, optimización de su comportamiento en el organismo y ensayos en animales y humanos. Pero el trabajo demuestra que el marco 1,3,4-oxadiazol–piperidina es un punto de partida fértil para futuros tratamientos dirigidos a la diabetes, condiciones inflamatorias y trastornos relacionados con la ureasa. La combinación de medidas experimentales cuidadosas con modelado computacional detallado proporciona una hoja de ruta para afinar estos candidatos hacia medicamentos más precisos y eficaces.
Cita: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Palabras clave: inhibidores de enzimas, descubrimiento de fármacos, compuestos oxadiazol, diabetes e inflamación, ureasa y lipoxigenasa