Clear Sky Science · es
SHP2 promueve el osteosarcoma regulando la vía STAT3/TET3/HOXB2
Por qué importa este estudio sobre el cáncer óseo
El osteosarcoma es el cáncer óseo primario más frecuente en niños y adolescentes y, a pesar de la quimioterapia y la cirugía modernas, la supervivencia de los pacientes con enfermedad avanzada o en recaída apenas ha mejorado en décadas. Este estudio explora el cableado interno de las células de osteosarcoma para identificar qué moléculas actúan como “interruptores maestros” que ayudan a los tumores a crecer, diseminarse y resistir el tratamiento. Al descubrir una vía de control clave centrada en una proteína llamada SHP2, el trabajo señala nuevos objetivos farmacológicos que podrían, en el futuro, hacer las terapias contra el osteosarcoma más efectivas y precisas.
Siguiendo las pistas en la actividad génica tumoral
Los investigadores empezaron tratando el osteosarcoma como un problema de datos. Minaron conjuntos públicos de expresión génica que comparan muestras tumorales con tejido óseo normal y usaron herramientas estadísticas para detectar genes que se activaban o reprimían de forma consistente en el cáncer. Cientos de genes diferían, y muchos se agruparon en vías cancerígenas bien conocidas que impulsan el crecimiento, la supervivencia y el movimiento celular. Entre ellos, una proteína, SHP2, destacó como un nodo conectado con varios otros: el factor de señalización STAT3, la enzima modificadora del ADN TET3 y el regulador del desarrollo HOXB2. Esto sugirió que estas moléculas podrían formar una cadena conectada que ayuda a las células de osteosarcoma a comportarse de forma agresiva. 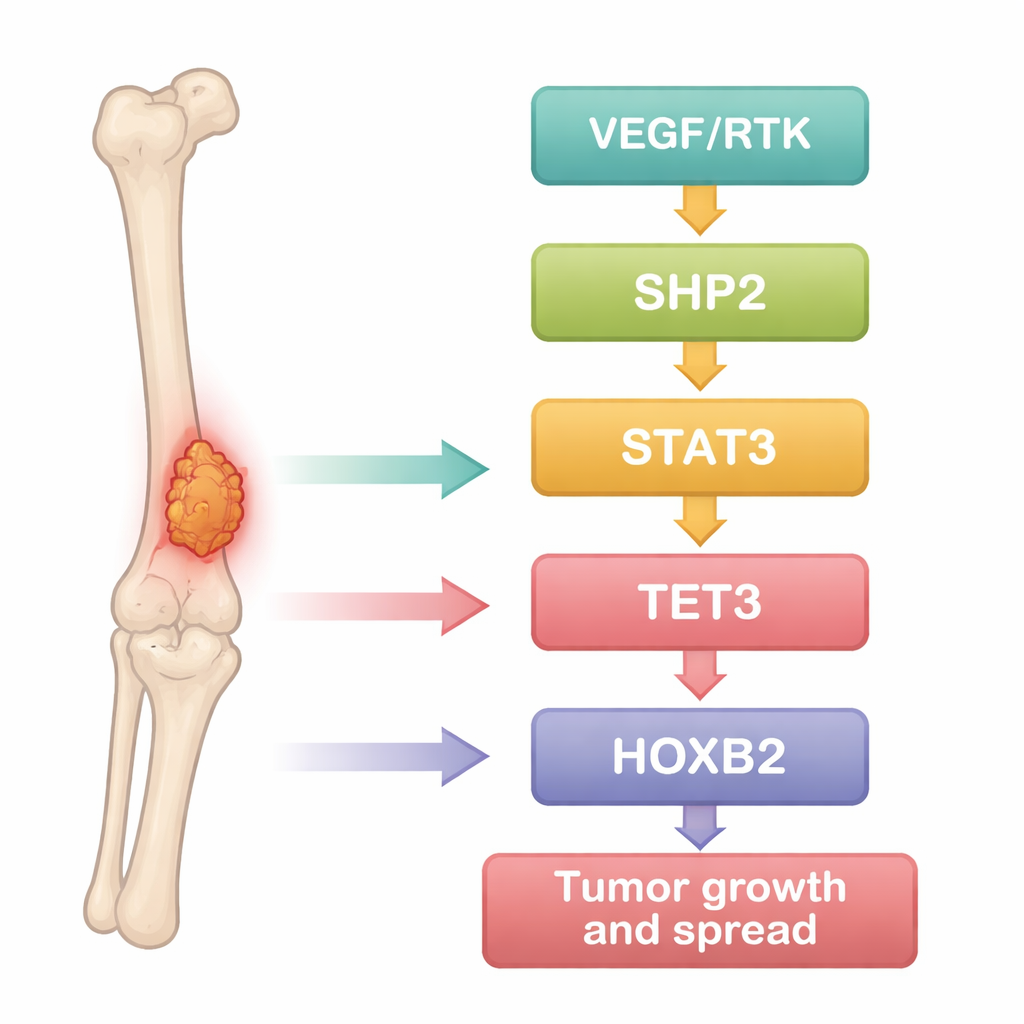
Comprobando el papel de SHP2 en células cancerosas
Para ir más allá de las correlaciones, el equipo modificó líneas celulares humanas de osteosarcoma (143B y MG63) para reducir o aumentar SHP2. Cuando disminuyeron SHP2, la capacidad de las células para multiplicarse, migrar por una superficie e invadir a través de una membrana cayó notablemente. También bajaron los niveles de las proteínas STAT3, TET3 y HOXB2, así como marcadores ligados al cáncer como c-Myc, NANOG y NUSAP1. Cuando reactivaron STAT3 o sobreexpresaron HOXB2, muchos de estos efectos se revirtieron, indicando que SHP2 se sitúa aguas arriba de una cadena que finalmente alimenta genes que controlan la división celular, rasgos tipo célula madre y la maquinaria de la mitosis.
Construyendo una vía tumoral paso a paso
Al reunir los experimentos, los autores describen un modelo escalonado. En el microambiente tumoral, altos niveles de factor de crecimiento endotelial vascular (VEGF) estimulan quinasas tirosina receptoras (RTK) en la superficie celular. Estas activan a su vez a SHP2 dentro de la célula. SHP2 activo enciende a STAT3, un factor de transcripción que se traslada al núcleo y contribuye a aumentar la producción de TET3. TET3 entonces edita las marcas químicas del ADN, eliminando específicamente grupos metilo de la región génica de HOXB2. Esta desmetilación actúa como quitar un freno, permitiendo que HOXB2 se exprese con mayor intensidad. HOXB2, un gen que normalmente guía el desarrollo, aumenta la actividad de c-Myc, NANOG y NUSAP1, que en conjunto alimentan el crecimiento desenfrenado de las células tumorales, potencian el comportamiento invasivo y sostienen rasgos asociados a la metástasis.
Del plato de cultivo a animales vivos
Para ver si esta vía tenía relevancia en tumores completos, los científicos implantaron células de osteosarcoma modificadas bajo la piel de ratones. Los tumores formados por células que sobreproducían SHP2 crecieron más y pesaron más que los tumores de control. Cuando TET3 se silenció en estas células ricas en SHP2, el crecimiento tumoral se ralentizó y los niveles de HOXB2 descendieron, aunque SHP2 y STAT3 permanecieron activos. Reintroducir HOXB2 restauró la vigorosidad del tumor. En todo momento, las mediciones de los niveles proteicos en el tejido tumoral reflejaron los hallazgos previos en cultivo celular, reforzando la idea de que SHP2, STAT3, TET3 y HOXB2 actúan como un eje conectado que empuja al osteosarcoma hacia un comportamiento más maligno. 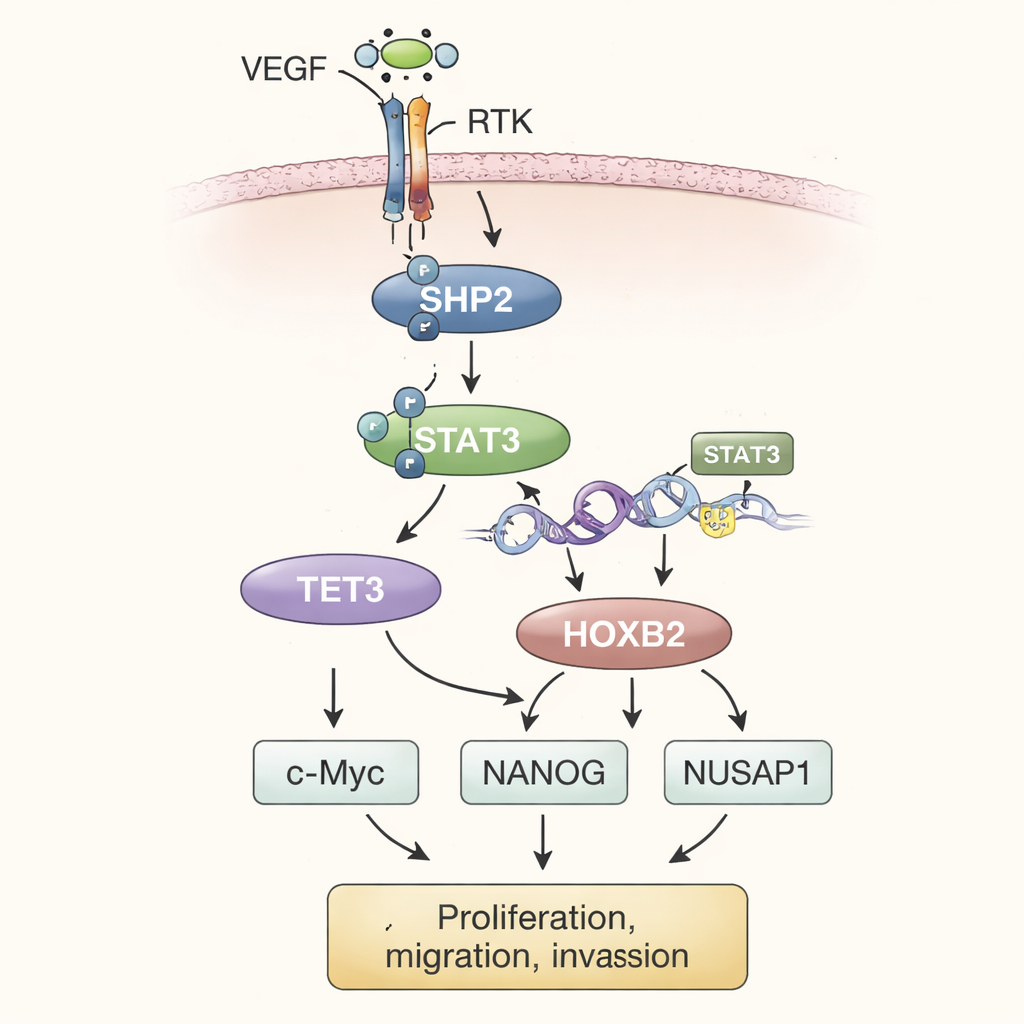
Qué significa esto para tratamientos futuros
Para un lector no especializado, la conclusión es que los investigadores han trazado una cadena de señal clara —desde VEGF y sus receptores de superficie, pasando por SHP2 y STAT3, hasta TET3, HOXB2 y varios genes potentes de crecimiento— que ayuda a explicar por qué el osteosarcoma puede crecer rápido y diseminarse pronto. Dado que SHP2 y STAT3 son enzimas que, en principio, pueden bloquearse con fármacos de pequeña molécula, y que TET3 y HOXB2 marcan pasos posteriores en la misma ruta, esta vía ofrece múltiples puntos donde futuras terapias podrían intervenir. Aunque este estudio se hizo en líneas celulares y en ratones, proporciona un mapa detallado que los desarrolladores de fármacos pueden usar para diseñar tratamientos combinados destinados a apagar los interruptores centrales del tumor en lugar de limitarse a atacar sus resultados finales.
Cita: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Palabras clave: osteosarcoma, SHP2, vía STAT3, señalización tumoral, terapia dirigida