Clear Sky Science · es
Desarrollo de un sistema de cribado global para detectar interacciones proteína–proteína mediante complementación de luminiscencia en levadura fisionante
Iluminando la vida oculta de las proteínas
Cada latido, pensamiento y respiración en nuestro cuerpo depende de que las proteínas se asocien dentro de las células. Estas diminutas colaboraciones, llamadas interacciones proteína–proteína, controlan todo, desde cómo se leen los genes hasta cómo responden las células al estrés. Sin embargo, muchas de estas asociaciones son fugaces o delicadas, lo que dificulta su detección con las herramientas actuales. Este estudio describe un nuevo sistema de cribado «basado en luz», muy sensible, construido en un organismo modelo sencillo, la levadura fisionante, para revelar miles de estas conexiones proteicas ocultas a la vez.
Por qué es tan difícil ver las asociaciones proteicas
Las proteínas rara vez actúan solas. Se unen a distintos socios en momentos distintos, a veces solo por instantes, y su comportamiento puede alterarse por modificaciones químicas o por su ubicación dentro de la célula. Los métodos tradicionales para estudiar estas interacciones o bien extraen las proteínas de su entorno natural o dependen de artificios genéticos que no capturan todos los emparejamientos. Como resultado, los mapas existentes sobre quién interactúa con quién en la célula son incompletos. Los autores se propusieron mejorar esta visión creando un sistema más flexible y sensible que pudiera sondear casi cada proteína de la levadura fisionante en células vivas.
Convertir el contacto en luz
En el centro del nuevo enfoque hay una enzima dividida que emite luz. Una parte, llamada LgBiT, se une a una proteína «cebo» que los investigadores quieren estudiar. La otra parte, SmBiT, se une a muchos posibles «presas», una por cada cepa de levadura. Por sí solos, estos dos fragmentos enzimáticos apenas interactúan. Pero cuando las proteínas cebo y presa se unen dentro de la célula, las dos piezas se juntan, reconstituyendo una enzima funcional que brilla en presencia de un sustrato químico. Midiendo la luz que produce cada cepa de levadura, el equipo puede identificar qué proteínas se encuentran realmente dentro de la célula y con qué intensidad interactúan. Para evitar perder socios porque la etiqueta bloquee la función normal, la proteína cebo se diseñó en dos versiones, con LgBiT unido a cualquiera de los dos extremos, lo que aumenta mucho las probabilidades de que al menos una orientación funcione. 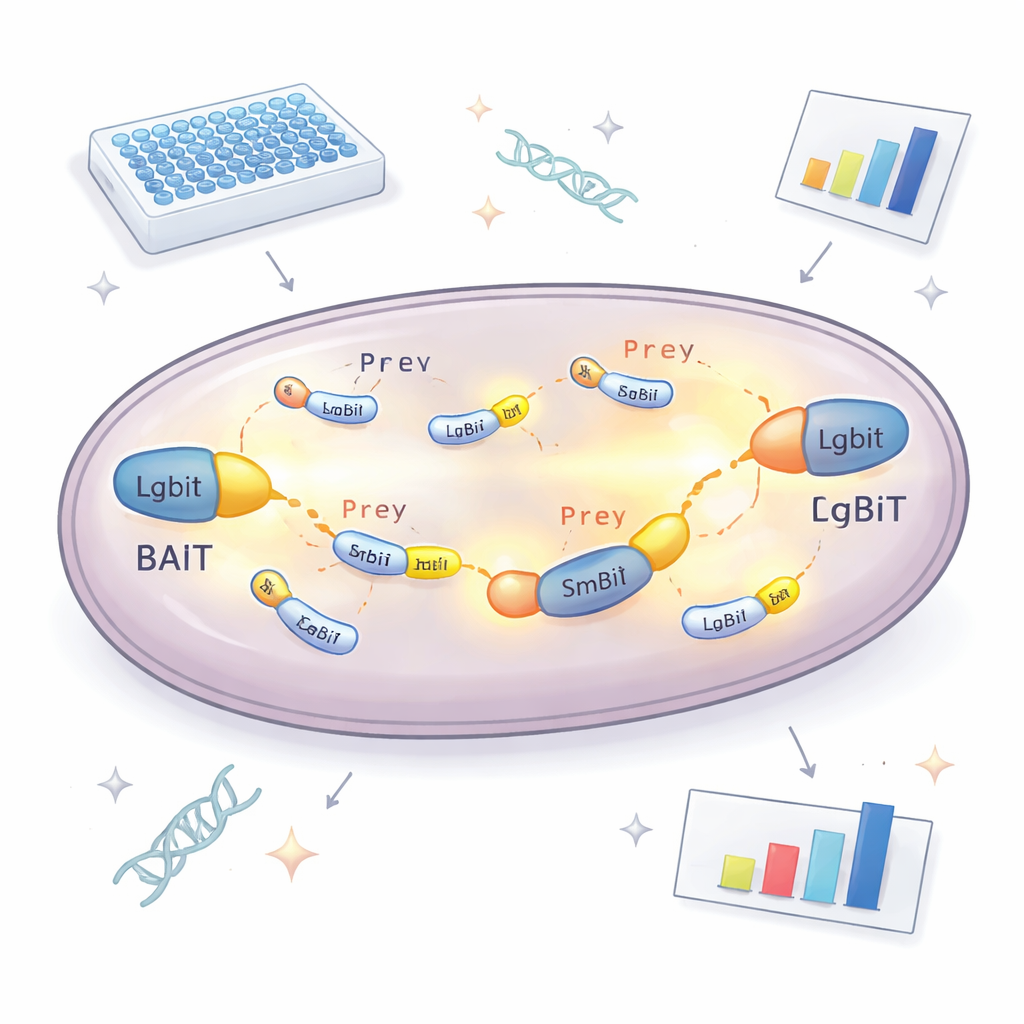
Ingeniería de una biblioteca de levaduras y un sistema de cepas
Construir esta plataforma requirió algo más que una enzima ingeniosa. Los investigadores también tuvieron que introducir miles de proteínas presa en la levadura de forma controlada y en copia única. Diseñaron un vector de ADN especial para las presas que se inserta en un lugar definido del genoma de la levadura y que porta un marcador fluorescente rojo. La intensidad de esta señal roja refleja cuántas copias se han insertado, permitiendo al equipo seleccionar fácilmente colonias con exactamente una copia, lo cual es esencial para comparaciones fiables. También crearon vectores cebo dedicados que sitúan LgBiT al principio o al final de la proteína cebo, separados por enlaces flexibles para que la proteína pueda plegarse y moverse con normalidad. A continuación, se construyeron cepas de levadura cuidadosamente diseñadas para alojar dos constructos cebo y un constructo presa a la vez, usando marcadores nutricionales para asegurar que solo sobrevivan las células combinadas correctamente.
Poniendo el sistema a prueba
Para comprobar si su diseño mejoraba realmente la detección, los científicos examinaron primero proteínas con socios bien conocidos. Confirmaron que la intensidad de la señal dependía en gran medida de dónde se colocaba la etiqueta emisora de luz: algunas interacciones solo se detectaron cuando LgBiT estaba en un extremo del cebo y no en el otro. Expresar ambas versiones simultáneamente aumentó la señal luminosa, demostrando que la estrategia de doble cebo facilita la detección de interacciones débiles o sensibles a la orientación. El sistema también detectó contactos que implican proteínas de membrana, una clase que resulta notoriamente difícil para los métodos tradicionales de doble híbrido en levadura. Con esta validación, el equipo amplió el método a un cribado a escala genómica, usando como cebo una proteína relacionada con la transcripción llamada Tfs1. Al cribar más de 4.600 proteínas presa, encontraron 31 candidatos fuertes, incluidos varios socios ya conocidos y muchos nuevos, algunos localizados fuera del núcleo en áreas como las mitocondrias y la superficie celular. 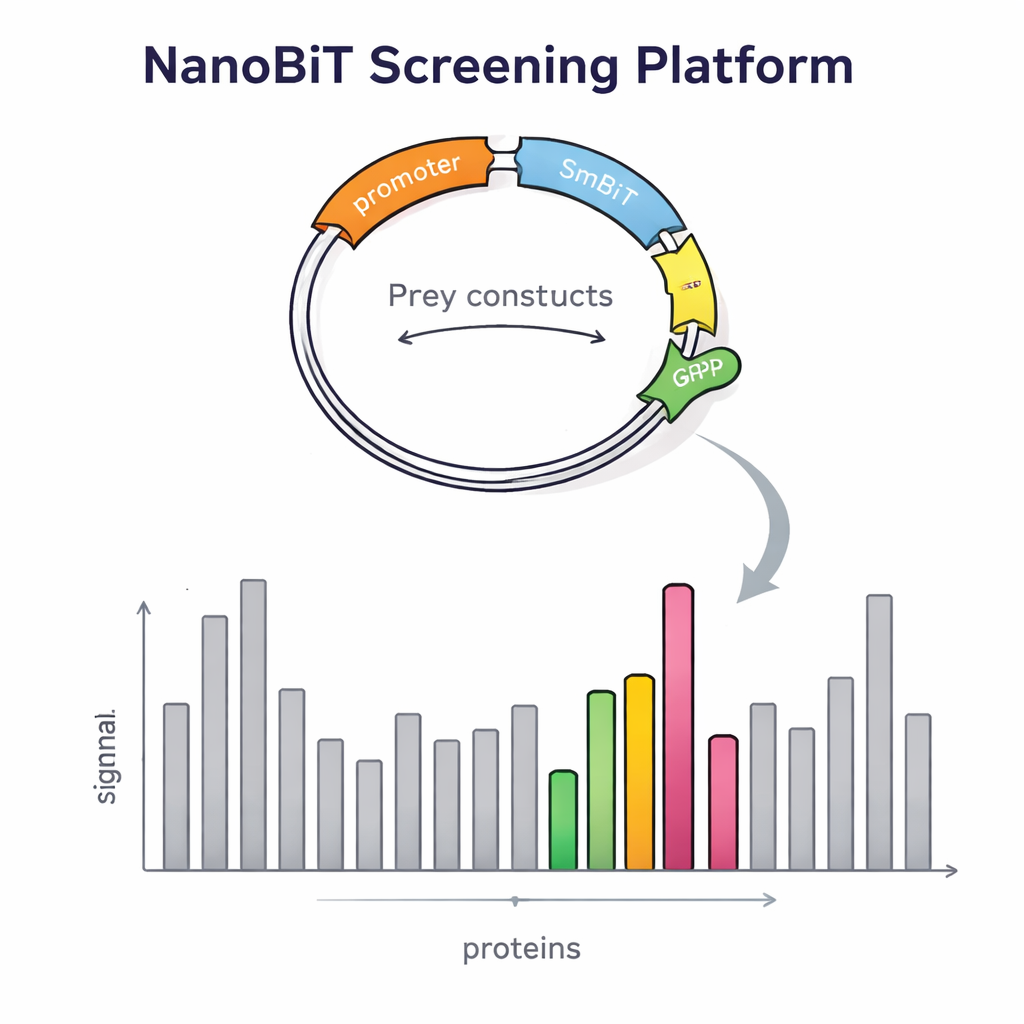
Qué implica esto para la biología y el descubrimiento de fármacos
Para un público no especialista, el mensaje clave es que los autores han construido un «radar de interacciones» más sensible dentro de células de levadura. Al convertir apretones de manos proteicos breves en destellos de luz medibles y al organizar genéticamente que puedan expresarse tres proteínas etiquetadas simultáneamente, su sistema descubre tanto socios conocidos como otros hasta ahora invisibles. Aunque siguen siendo necesarias comprobaciones adicionales con otras técnicas para confirmar cada nuevo emparejamiento, esta plataforma rellena lagunas importantes en nuestros mapas de las redes celulares. Dado que las cepas también se diseñaron para ser más sensibles a pequeñas moléculas, la misma configuración podría adaptarse para buscar fármacos que interrumpan asociaciones proteicas dañinas o que estabilicen las beneficiosas, ofreciendo una nueva herramienta potente tanto para la biología básica como para las etapas iniciales del descubrimiento de fármacos.
Cita: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Palabras clave: interacciones de proteínas, levadura fisionante, ensayo de luminiscencia, cribado de alto rendimiento, herramientas para el descubrimiento de fármacos