Clear Sky Science · es
Diagnóstico automático de la degeneración macular relacionada con la edad mediante aprendizaje automático y técnicas de procesamiento de imágenes
Por qué esto importa para su vista
A medida que la población envejece, más personas enfrentan la degeneración macular relacionada con la edad (DMAE), una enfermedad que erosiona gradualmente la visión central y puede dificultar o impedir actividades como leer, conducir o reconocer rostros. Los oftalmólogos pueden detectar señales tempranas en fotografías del fondo del ojo, pero hacerlo a mano para miles de pacientes consume mucho tiempo y requiere especialistas. Este estudio explora cómo una herramienta transparente basada en aprendizaje automático puede ayudar a detectar la DMAE de forma temprana a partir de fotografías rutinarias del ojo, sin depender de las frágiles y poco explicables «cajas negras» de aprendizaje profundo.
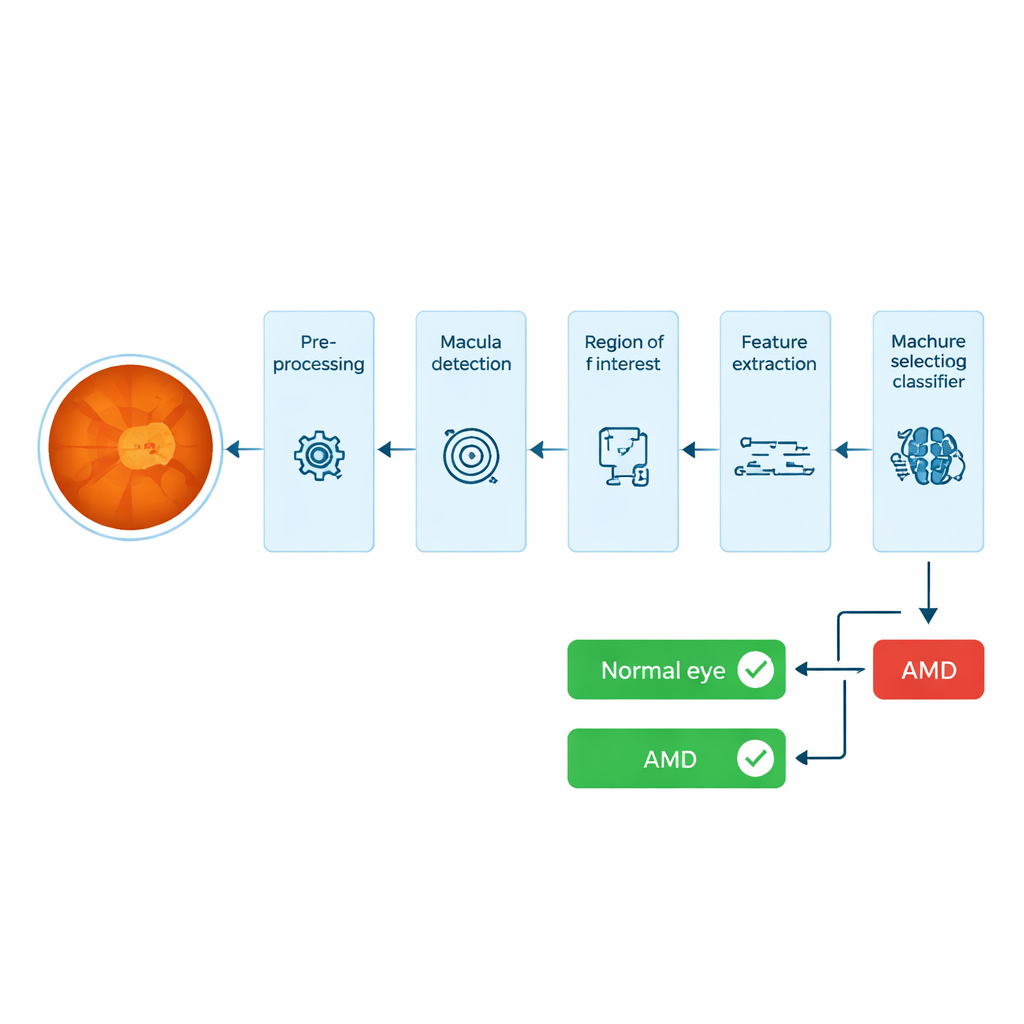
Buscando problemas en la zona de visión nítida del ojo
La DMAE ataca la mácula, una pequeña zona oscura cerca del centro de la retina que proporciona visión nítida y detallada. Muchos sistemas automáticos intentan localizar diminutos depósitos grasos llamados drusas en imágenes de toda la retina, pero las drusas pueden confundirse fácilmente con otros puntos brillantes como pequeños sangrados y presentan gran variabilidad en forma y tamaño. Eso hace que su detección por ordenador sea difícil de fiabilizar, y aun los expertos deben revisar cuidadosamente los resultados. Los autores siguen un camino distinto: en vez de buscar drusas por toda la retina, se centran en la región macular y miden cómo cambian su textura y color cuando existe DMAE.
De la foto sin procesar a la «huella» de la mácula
El sistema parte de una fotografía en color del fondo del ojo, llamada imagen de fondo (fundus). Primero mejora el contraste usando pasos estándar de procesamiento de imágenes para que las zonas oscuras y claras sean más distinguibles. A continuación, localiza automáticamente el disco óptico —la zona circular y brillante por donde salen los nervios del ojo— y, usando la relación geométrica conocida con la mácula, busca a lo largo de una franja estrecha la región más oscura que encaje con el tamaño y la posición esperados de la mácula. Alrededor de ese punto, el sistema recorta un pequeño rectángulo: esta es la región de interés, que contiene el tejido con mayor probabilidad de mostrar daños tempranos relacionados con la DMAE.
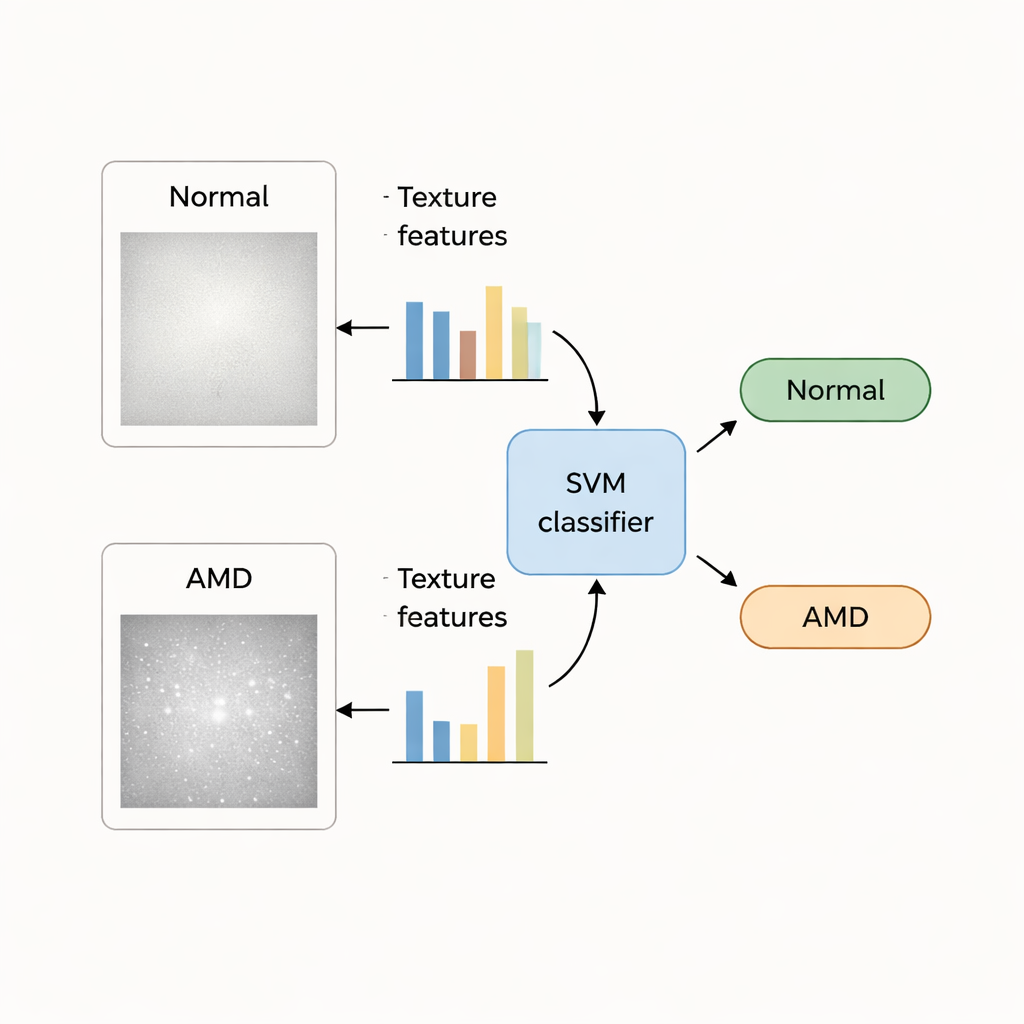
Transformar patrones y colores en números
Dentro de este parche macular, los investigadores calculan un amplio conjunto de descriptores numéricos, o «características diseñadas a mano». Las características de textura capturan cómo se distribuyen las intensidades de los píxeles —si la superficie se ve lisa, moteada o irregular—, mientras que las de color registran cambios en brillo y tono que pueden reflejar variaciones en el pigmento y la salud del tejido. En total se miden 140 valores de textura y 48 de color para cada imagen ocular. Dado que no todos estos números son igualmente útiles, el equipo aplica pruebas estadísticas y un método de ordenación de características para seleccionar un subconjunto más pequeño que mejor separa ojos sanos y con DMAE, eliminando mediciones redundantes o ruidosas.
Entrenar a las máquinas para decir «DMAE» o «normal»
Con estas características seleccionadas, los autores entrenan varios clasificadores bien conocidos de aprendizaje automático —Máquina de Vectores de Soporte (SVM), k‑Vecinos más cercanos, Naïve Bayes y una red neuronal simple— para aprender la diferencia entre ojos normales y ojos afectados por DMAE. Utilizan dos colecciones públicas de imágenes de retina: el conjunto STARE, que incluye 35 imágenes normales y 74 con DMAE, y el mayor conjunto ODIR, con cientos de casos etiquetados. Para evaluar la fiabilidad, dividen repetidamente cada conjunto en porciones de entrenamiento y prueba, rotando las imágenes para que cada ojo sirva como prueba al menos una vez, y miden la precisión, la tasa de error y la frecuencia con que se detecta correctamente la DMAE.
Resultados claros y razonamiento más claro
En todas las pruebas, el clasificador SVM que utiliza características de textura de la región macular destaca. En el conjunto STARE, distingue correctamente la DMAE de ojos normales casi el 99% de las veces; en ODIR, la precisión ronda el 95%. La información de textura resulta más potente que el color por sí solo, y la combinación de ambos tipos de características no supera el rendimiento de la textura por sí misma. Aunque algunos sistemas de aprendizaje profundo de la literatura alcanzan puntuaciones comparables o ligeramente superiores, requieren grandes cantidades de datos etiquetados y ofrecen poca información sobre las claves de imagen que utilizan. En contraste, las características de textura y color diseñadas en este estudio se corresponden con estructuras reconocibles en la retina, lo que hace el sistema más interpretable para los clínicos.
Qué significa esto para los pacientes
En términos cotidianos, el estudio demuestra que un programa informático relativamente simple y transparente puede examinar una foto estándar del ojo, acercarse a la mácula y —con muy alta fiabilidad— señalar si probablemente existe DMAE, sin intentar primero rastrear cada pequeño depósito. Una herramienta así podría ayudar a clínicas oftalmológicas y programas de cribado a clasificar rápidamente grandes cantidades de imágenes, asegurando que los pacientes con enfermedad temprana sean derivados a especialistas antes, y al mismo tiempo proporcionando a los médicos una visión más clara de qué patrones visuales está usando la máquina para tomar su decisión.
Cita: Agarwal, D., Bhargava, A., Alsharif, M.H. et al. Automatic diagnosis of age-related macular degeneration using machine learning and image processing techniques. Sci Rep 16, 5037 (2026). https://doi.org/10.1038/s41598-026-35428-2
Palabras clave: degeneración macular relacionada con la edad, imágenes de la retina, aprendizaje automático, detección temprana de enfermedades, análisis de imágenes médicas