Clear Sky Science · es
Secretoma dependiente de la partícula de reconocimiento de señal en humanos
Cómo deciden las células qué proteínas salen de la célula
Nuestras células envían constantemente proteínas que forman hormonas, anticuerpos y la estructura entre tejidos. Pero no todas las proteínas están destinadas a viajar. Este estudio plantea una pregunta básica aún sin respuesta: ¿cómo deciden las células humanas qué proteínas necesitan de un ayudante clave llamado partícula de reconocimiento de señal (SRP) para llegar al centro de envío interno de la célula y cuáles pueden hacerlo sin ella? Al cartografiar esta decisión a través de miles de proteínas a la vez, los autores revelan quién depende de SRP, quién no, y qué ocurre cuando este sistema falla, un tema relevante para muchas enfermedades vinculadas a proteínas secretadas mal dirigidas o ausentes.
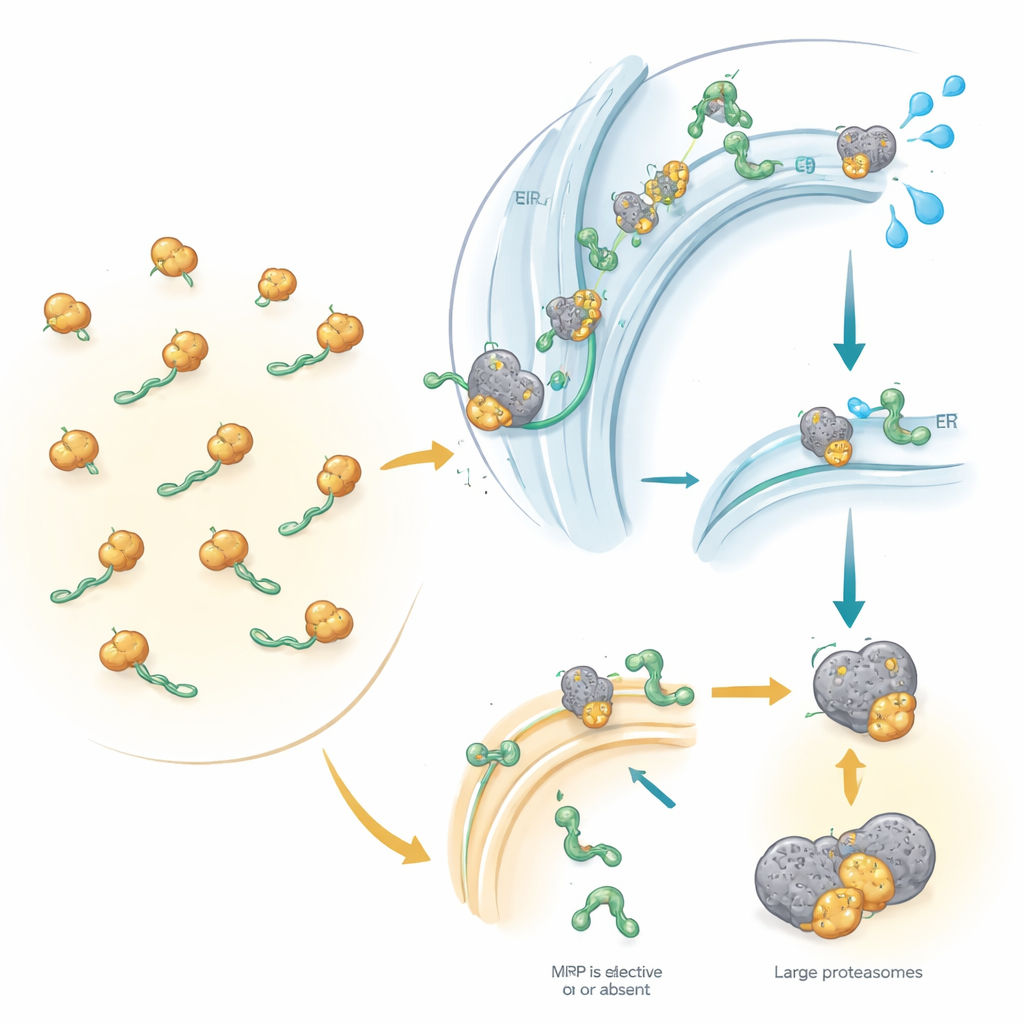
El muelle de envío de la célula y su guía principal
Aproximadamente una de cada tres proteínas humanas está destinada a la superficie celular, a las membranas celulares o a ser liberada fuera de la célula. Para alcanzar el lugar correcto, la mayoría de estas proteínas deben entrar primero en una red de membranas internas llamada retículo endoplásmico, el muelle de envío de la célula. La SRP actúa como guía: reconoce una pequeña «etiqueta de dirección» al principio de las proteínas recién sintetizadas y pausa temporalmente su producción. Esta pausa da tiempo al ribosoma —la máquina que fabrica proteínas— para acoplarse al retículo endoplásmico, donde la síntesis se reanuda y la proteína en crecimiento se introduce en o a través de la membrana. Sin embargo, se sabe que algunas proteínas usan rutas alternativas que no requieren SRP, especialmente las proteínas muy pequeñas o las ancladas por su extremo final. Hasta ahora, los científicos no sabían, a escala global, qué proteínas humanas requieren realmente la SRP y cuáles pueden evitarla.
Reducir la SRP para ver qué se rompe
Para responder a esto, los investigadores redujeron selectivamente los niveles de un componente esencial de la SRP, SRP54, en células humanas HeLa. Luego emplearon una técnica sensible llamada espectrometría de masas para medir más de 6.000 proteínas dentro de las células y casi 2.000 proteínas presentes en el líquido circundante, conocido como medio condicionado. Comparar células con niveles normales de SRP54 con aquellas con SRP54 reducido les permitió ver qué proteínas disminuían, cuáles aumentaban y cuáles permanecían sin cambios. Una fuerte caída en el nivel de una proteína —especialmente tanto dentro de la célula como en el medio— se interpretó como una señal de que esa proteína depende de la SRP para ser sintetizada y dirigida correctamente.
Quién depende de la SRP y quién se las arregla sin ella
El análisis mostró que la mayoría de las proteínas normalmente secretadas en el medio dependen claramente de la SRP. Cuando SRP54 se redujo, la mayor parte de estas proteínas secretadas, especialmente las que portan una etiqueta de señal clásica, disminuyeron drásticamente. Muchas proteínas de membrana dentro de la célula también se redujeron, revelándolas como clientes de la SRP. Un conjunto más pequeño de proteínas con etiquetas de señal similares no se vio mayormente afectado, marcándolas como independientes de la SRP; probablemente usan rutas alternativas para llegar al retículo endoplásmico. Los investigadores también descubrieron que características específicas de la etiqueta de señal —como una región cargada positivamente al inicio— eran más comunes entre las proteínas dependientes de SRP, lo que sugiere reglas sutiles que ayudan a la SRP a elegir su carga. Al mismo tiempo, algunas proteínas implicadas en etiquetar proteínas dañadas para su destrucción y en la función mitocondrial aumentaron, lo que sugiere que las células activan sistemas de respaldo y la producción de energía cuando su guía principal de envío está comprometida.
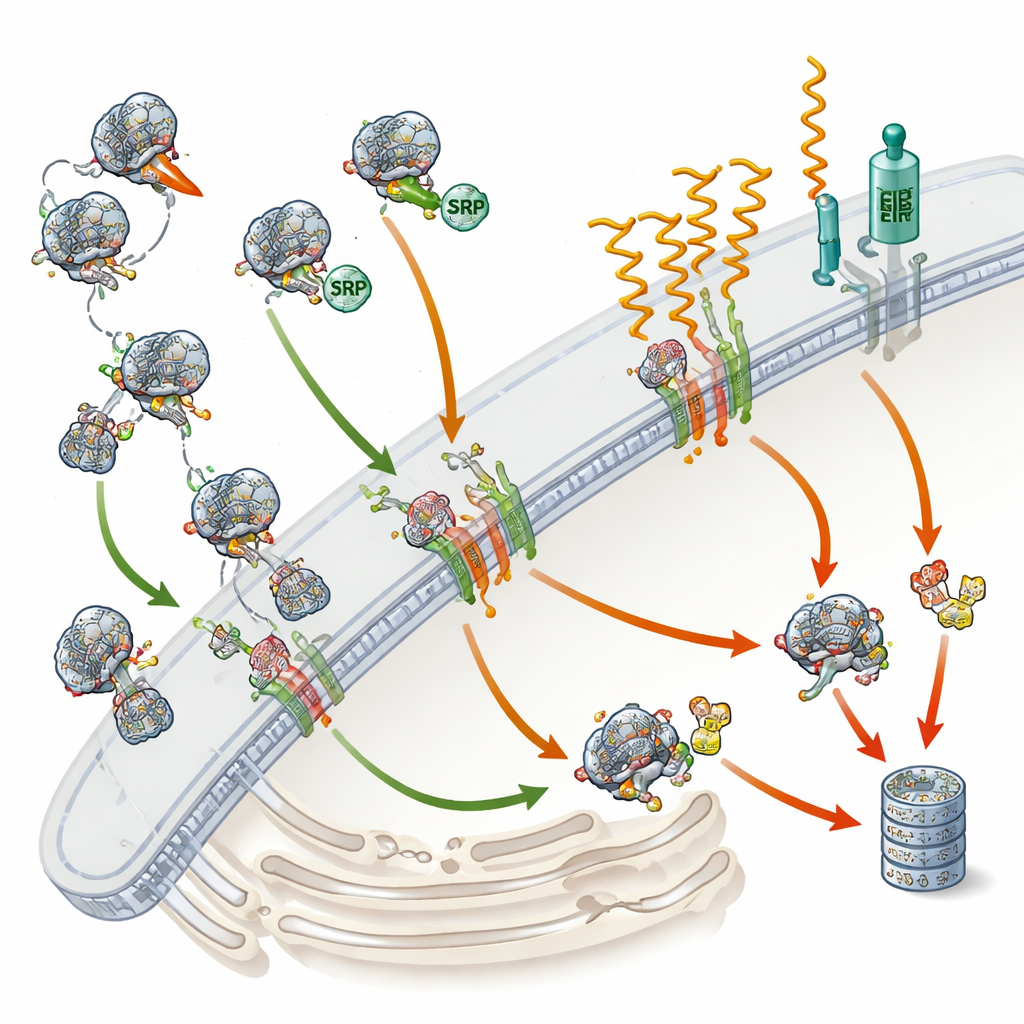
Control de calidad cuando el direccionamiento falla
El estudio fue más allá del recuento de proteínas: comparó estos cambios con variaciones en el ARN mensajero, los planos utilizados para fabricar proteínas. Muchas proteínas dependientes de SRP perdieron no solo la proteína sino también sus planos de ARN, implicando una vía de control de calidad conocida como RAPP. Cuando la SRP no puede involucrarse correctamente con una proteína secretoria o de membrana emergente, esta vía parece desencadenar la degradación del ARN correspondiente, impidiendo la producción continua de una proteína mal dirigida. Al mismo tiempo, las proteínas incompletas que no logran alcanzar el retículo endoplásmico probablemente son etiquetadas con pequeñas banderas moleculares y enviadas a los “trituradores” celulares llamados proteasomas. Curiosamente, las vías clásicas de estrés en el retículo endoplásmico no se activaron de forma pronunciada, lo que sugiere que la deficiencia de SRP provoca un tipo de respuesta al estrés celular distinto.
Qué significa esto para la salud y la enfermedad
Al cartografiar, por primera vez en células humanas, qué proteínas secretadas y de membrana son dependientes de SRP y cuáles son independientes, este trabajo proporciona un mapa de referencia de las reglas de envío celular. Los hallazgos muestran que la mayoría de las proteínas exportadas dependen realmente de la SRP y que, cuando la SRP falla, las células responden degradando tanto las proteínas como sus planos mientras activan mecanismos alternativos de afrontamiento. Dado que muchas mutaciones causantes de enfermedades afectan las «etiquetas de dirección» en proteínas secretadas, comprender exactamente cómo la SRP reconoce a sus clientes y cómo RAPP elimina a los defectuosos puede ayudar a explicar por qué ciertas mutaciones conducen a deficiencias hormonales, problemas inmunitarios o neurodegeneración, y potencialmente señalar nuevas vías para ajustar el direccionamiento de proteínas en la salud humana.
Cita: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Palabras clave: secreción de proteínas, partícula de reconocimiento de señal, secretoma, control de calidad de proteínas, retículo endoplásmico