Clear Sky Science · es
La inhibición secuencial con platino y PARP mejora la eficacia de la inmunoterapia PD1 en un modelo murino de cáncer pancreático con mutación Brca2
Por qué esta investigación importa para los pacientes
El cáncer de páncreas es uno de los más letales y, aunque los médicos identifiquen una vulnerabilidad útil en el tumor —por ejemplo, una mutación en el gen BRCA2—, los tratamientos actuales rara vez controlan la enfermedad por mucho tiempo. Este estudio utiliza un modelo murino realista para plantear una pregunta práctica que afrontan muchos pacientes y oncólogos hoy en día: después de una quimioterapia intensiva y un inhibidor de PARP, ¿puede añadir la inmunoterapia moderna prolongar la supervivencia de forma significativa, y por qué los tumores vuelven con tanta frecuencia?
Un cáncer tercamente resistente con un punto débil genético
El adenocarcinoma ductal pancreático es notoriamente difícil de tratar, con una supervivencia a cinco años que sigue en cifras muy bajas. Una pequeña fracción de pacientes presenta defectos heredados o específicos del tumor en BRCA2, un gen necesario para reparar el ADN dañado. Estos tumores son inusualmente sensibles a fármacos que dañan el ADN, como la quimioterapia basada en platino, y a los inhibidores de PARP, que dificultan aún más la capacidad de las células cancerosas para reparar su ADN. La atención estándar actual para el cáncer pancreático avanzado con mutación BRCA es varios meses de quimioterapia con platino seguidos de tratamiento de mantenimiento con un inhibidor de PARP. Sin embargo, en el ensayo clínico clave POLO, esta estrategia no prolongó la supervivencia global, lo que subraya la necesidad de comprender la resistencia y diseñar enfoques de mantenimiento mejores.
Construyendo un modelo murino más realista
Muchos modelos de laboratorio eliminan componentes inmunitarios y estromales que rodean a los tumores reales en los pacientes. Para superar esto, los autores diseñaron ratones que desarrollan tumores pancreáticos deficientes en BRCA2 en el contexto de un sistema inmunitario completamente funcional. A partir de estos tumores espontáneos obtuvieron líneas celulares clónicas que podían implantarse en ratones genéticamente emparejados. Estos tumores con mutación en Brca2 se parecían y se comportaban de manera muy similar a los cánceres pancreáticos humanos: presentaban fibrosis densa, exclusión generalizada de células T y altos niveles de daño espontáneo del ADN. De forma crucial, los tumores eran muy sensibles a una combinación habitual de platino (gemcitabina más cisplatino), mientras que el tratamiento con inhibidor de PARP solo tuvo efectos modestos y de corta duración en los animales, a pesar de mostrar gran actividad contra las mismas células en cultivo. 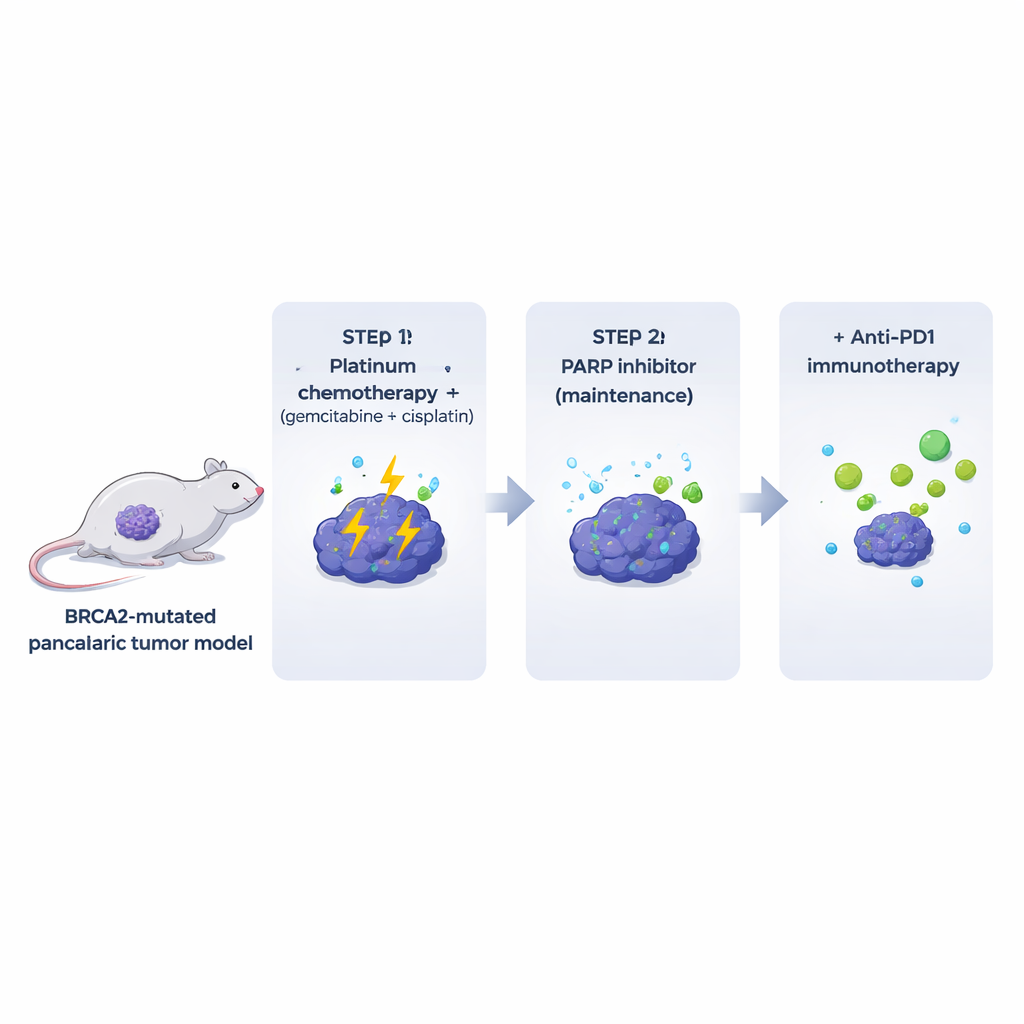
La quimioterapia remodela el vecindario tumoral
El equipo investigó a continuación qué ocurría dentro del tumor tras la quimioterapia con platino. Diez días después del tratamiento, los tumores se habían reducido pero no se habían erradicado. Los análisis de expresión génica revelaron un cambio llamativo hacia la actividad relacionada con el sistema inmunitario: se activaron vías vinculadas a la activación de células T y a la inmunidad adaptativa. Se detectaron más células T dentro de los tumores tratados, y muchas de esas células T mostraban marcadores de agotamiento —señales de que se habían activado pero estaban volviéndose ineficaces. Patrones similares de mayor presencia de células T se observaron en cánceres pancreáticos humanos con mutaciones en BRCA o en el gen relacionado PALB2 tras la administración de quimioterapia con platino antes de la cirugía. Al mismo tiempo, las células tumorales aumentaron los niveles de PD-L1, una proteína de superficie que puede desactivar las células T al interactuar con el receptor PD-1, lo que sugiere que los tumores se defendían contra esta nueva presión inmune.
Por qué PARP solo no basta — y dónde surge la resistencia
De manera análoga a la atención clínica, los investigadores administraron a los ratones un ciclo inicial de gemcitabina y cisplatino, seguido de mantenimiento con el inhibidor de PARP olaparib. Esta secuencia mejoró el control tumoral y la supervivencia en comparación con la quimioterapia sola, confirmando que la quimioterapia previa puede hacer que los tumores sean más susceptibles a la inhibición de PARP. Sin embargo, ningún ratón fue curado: los tumores eventualmente volvieron a crecer durante el mantenimiento con PARP. Los tumores resistentes mostraron una apariencia más diferenciada y aumentaron de forma marcada los niveles del regulador del desarrollo CDX2. Esto sugiere que, al menos en este modelo, la resistencia no surge simplemente por la reparación del defecto original en la reparación del ADN, sino que puede implicar un cambio en la identidad celular del tumor. CDX2 podría servir potencialmente como biomarcador de resistencia emergente en pacientes.
Desbloquear la inmunoterapia con la secuencia adecuada
Los fármacos que bloquean puntos de control inmunitario, como los anticuerpos anti‑PD1, han transformado el tratamiento de varios cánceres, pero el cáncer pancreático ha permanecido en gran medida poco sensible. En consonancia con ello, anti‑PD1 (con o sin otro inhibidor de punto de control, anti‑CTLA4) no ayudó cuando se administró a tumores con mutación BRCA2 no tratados previamente, y tampoco aportó mucho cuando se añadió simplemente al tratamiento con inhibidor de PARP. El panorama cambió cuando se empleó la secuencia completa: quimioterapia con platino primero, seguida de mantenimiento con inhibidor de PARP más anti‑PD1. En este contexto, los tumores se redujeron más profundamente y los ratones vivieron más tiempo que con quimioterapia más PARP o anti‑PD1 por separado. Añadir anti‑CTLA4 al mantenimiento con PARP no produjo beneficios similares, lo que sugiere que el microambiente tumoral primado por la quimioterapia está específicamente predispuesto a responder al bloqueo de PD‑1. 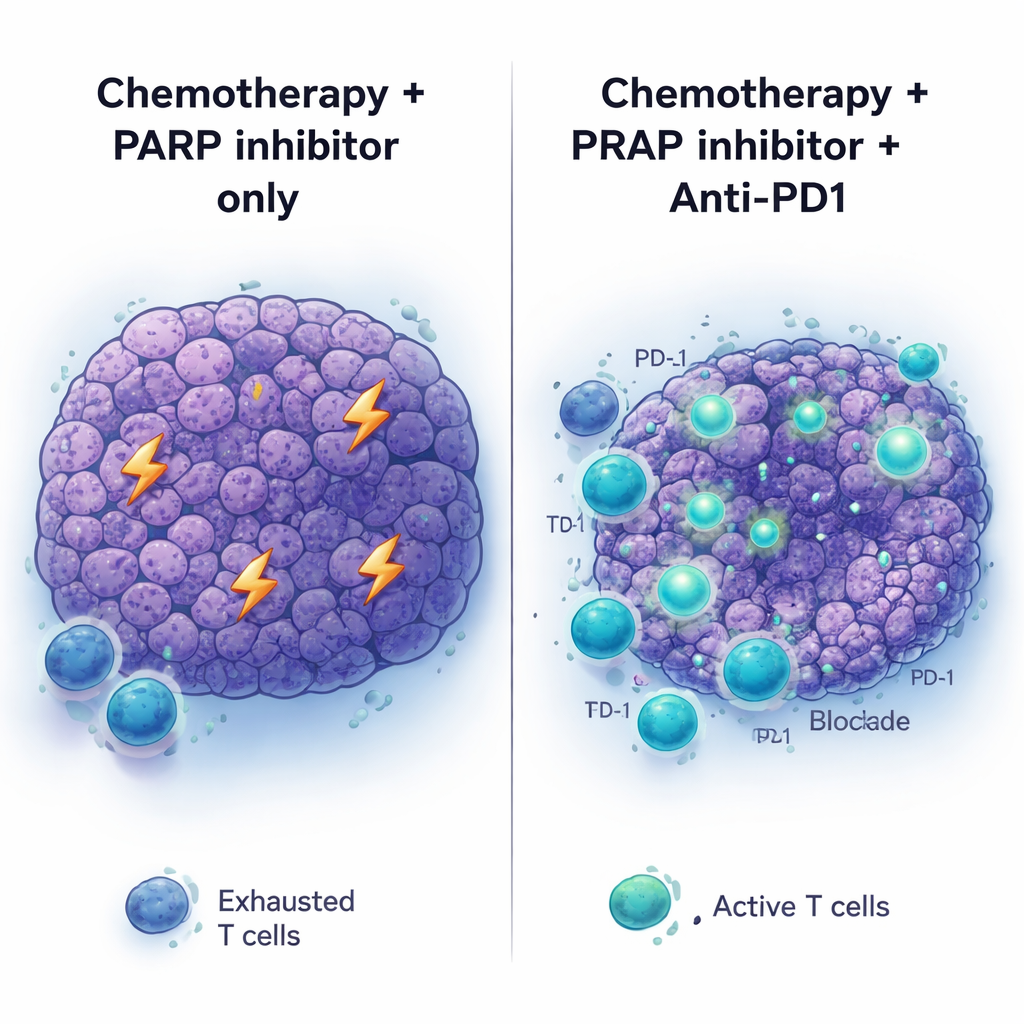
Qué podría significar esto para la atención futura
En conjunto, el estudio sostiene que, en el cáncer pancreático con mutación BRCA, el orden y la combinación de las terapias importan mucho. La quimioterapia fuerte que daña el ADN no solo ataca directamente las células tumorales, sino que también despierta una respuesta inmune, aunque esa respuesta esté inicialmente atenuada por el agotamiento y las defensas mediadas por PD‑L1. Los inhibidores de PARP pueden prolongar ese beneficio pero probablemente no sean curativos por sí solos y pueden empujar a los tumores hacia un estado resistente con altos niveles de CDX2. Superponer la inmunoterapia anti‑PD1 al mantenimiento con PARP tras la quimioterapia con platino podría convertir este paisaje inmune brevemente inflamado y agotado en un ataque antitumoral más eficaz y duradero. Los ensayos clínicos en curso que combinan inhibidores de PARP con inmunoterapia en cáncer pancreático relacionado con BRCA serán clave para determinar si esta estrategia cronometrada puede traducirse en vidas más largas y de mejor calidad para los pacientes.
Cita: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Palabras clave: cáncer de páncreas, mutación BRCA2, quimioterapia con platino, inhibidor de PARP, inmunoterapia PD-1