Clear Sky Science · es
Síntesis eficiente de amidas sin disolventes mediante la reacción de Ritter catalizada por un nanocompuesto reutilizable Fe3O4/g-C3N4/NTMPA
Por qué importa una química más limpia
Muchos de los medicamentos que tomamos, los plásticos que nos rodean e incluso las fibras de alto rendimiento se construyen a partir de un tipo simple de enlace químico llamado enlace amida. Producir estos enlaces a escala industrial suele exigir ácidos fuertes y corrosivos y grandes volúmenes de disolvente, lo que genera residuos y problemas de seguridad. Este artículo describe un nuevo catalizador sólido, sensible a campos magnéticos, que puede formar amidas con altos rendimientos sin usar disolventes, apuntando hacia una fabricación más segura y sostenible de fármacos y materiales.
Un eslabón clave en fármacos y materiales
Las amidas son los enlaces que mantienen unidas a las proteínas y también se encuentran en innumerables fármacos, agroquímicos y polímeros como el nylon. Los químicos disponen de muchas formas de formar enlaces amida, pero la mayoría de los métodos requieren materiales de partida preactivados o condiciones severas. La reacción de Ritter destaca porque une directamente un alcohol (o un alqueno) con una nitrila en un solo paso. Sin embargo, en su forma clásica la reacción de Ritter depende de ácidos minerales concentrados como el sulfúrico o el clorhídrico. Estos ácidos líquidos son corrosivos, difíciles de separar de los productos y complicados de reciclar, por lo que no encajan bien con la química verde.
Un pequeño imán que puedes remover con una barra
Los investigadores diseñaron un catalizador sólido y separable magnéticamente que podría sustituir a esos ácidos líquidos. Su material combina tres componentes: nanopartículas de óxido de hierro (Fe3O4), que proporcionan propiedades magnéticas; un sólido estratificado rico en carbono y nitrógeno (nitruro de carbono grafítico, g‑C3N4), que actúa como soporte protector; y una molécula fuertemente ácida llamada nitrilotri(ácido metilfosfónico) (NTMPA), que aporta la acidez necesaria para la reacción. Estas piezas están ensambladas de modo que NTMPA queda anclada en la superficie del g‑C3N4, mientras pequeñas partículas de Fe3O4 están incrustadas en toda la matriz. Como todo el compuesto responde a un imán, puede extraerse de la mezcla de reacción simplemente colocando un imán fuera del matraz.
Demostrando la estructura del catalizador
Para confirmar que habían construido lo previsto, los autores utilizaron una batería de técnicas de ciencia de materiales. La espectroscopía infrarroja mostró señales de los grupos ácido fosfónico, del entramado carbono‑nitrógeno y de los enlaces hierro–oxígeno, presentes conjuntamente en el compuesto final. La difracción de rayos X indicó que el óxido de hierro magnético mantenía su forma cristalina, mientras que el nitruro de carbono permanecía como un sólido estratificado y algo desordenado. La microscopía electrónica reveló partículas en forma de lámina decoradas con esferas uniformemente dispersas en el rango de 10–20 nanómetros, y el mapeo elemental mostró hierro, carbono, nitrógeno, oxígeno y fósforo distribuidos de manera uniforme. Las mediciones de área superficial y tamaño de poro confirmaron una estructura mesoporosa —llena de canales a escala nanométrica que permiten a los reactivos alcanzar los sitios activos—, mientras que el análisis térmico mostró que el material permanece estable hasta varios cientos de grados Celsius.
Reacciones rápidas sin disolventes
Con la estructura establecida, el equipo probó el catalizador en la reacción de Ritter entre diversos alcoholes y nitrilas. Descubrieron que las mejores condiciones eran sorprendentemente sencillas: cantidades equimolares de alcohol y nitrila, una pequeña dosis del catalizador sólido, calentamiento a 80 °C y sin disolvente añadido. Bajo estas condiciones, muchos sustratos se convirtieron en sus amidas correspondientes con rendimientos altos o excelentes, a menudo superiores al 90 %. Alcoholes terciarios y benzílicos (que forman más fácilmente el intermedio reactivo necesario para la reacción de Ritter) reaccionaron en apenas 1–4 horas, mientras que sustratos más exigentes necesitaron algo más de tiempo. Tanto las nitrilas aromáticas como las alifáticas funcionaron bien, siendo las sustituciones fuertemente atractoras de electrones en nitrilas aromáticas las que aumentaron aún más la eficiencia. En conjunto, el estudio demostró que el catalizador sólido puede igualar o superar a muchos ácidos líquidos, evitando medios corrosivos y disolventes adicionales.
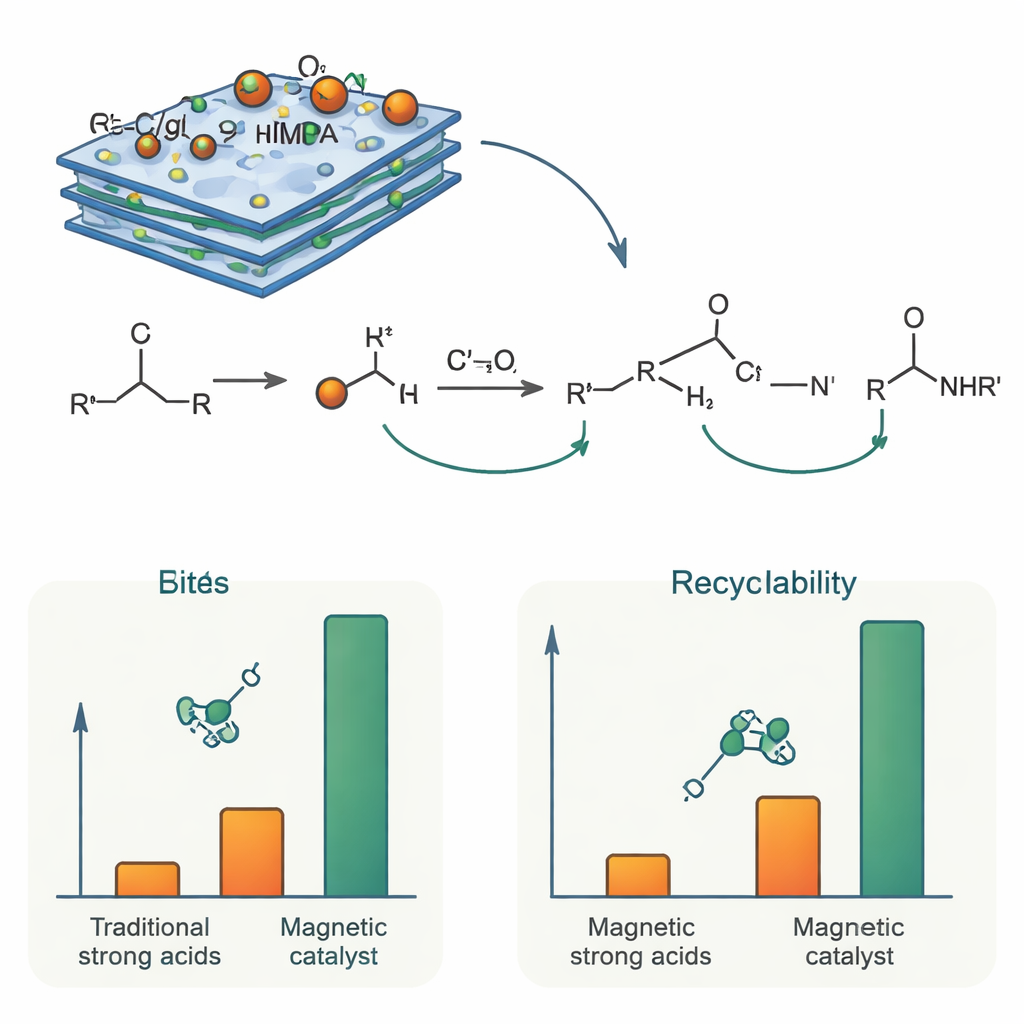
Cómo funciona y por qué perdura
Químicamente, la función del catalizador es protonar brevemente el alcohol y facilitar la pérdida de agua, generando una especie de corta vida con carga positiva. Una molécula de nitrila ataca entonces este intermedio para formar un nuevo enlace carbono–nitrógeno, que finalmente se convierte en amida por reacción con el agua formada en el proceso. Los grupos ácido fosfónico en NTMPA proporcionan una acidez controlada, lo bastante fuerte para impulsar estos pasos pero moderada por la superficie de nitruro de carbono circundante, de modo que se minimizan reacciones secundarias no deseadas. Como las unidades activas de NTMPA están químicamente ancladas al soporte sólido, no se disuelven durante la reacción. Mediciones de magnetización confirmaron que las partículas mantienen una fuerte magnetización, lo que permite retirar rápidamente el catalizador gastado con un imán. En pruebas de reutilización, el mismo lote de catalizador se empleó al menos seis veces con solo una pequeña caída en la actividad, y los análisis estructurales posteriores al uso mostraron que su composición y morfología permanecieron en gran medida sin cambios.
Qué supone esto para una fabricación más verde
Para un lector no especializado, la conclusión clave es que los autores han desarrollado un polvo reutilizable y sensible a campos magnéticos que puede ayudar a los químicos a ensamblar enlaces amida importantes sin depender de ácidos líquidos corrosivos y disolventes adicionales. Este enfoque reduce los residuos, simplifica la purificación del producto y facilita el reciclaje del catalizador, aspectos todos importantes para una química industrial más verde. Aunque el trabajo se centra en un tipo de reacción, los mismos principios de diseño —anclar grupos de ácido fuerte sobre un soporte robusto y magnético— podrían aplicarse a muchas otras transformaciones que sustentan la producción de fármacos y materiales avanzados.
Cita: Karimitabar, H., Sardarian, A.R. Efficient solvent-free amide synthesis via Ritter reaction catalyzed by a reusable Fe3O4/g-C3N4/ NTMPA nanocomposite. Sci Rep 16, 6494 (2026). https://doi.org/10.1038/s41598-026-35371-2
Palabras clave: síntesis de amidas, reacción de Ritter, nanocatalizador magnético</keyword:n> <keyword>química sin disolventes, catálisis verde