Clear Sky Science · es
Alteración de la homeostasis del hierro intracelular por disfunción mitocondrial asociada a la supresión de la expresión de ATP13A2
Por qué importa el hierro dentro de las células cerebrales
La enfermedad de Parkinson es más conocida por los temblores y la rigidez, pero en el interior de las neuronas afectadas se desarrolla otro problema: el hierro, un metal esencial, comienza a acumularse donde no debería. Este estudio plantea una pregunta simple pero importante: ¿cómo ocurre esa acumulación de hierro y cómo podría dañar a las pequeñas plantas de energía y a los centros de reciclaje dentro de las células nerviosas? Al responderla, el trabajo ofrece pistas sobre por qué ciertas regiones cerebrales degeneran en el Parkinson y trastornos relacionados, y apunta hacia nuevos enfoques terapéuticos que van más allá de reemplazar la dopamina.
Una mirada más cercana a una pista genética rara
Los investigadores se centran en una forma hereditaria rara de la enfermedad de Parkinson, llamada PARK9, causada por defectos en un gen denominado ATP13A2. Este gen codifica una proteína localizada en los lisosomas, los compartimentos de la célula encargados del procesamiento y reciclaje de desechos. Las personas con mutaciones en ATP13A2 también pueden desarrollar una condición caracterizada por depósitos de hierro en el cerebro. Ese vínculo convirtió a ATP13A2 en un punto de entrada ideal para estudiar cómo se desregula el equilibrio del hierro. Usando una línea celular humana similar a neuronas que sobreproduce la proteína relacionada con el Parkinson alfa‑sinucleína, el equipo empleó pequeños fragmentos de ARN para reducir ATP13A2 y luego siguió cómo cambiaban el hierro, la producción de energía y la salud celular.
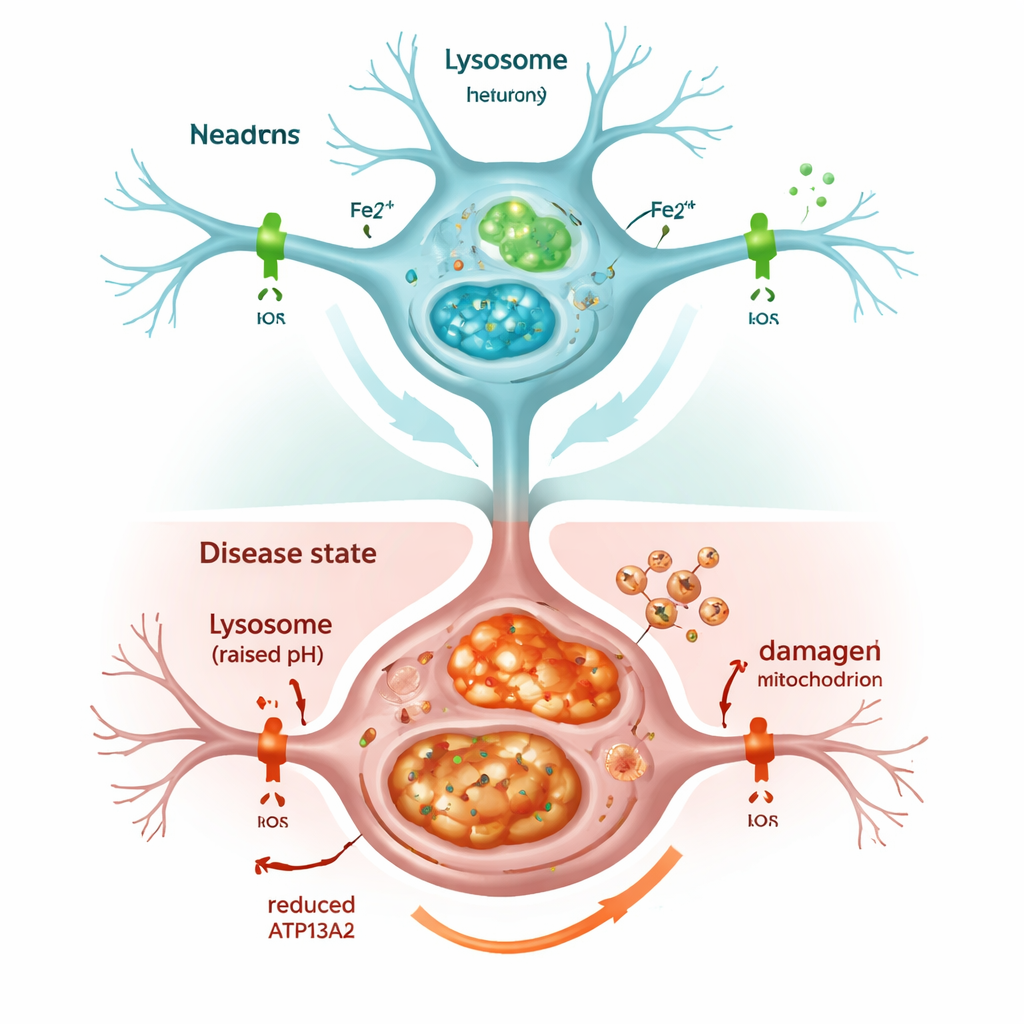
Cuando el sistema de reciclaje celular se atasca
La inhibición de ATP13A2 debilitó rápidamente los lisosomas. Su acidez interna, crítica para degradar material no deseado, disminuyó, y los marcadores del proceso de limpieza celular conocido como autofagia se acumularon en lugar de eliminarse. Como resultado, la alfa‑sinucleína se acumuló, reproduciendo lo observado en cerebros con Parkinson. Las células también mostraron más hierro en general, y especialmente más de la forma químicamente activa, llamada Fe2+, tanto dentro de lisosomas como de mitocondrias. La célula respondió produciendo más ferritina, una proteína que almacena hierro, pero esto no fue suficiente para evitar problemas: las mitocondrias sobrecargadas generaron un exceso de especies reactivas de oxígeno y la supervivencia celular disminuyó. Tratar las células con un fármaco quelante del hierro, similar a algunos usados clínicamente, redujo este estrés oxidativo y rescató parcialmente la viabilidad celular, subrayando que el exceso de hierro fue un conductor clave del daño.
Los sensores de hierro dejan de escuchar al metal
Normalmente, las células cuentan con un sistema de retroalimentación que detecta cuando los niveles de hierro aumentan y responde reduciendo la entrada de hierro. Una proteína llamada IRP2 percibe el hierro, en parte mediante una señal dependiente del hemo procedente de las mitocondrias, y ajusta la producción de proteínas transportadoras de hierro en la superficie celular. En las células deficientes en ATP13A2, esta salvaguarda falló. Los transportadores que introducen hierro en la célula se mantuvieron elevados pese a que el hierro ya estaba aumentado. Los niveles de proteína IRP2 cambiaron apenas, y añadir hierro extra desde el exterior no desencadenó su degradación habitual. El equipo rastreó este fallo hasta las mitocondrias: las mitocondrias dañadas respiraban con menor eficiencia, mostraban signos de control de calidad defectuoso (mitofagia) y, crucialmente, perdieron la capacidad de sintetizar hemo, la molécula que contiene hierro y que ayuda a IRP2 a detectar el hierro. Sin suficiente hemo, IRP2 no recibió el mensaje de “demasiado hierro” y permitió la entrada continuada de hierro.
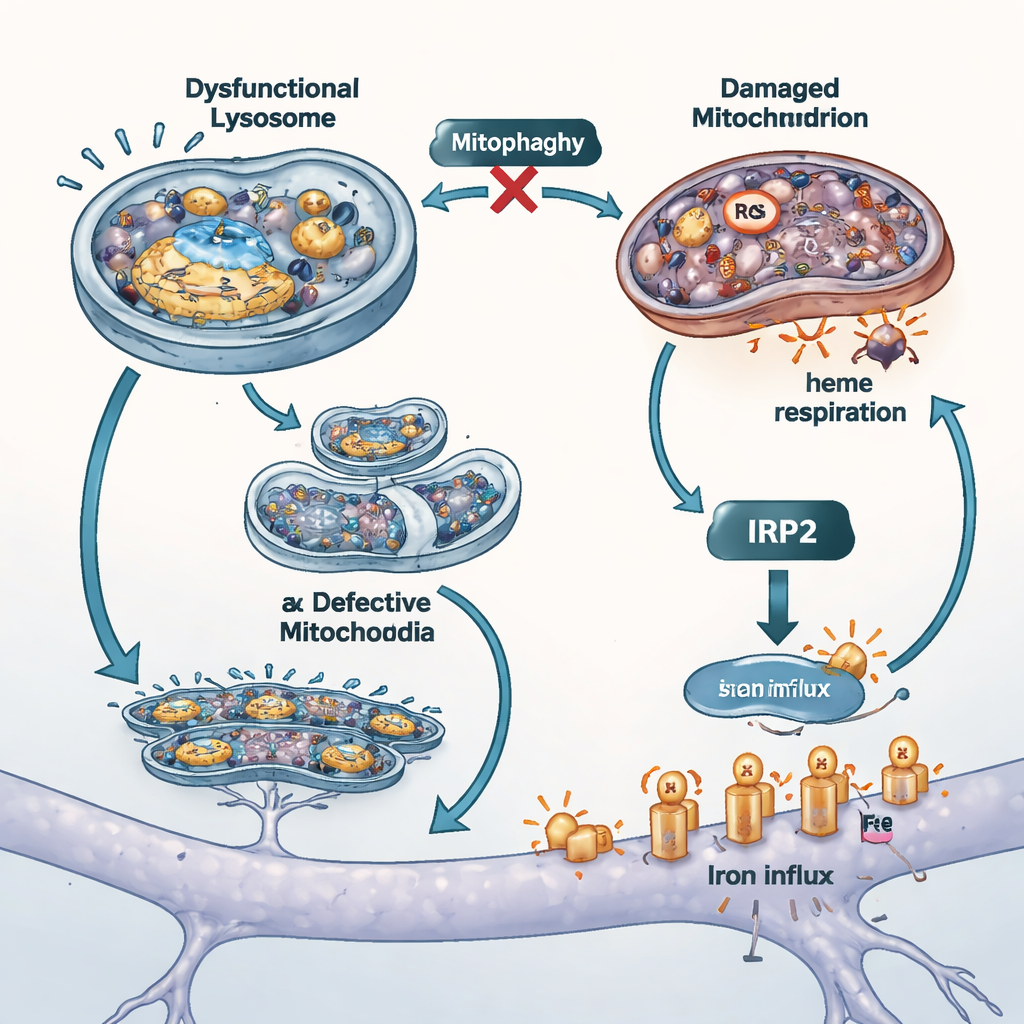
Tapar la llave del hierro y probar otros modelos
Para evaluar cuánto contribuía esta entrada incontrolada de hierro al daño celular, los científicos bloquearon dos rutas principales de captación de hierro. Usaron una versión sin hierro de la proteína plasmática transferrina para competir por un importador, y un fármaco pequeño para atenuar la actividad de otro transportador llamado DMT1. Ambas maniobras redujeron el hierro total y libre dentro de las células, disminuyeron el estrés oxidativo mitocondrial y mejoraron la supervivencia, lo que sugiere que los canales de hierro en la superficie son amplificadores importantes del daño cuando se pierde ATP13A2. Los investigadores también repitieron experimentos clave en células carentes de otro gen vinculado al Parkinson, PINK1, conocido por afectar la mitofagia. Estas células mostraron la misma combinación de acumulación de hierro y debilitamiento de la producción de hemo, apoyando la idea de que el control de calidad mitocondrial y el equilibrio del hierro están fuertemente entrelazados en distintas formas de la enfermedad.
Qué significa esto para el Parkinson y futuros tratamientos
En términos sencillos, el estudio describe un ciclo vicioso. Cuando se suprime ATP13A2, los lisosomas dejan de eliminar componentes dañados, incluidas mitocondrias defectuosas. Esas mitocondrias debilitadas producen menos energía y menos hemo, entorpeciendo el sistema de detección del hierro de la célula. El hierro sigue entrando por los transportadores de la superficie, se acumula en compartimentos vulnerables y alimenta reacciones tóxicas que lesionan aún más a las mitocondrias. Con el tiempo, este círculo puede contribuir a explicar por qué ciertas neuronas mueren en el Parkinson y en otros trastornos cerebrales con carga de hierro. Los hallazgos sugieren que las terapias futuras podrían no solo intentar eliminar el exceso de hierro, sino también restaurar la función lisosomal adecuada, el control de calidad mitocondrial y la producción de hemo: atacar el problema en su origen en lugar de solo limpiar el metal una vez ocurrido el daño.
Cita: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
Palabras clave: Enfermedad de Parkinson, hierro cerebral, mitocondrias, lisosomas, síntesis del hemo