Clear Sky Science · es
Investigación de los residuos funcionales críticos de una enzima mediante el seguimiento en tiempo real de la reacción enzimática usando NMR y enfoques computacionales
Por qué esto importa para los antivirales del futuro
Favipiravir es una pastilla ya usada contra la gripe y ensayada frente a la COVID-19, pero no combate a los virus en la forma que ingerimos. Nuestras propias células deben convertirla primero en una molécula activa que bloquee al virus. Este estudio desmenuza, casi átomo por átomo, cómo una enzima humana realiza un paso crucial de activación y qué pequeñas partes de la enzima actúan como “puntos calientes” que controlan la rapidez y eficacia con que se activa el fármaco. Comprender estos detalles podría orientar el diseño de antivirales de nueva generación que sean tanto más potentes como más predecibles en los pacientes.
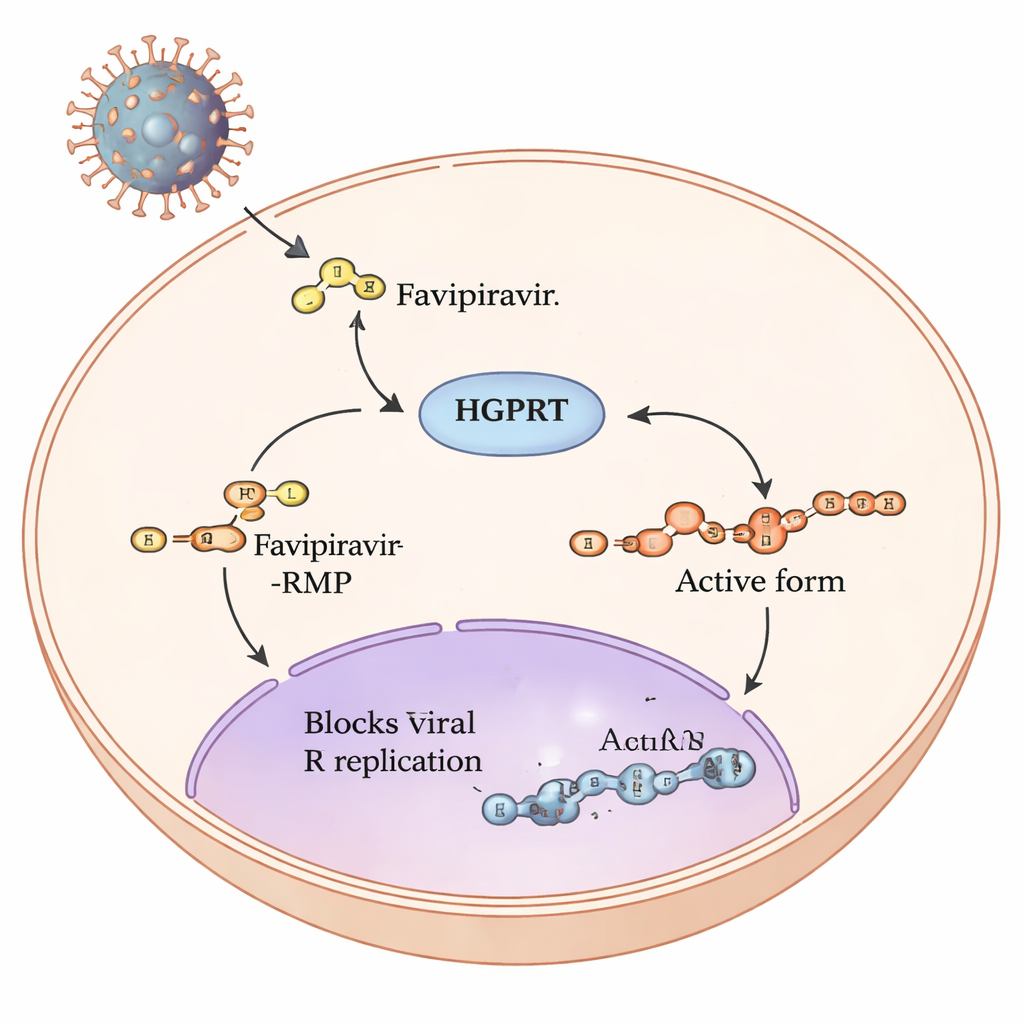
El recorrido de un profármaco dentro de nuestras células
Favipiravir es un llamado profármaco: una vez que entra en las células humanas, una serie de pasos químicos lo reconvierten en una forma capaz de bloquear la maquinaria de copia de virus con genoma de ARN, como la gripe y el SARS-CoV-2. El primer y más lento paso de esta vía lo realiza una enzima humana llamada hipoxantina-guanina fosforibosiltransferasa, o HGPRT. HGPRT añade un pequeño grupo azúcar-fosfato al favipiravir, produciendo favipiravir‑RMP. Solo después de este paso otras enzimas pueden construir la forma triphosfato totalmente activa que interfiere directamente con la ARN polimerasa viral. Dado que este primer paso impulsado por HGPRT actúa como un cuello de botella sobre la cantidad de fármaco activo que se produce, los autores se propusieron identificar qué partes de HGPRT son más importantes para procesar el favipiravir.
Observando la química en tiempo real con NMR
De forma única, el favipiravir contiene un átomo de flúor que se comporta como un pequeño transmisor en un campo magnético. El equipo aprovechó esto usando espectroscopía de resonancia magnética nuclear de flúor-19 (NMR) para observar, en tiempo real, cuánto favipiravir y cuánto favipiravir‑RMP había en un tubo de ensayo a medida que progresaba la reacción. Puesto que solo el fármaco lleva flúor, las señales de NMR son limpias y fáciles de seguir. Al registrar espectros de manera repetida durante 12 horas, los investigadores pudieron seguir la desaparición del fármaco inicial y la aparición del producto modificado, y extraer medidas cinéticas estándar como la velocidad de la reacción y la aparente afinidad con la que la enzima une el fármaco.
Ajustando posiciones clave en la enzima
Tomografías por rayos X previas de HGPRT unido a favipiravir‑RMP habían sugerido un puñado de aminoácidos que acunan el fármaco en un bolsillo. El nuevo trabajo prueba tres de estas posiciones realizando cambios precisos de una sola letra en la proteína y comparando cada enzima mutante con la natural. Un cambio, denominado T138A, hizo inesperadamente que la enzima fuera unas cuatro a seis veces más rápida en convertir el favipiravir, pese a que eliminaba un grupo químico que se pensaba ayudaba a retener el fármaco. Un segundo cambio, K140M, ralentizó moderadamente la reacción y debilitó ligeramente la unión aparente. Un tercer cambio, D193N, abolió por completo la capacidad de la enzima para producir favipiravir‑RMP, aunque la proteína alterada aún podía producirse y unir el producto. En conjunto, estos resultados muestran que no todos los puntos de contacto son iguales: algunos actúan como reguladores sutiles de la velocidad, mientras que otros son interruptores esenciales.
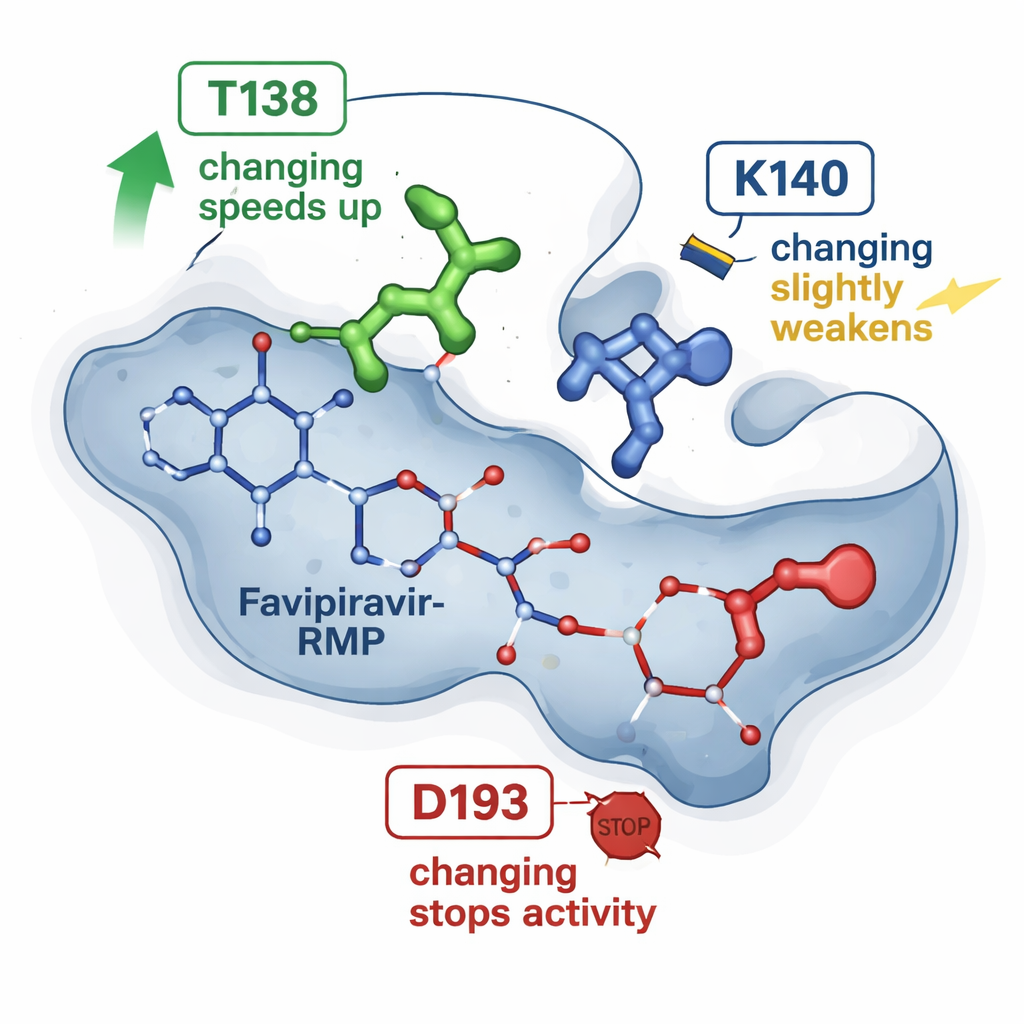
Simulando las partes móviles en un ordenador
Para ver más allá de las estructuras estáticas, los investigadores recurrieron a simulaciones moleculares. Partiendo de la estructura tridimensional conocida de HGPRT con favipiravir‑RMP, utilizaron herramientas computacionales consolidadas para estimar qué tan fuertemente se une el fármaco en cada mutante y para ejecutar muchas simulaciones de dinámica molecular cortas. Estas simulaciones rastrean cómo vibran e interactúan los átomos en decenas de nanosegundos. Los cálculos concordaron con las tendencias derivadas de NMR: la variante T138A tendía a retener favipiravir‑RMP de forma más favorable, pero también mostró episodios en los que el fármaco se movía hacia una vía de “escape”, guiado por otro residuo (K140) que ancla brevemente el grupo fosfato antes de su liberación. En contraste, la variante D193N aún sujetaba el producto, pero probablemente fallaba en un paso catalítico anterior que requiere un ion magnesio, lo que explica por qué perdió actividad a pesar de mantener una unión estable.
Una hoja de ruta para un diseño antiviral más inteligente
Al combinar mediciones NMR en tiempo real con modelos computacionales detallados, este estudio cartografía los puntos calientes funcionales en HGPRT que gobiernan la eficiencia con la que se activa el favipiravir. Para el público general, la conclusión es que nuestras propias enzimas pueden influir de forma notable en la cantidad de fármaco antiviral activo que se acumula dentro de las células, y que modificar ya sea la forma del fármaco o el bolsillo enzimático puede cambiar dramáticamente ese resultado. La estrategia híbrida de los autores ofrece un esquema general para sondear cómo otras medicinas interactúan con sus proteínas diana, lo que podría acelerar el desarrollo de nuevos compuestos antivirales mejor adaptados a la maquinaria de activación del organismo.
Cita: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Palabras clave: favipiravir, activación antiviral, enzima HGPRT, espectroscopía NMR, diseño de fármacos