Clear Sky Science · es
Patrones informados y con conciencia espacial para datos de inmunofluorescencia multiplexada
Por qué importa el vecindario de las células tumorales
El cáncer de páncreas es uno de los más mortales, en parte porque sus tumores se encuentran en un “vecindario” complejo de células inmunitarias y de soporte que pueden tanto combatir al tumor como ayudarlo a ocultarse. Este estudio presenta una nueva forma de leer la disposición espacial de esas células en imágenes microscópicas, revelando cómo se comporta el sistema inmunitario de manera distinta en el adenocarcinoma ductal pancreático (PDAC) —una forma agresiva— frente a su primo precanceroso, el neoplasia papilar mucinosa intraductal (IPMN). Comprender estos patrones ocultos podría señalar mejores diagnósticos y tratamientos más inteligentes y dirigidos.
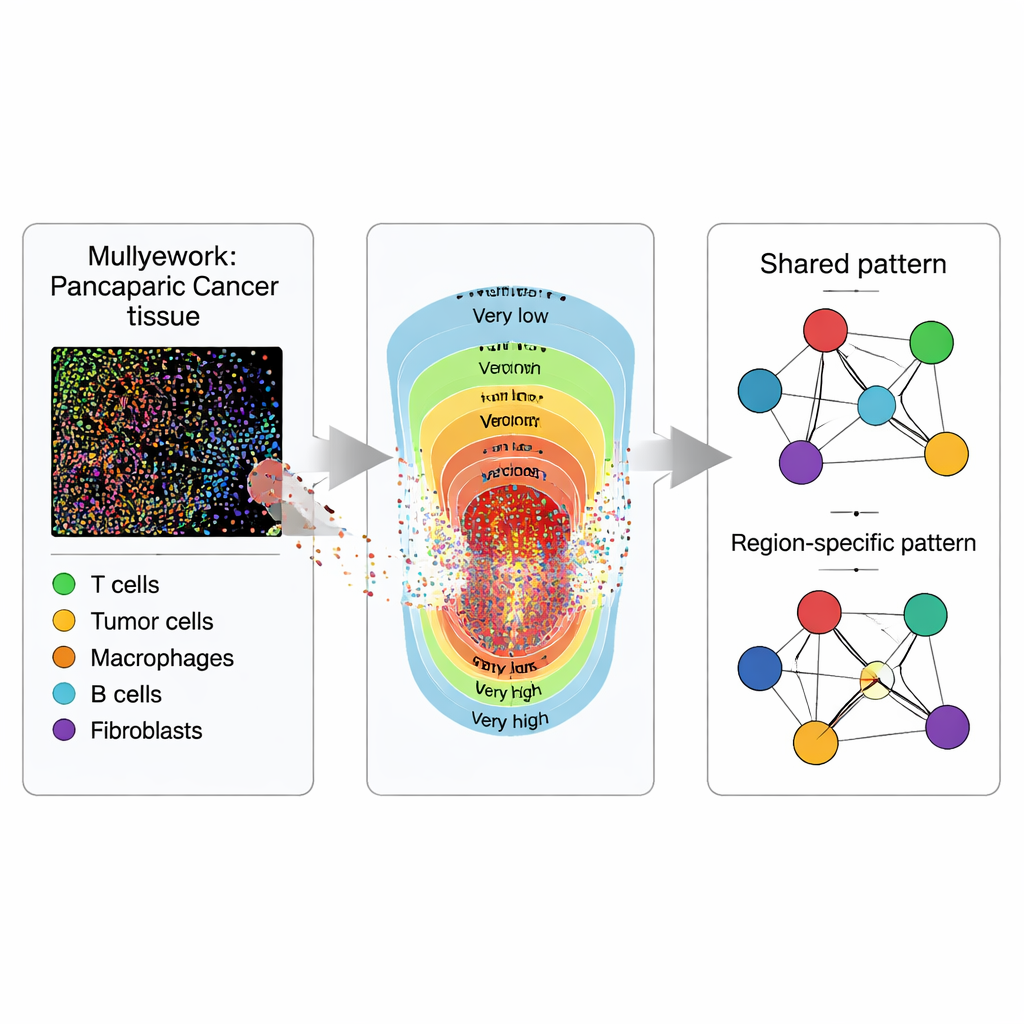
Ver los tejidos como mapas, no solo como imágenes
En lugar de tratar una rebanada tumoral como una imagen plana, los investigadores la consideran como un mapa lleno de puntos. Usando imágenes de inmunofluorescencia multiplexada, tiñen muestras de tejido de 119 pacientes con PDAC y 53 con IPMN para que distintos tipos de células brillen en colores diferentes. Software especializado convierte cada célula visible en un punto con coordenadas y una etiqueta: células tumorales (epiteliales), varias clases de células T que pueden atacar o regular respuestas inmunitarias, y células presentadoras de antígeno que muestran fragmentos tumorales a las células T. La pregunta clave no es solo cuántas de cada célula hay, sino dónde se sitúan unas respecto a otras a lo largo del tejido.
Dividir el tumor en zonas
Para capturar cómo cambian los tumores desde el centro hacia afuera, cada muestra de tejido se divide en cinco zonas según la densidad de células tumorales, desde intensidad tumoral “muy baja” hasta “muy alta”. Estas zonas representan un gradiente de carga tumoral y de hacinamiento celular que los patólogos suelen observar al microscopio pero rara vez cuantifican. Dentro de cada zona, el equipo estima mapas de “intensidad” suavizados para cada tipo celular, esencialmente convirtiendo puntos dispersos en mapas de calor continuos de dónde tiende a agruparse cada tipo celular. Esta zonificación les permite comparar no solo cómo interactúan las células en general, sino cómo esas interacciones cambian de regiones tumorales escasas a densas.
Convertir los vecindarios celulares en redes
A continuación, los investigadores traducen los patrones espaciales a redes, donde cada tipo celular es un nodo y los enlaces representan cuán fuertemente dos tipos celulares tienden a aparecer juntos tras ajustar por los demás. Usando un marco estadístico bayesiano que llaman ISPat (Informed Spatially aware Patterns), separan las características compartidas entre todas las zonas de las que son específicas de una zona. ISPat también puede incorporar conocimiento biológico previo cuando está disponible, ayudando a estabilizar las estimaciones en datos complejos. Experimentos de simulación muestran que ISPat puede recuperar patrones conocidos de forma fiable y lo hace mucho más rápido que métodos tradicionales, lo que lo hace práctico para estudios de imágenes a gran escala.
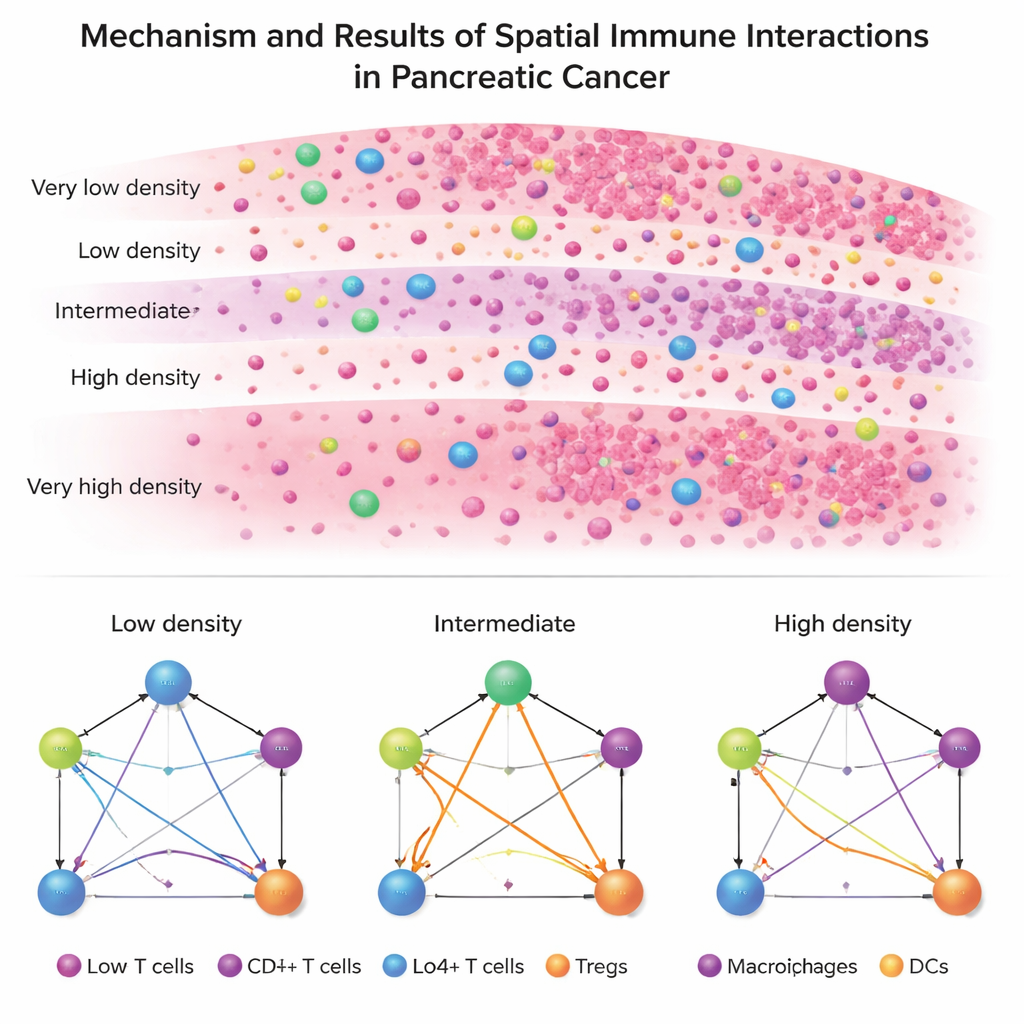
Dos enfermedades, dos arquitecturas inmunitarias
Al aplicar ISPat a datos de pacientes reales surge un contraste llamativo entre PDAC e IPMN. PDAC muestra una arquitectura inmunitaria rígida y uniforme: en casi todas las zonas, las células tumorales, las células T colaboradoras, las células T citotóxicas (asesinas), las células T reguladoras y las células presentadoras de antígeno mantienen prácticamente el mismo patrón de relaciones. Esto sugiere un entorno inmunosupresor estable y arraigado que es difícil de desarticular. En contraste, IPMN presenta mucha más variación zona a zona, especialmente en cómo las células T reguladoras se conectan con otras células inmunitarias. En IPMN, las zonas de densidad intermedia—ni completamente llenas de células tumorales ni casi libres de ellas—muestran la remodelación más drástica de las interacciones inmunitarias.
Puntos calientes para la evasión inmune y la terapia
Profundizando, el estudio identifica pares específicos de tipos celulares cuyas interacciones difieren de forma consistente entre PDAC e IPMN, particularmente en esas zonas de densidad intermedia. Muchas de estas involucran células T reguladoras, que pueden atenuar los ataques inmunitarios, y células presentadoras de antígeno y células T asesinas, que inician y ejecutan respuestas antitumorales. De manera notable, las interacciones que impulsan la presentación de antígenos y la eliminación directa del tumor, así como las que refuerzan la supresión inmune, divergen con más fuerza en estas áreas de gradiente medio, no en las regiones tumorales más extremas. Este patrón sugiere que el campo de batalla crucial para el control inmunitario se encuentra en zonas de transición donde el tumor y el sistema inmunitario aún están negociando activamente.
Qué significa esto para los pacientes
Para un público general, la conclusión es que la ubicación de las células dentro de un tumor importa tanto como qué células están presentes. PDAC parece consolidar un “diseño” inmunosupresor estable, mientras que el paisaje inmunitario de IPMN sigue siendo más flexible y dependiente de la región. Estas huellas espaciales podrían convertirse en biomarcadores para distinguir tumores peligrosos de lesiones precancerosas y para predecir qué pacientes podrían beneficiarse de determinadas inmunoterapias. El marco ISPat ofrece una herramienta general para leer esos códigos espaciales en muchas enfermedades, apoyando un futuro en el que el tratamiento del cáncer esté guiado no solo por la genética y los tipos celulares, sino por la geografía detallada de las células dentro del tumor de cada paciente.
Cita: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Palabras clave: cáncer de páncreas, microambiente tumoral, imágenes espaciales, interacciones inmunitarias, oncología de precisión