Clear Sky Science · es
Un sistema de etiqueta REC sin lisina para aplicaciones de biotinilación por proximidad
Por qué importan las etiquetas pequeñas en las proteínas
Dentro de cada célula, las proteínas rara vez actúan solas: se asocian en sociedades cambiantes que impulsan la salud y la enfermedad. Para estudiar estas asociaciones, los científicos con frecuencia adosan pequeñas “etiquetas de identificación” a las proteínas para poder seguirlas, extraerlas de una mezcla o verlas al microscopio. Un método popular llamado biotinilación por proximidad permite a los investigadores mapear quién está cerca de quién dentro de la célula, pero tiene un problema oculto: muchas de estas etiquetas quedan químicamente modificadas y dejan de ser detectables justo cuando más se necesitan. Este estudio presenta un nuevo tipo de etiqueta, llamada etiqueta REC, diseñada para permanecer visible bajo estas condiciones exigentes.
Un marcador químico para los vecinos proteicos
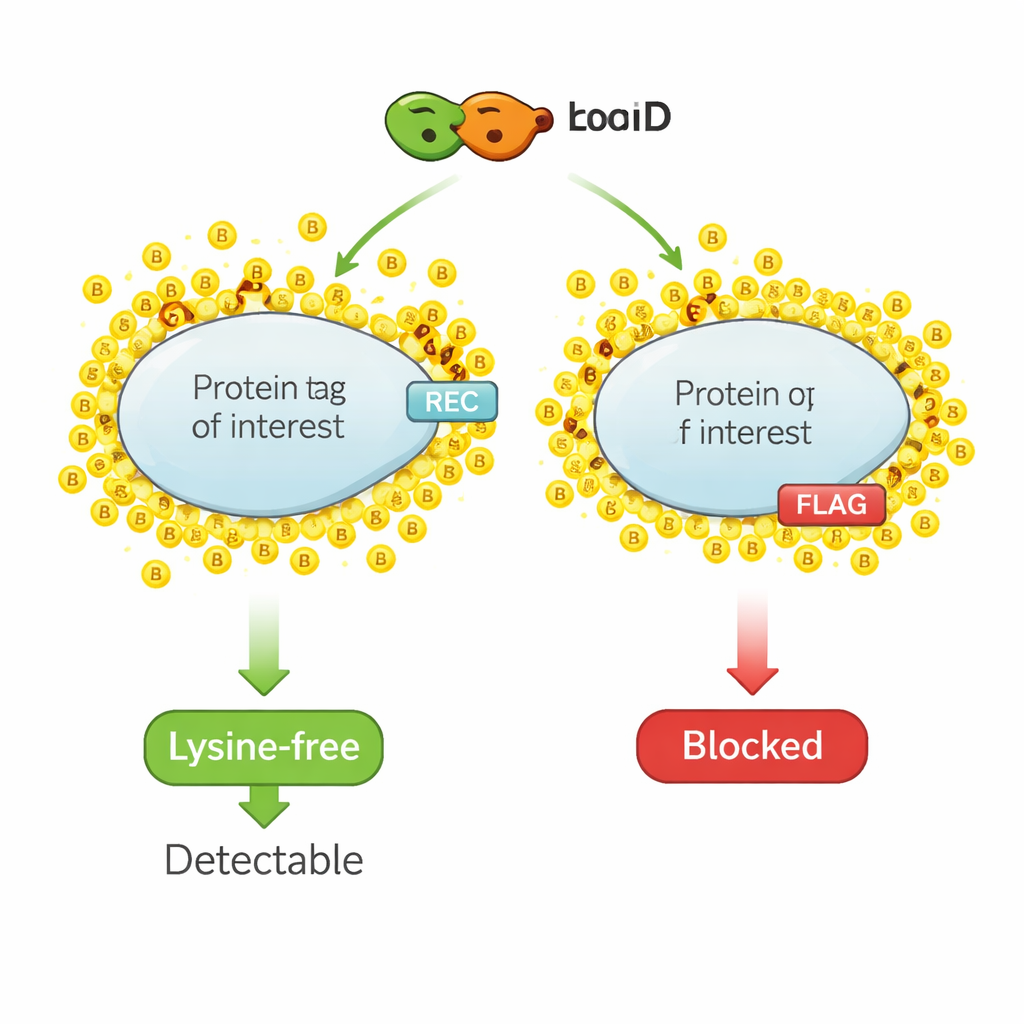
La biotinilación por proximidad funciona como un rotulador molecular. Una enzima diseñada, como TurboID, se fusiona a una proteína de interés. Cuando se añade biotina —una vitamina pequeña— TurboID une rápidamente moléculas de biotina a las proteínas cercanas. Los investigadores luego capturan todas las proteínas marcadas con biotina y las identifican, obteniendo una instantánea del vecindario proteico. Sin embargo, la misma química que etiqueta a las proteínas próximas también ataca las pequeñas etiquetas epítopo que se usan habitualmente para la detección, porque esas etiquetas suelen contener lisina, un aminoácido que es el principal sitio receptor de la biotina. Cuando las lisinas en la etiqueta quedan cubiertas con biotina, los anticuerpos ya no reconocen la etiqueta y la señal en los métodos de detección estándar disminuye o desaparece.
Diseñar una etiqueta que se niegue a modificarse
Para resolver esto, los autores se propusieron crear una nueva etiqueta completamente libre de lisina. Partieron de un fragmento de una proteína del parásito de la malaria llamada PfRipr5, que tiene poca similitud con proteínas humanas, reduciendo el riesgo de reacciones cruzadas indeseadas. Usando un método de cribado en microchips en conejos, generaron 22 anticuerpos monoclonales contra PfRipr5 e identificaron uno, denominado clon n.º 6, con unión especialmente fuerte y específica. Mediante recortes y mutaciones sistemáticas del fragmento PfRipr5, estrecharon el epítopo del anticuerpo hasta una secuencia de 11 aminoácidos. Esta secuencia mínima contenía solo una lisina, que reemplazaron por un aminoácido similar, arginina. De forma notable, el anticuerpo siguió uniéndose igual de bien. Esta secuencia optimizada, sin lisina, fue denominada etiqueta REC, y el anticuerpo emparejado, anticuerpo REC.
Ponemos a prueba la etiqueta REC
El equipo comprobó entonces si la etiqueta REC podía sustituir a etiquetas ampliamente usadas como FLAG en técnicas de laboratorio comunes. Cuando se fusionó a proteínas fluorescentes o de señalización y se produjeron en sistemas libres de células y en células de mamífero, las proteínas con etiqueta REC fueron fácilmente detectadas mediante inmunoblots, un ensayo de placa de alta sensibilidad basado en luz llamado AlphaScreen y mediante inmunotinción en células. La intensidad de la detección fue similar a la de la etiqueta FLAG y a la de otro sistema sin lisina (AGIA), y el anticuerpo REC mostró muy poco ruido de fondo en diversas líneas celulares humanas y de mono. Importa destacar que la etiqueta funcionó tanto si se colocó al inicio como al final de la proteína, y en proteínas localizadas en distintas regiones celulares, incluyendo el núcleo, las mitocondrias, el retículo endoplásmico y la membrana celular.
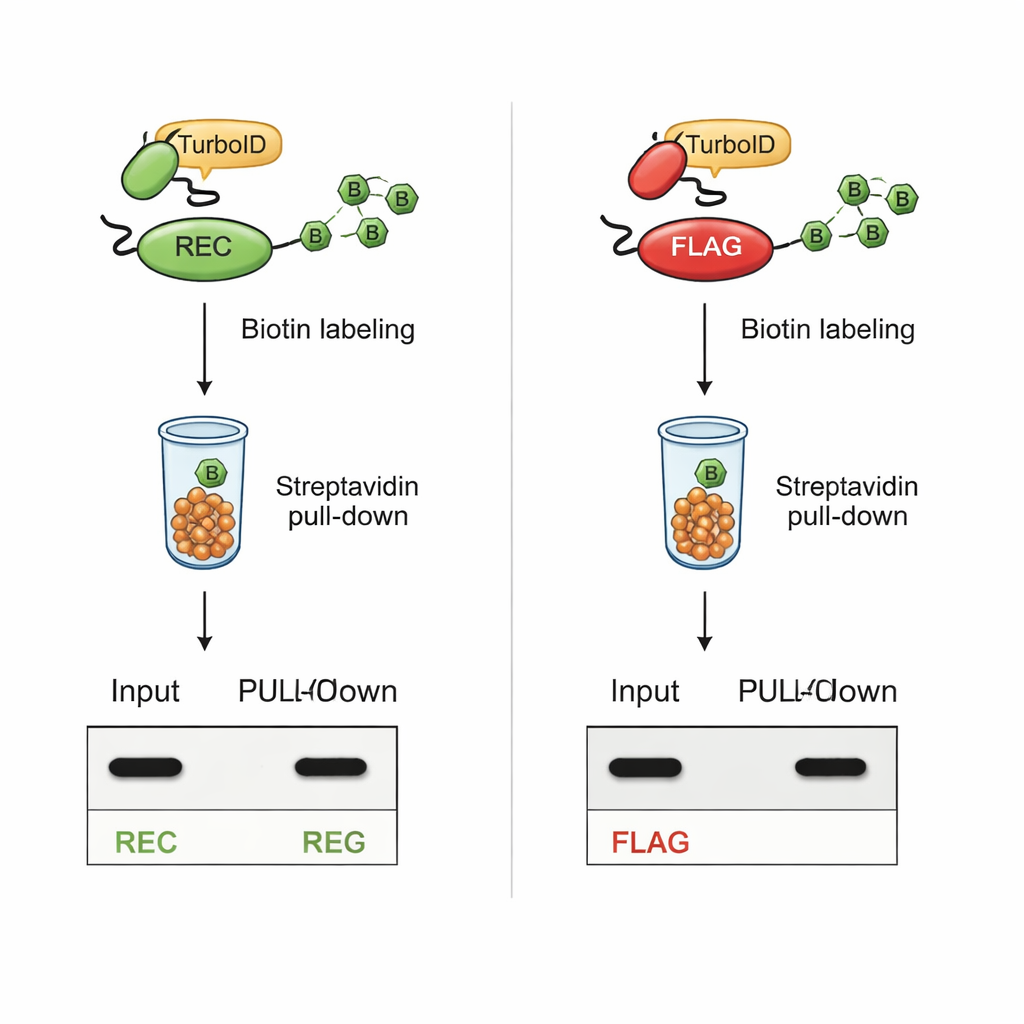
Permanecer visible durante un marcado intenso
La prueba crítica fue si REC seguiría siendo detectable tras la biotinilación mediada por TurboID. En células donde TurboID estaba fusionado a socios de interacción conocidos, las proteínas con la etiqueta REC siguieron claramente visibles tanto en extractos totales de la célula como en la fracción purificada marcada con biotina. En contraste, las proteínas con la clásica etiqueta FLAG perdieron su señal FLAG una vez que TurboID estaba activo, aunque las proteínas en sí seguían presentes. Experimentos adicionales con péptidos sintéticos mostraron que TurboID biotinila directamente las lisinas de la secuencia FLAG, bloqueando físicamente el acceso del anticuerpo. La etiqueta REC, al carecer por completo de lisina, quedó intacta frente a TurboID y siguió siendo fácil de detectar.
Qué significa esto para experimentos futuros
Para los investigadores que exploran redes proteicas dentro de células vivas, la etiqueta REC ofrece una herramienta práctica: se comporta como las etiquetas familiares en los ensayos cotidianos pero continúa funcionando incluso cuando enzimas potentes de marcado por proximidad están activas. Esto permite a los científicos confirmar con mayor fiabilidad que sus proteínas etiquetadas están presentes y han sido capturadas correctamente, y estudiar otras modificaciones basadas en lisina —como la ubiquitinación y la acetilación— sin que la propia etiqueta interfiera. En resumen, REC es un pequeño cambio de diseño con un gran impacto, que ayuda a que los experimentos complejos de cartografía proteica sean más claros y fiables.
Cita: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Palabras clave: marcado de proteínas, biotinilación por proximidad, TurboID, interacciones proteicas, epítopos