Clear Sky Science · es
Interacción entre la metilación del ADN de ELMO1 y Med31 promueve la EMT y la metaplasia intestinal inducidas por H. pylori en el cáncer gástrico mediante polarización M2
Por qué las bacterias del estómago importan para el riesgo de cáncer
La mayoría de nosotros albergamos miles de millones de bacterias en el tracto digestivo, y una de ellas —Helicobacter pylori— puede vivir de forma silenciosa en el estómago durante décadas. Para algunas personas esta infección es inocua, pero para otras se convierte en el primer paso hacia el cáncer gástrico, uno de los cánceres más letales del mundo. Este estudio explora cómo un pequeño cambio químico en el ADN de las células gástricas ayuda a transformar una infección prolongada en un daño precanceroso y, finalmente, en un entorno donde el cáncer puede desarrollarse.
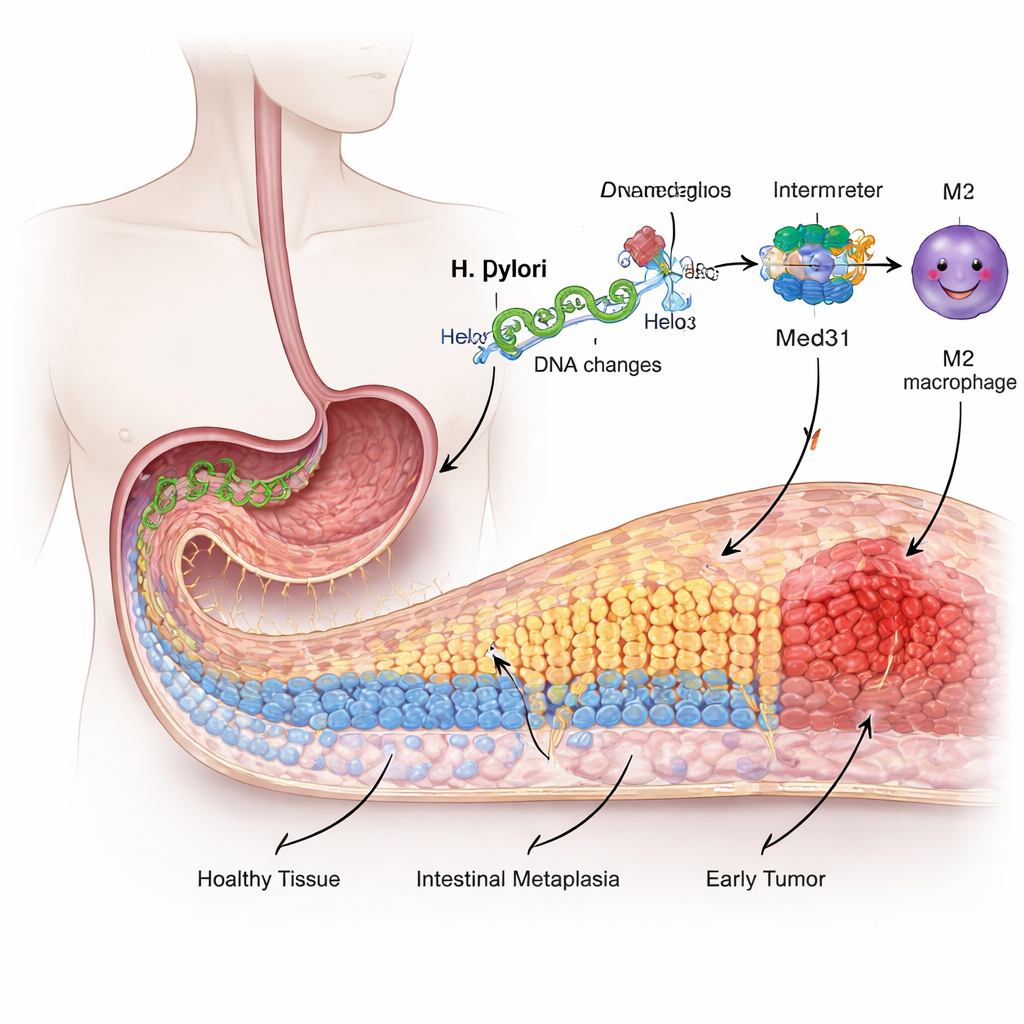
De un revestimiento amigable a un cambio arriesgado
La superficie interna del estómago está recubierta por células especializadas adaptadas a manejar el ácido fuerte, no la digestión de los alimentos como ocurre en el intestino. Tras años de irritación e inflamación por H. pylori, algunas de estas células gástricas comienzan a “redecorarse”, adoptando rasgos de las células intestinales en un proceso llamado metaplasia intestinal. Este cambio se considera una etapa precancerosa. Los investigadores usaron una línea celular gástrica humana para imitar la infección y encontraron que la exposición a H. pylori hacía que estas células crecieran más rápido, se desplazaran con mayor facilidad y activaran marcadores de tipo intestinal, señales que indican que el revestimiento está perdiendo su identidad normal.
Pequeñas etiquetas químicas con grandes consecuencias
Nuestro ADN puede ser marcado con diminutas etiquetas químicas llamadas grupos metilo que actúan como interruptores de encendido y apagado para los genes sin alterar el código genético en sí. El equipo se centró en un gen llamado ELMO1, ya conocido por participar en el movimiento celular y la diseminación tumoral. Demostraron que la infección por H. pylori aumentaba la metilación del gen ELMO1 y, de forma algo contraintuitiva, incrementaba su actividad y los niveles de su proteína en las células gástricas. Cuando usaron un fármaco que elimina estas etiquetas metilo, las células perdieron muchos de los cambios inducidos por la infección: se dividieron menos, se movieron menos y mostraron menos señales de metaplasia intestinal. Esto señaló a la metilación de ELMO1 como un interruptor crucial activado por la bacteria.
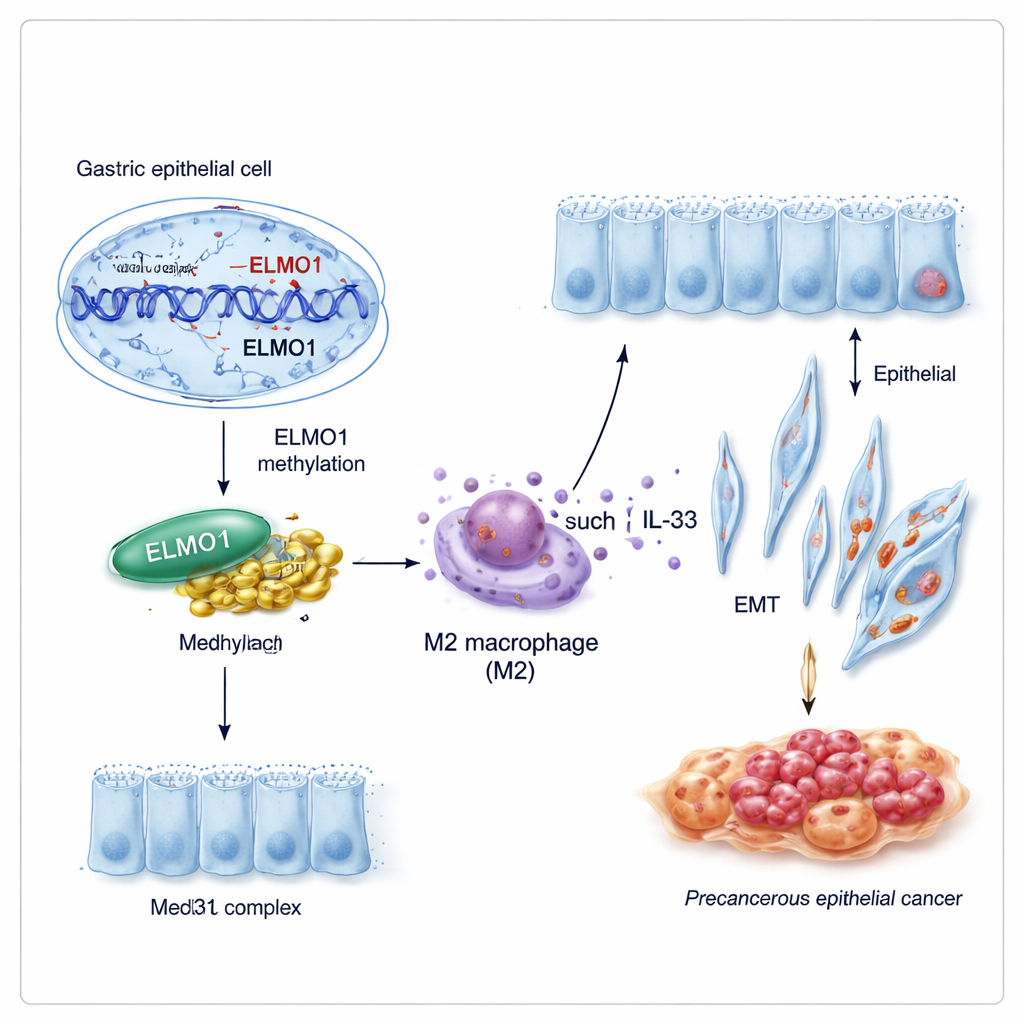
Una nueva asociación que reconecta el comportamiento celular
Los genes rara vez actúan de forma aislada. Los investigadores descubrieron que ELMO1 metilado favorece una asociación con otra proteína, Med31, parte de una gran “placa de control” que ayuda a decidir qué genes activa una célula. Bajo condiciones que promueven la metilación del ADN, los niveles de ELMO1 aumentaron, Med31 también se incrementó y ambos se unieron físicamente, mientras que una pareja previamente conocida de ELMO1, DOCK10, quedó relegada. Este nuevo equipo ELMO1–Med31 parece reprogramar la expresión génica de las células gástricas de maneras que las empujan a adoptar características intestinales y a comportarse de forma más agresiva.
Cómo las células inmunes son empujadas a ayudar al tumor
El cáncer no se desarrolla de forma aislada; crece dentro de un vecindario complejo de células inmunes y de apoyo. El estudio muestra que las células gástricas infectadas con ELMO1 metilado liberan mayores niveles de IL‑33, una señal que empuja a las células inmunes cercanas llamadas macrófagos hacia un estado “M2” favorable al tumor. Usando un sistema de cocultivo, los autores encontraron que los macrófagos expuestos a estas señales se inclinaron fuertemente hacia el tipo M2 y, a su vez, secretaron factores que empujaron a nuevas células gástricas a volverse más móviles, más invasivas y más parecidas a células intestinales. Los marcadores de transición epitelio‑mesénquima —cuando las células epiteliales estacionarias se transforman en células capaces de moverse e invadir— aumentaron notablemente bajo la influencia de estos macrófagos M2.
Qué significa esto para prevenir el cáncer de estómago
En conjunto, el trabajo traza una cadena de acontecimientos: la infección por H. pylori altera la metilación del ADN de ELMO1, este ELMO1 modificado se asocia con Med31, las células infectadas envían señales que convierten a las células inmunes cercanas en ayudantes M2, y estos ayudantes impulsan tanto la metaplasia intestinal como un estado celular más invasivo. Para quienes no son especialistas, la idea clave es que una bacteria común del estómago puede remodelar tanto el revestimiento gástrico como la respuesta inmune local mediante marcas químicas reversibles en el ADN. Comprender esta vía puede abrir la puerta a nuevos análisis basados en sangre que detecten temprano patrones de metilación riesgosos, así como a fármacos que interrumpan el eje ELMO1–Med31–M2 antes de que una infección crónica progrese a cáncer gástrico.
Cita: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Palabras clave: cáncer gástrico, Helicobacter pylori, metilación del ADN, metaplasia intestinal, microambiente tumoral