Clear Sky Science · es
Modelización y verificación experimental de la precipitación de nanopartículas de policaprolactona
Por qué importan las esferas plásticas diminutas en medicina
Imagine encapsular un fármaco potente dentro de una mota tan pequeña que puede deslizarse por los vasos sanguíneos y liberar su carga exactamente donde se necesita. Esas motas, llamadas nanopartículas poliméricas, están en el centro de muchos tratamientos e instrumentos de imagen emergentes. Pero fabricarlas con un tamaño correcto y reproducible resulta sorprendentemente difícil. Este estudio muestra cómo un modelo informático sencillo basado en la física puede predecir y ajustar el tamaño de una nanopartícula biodegradable de uso frecuente, acortando potencialmente años de ensayo y error en el desarrollo de nuevas nanomedicinas.
De mezclar en la cocina a la precisión de laboratorio
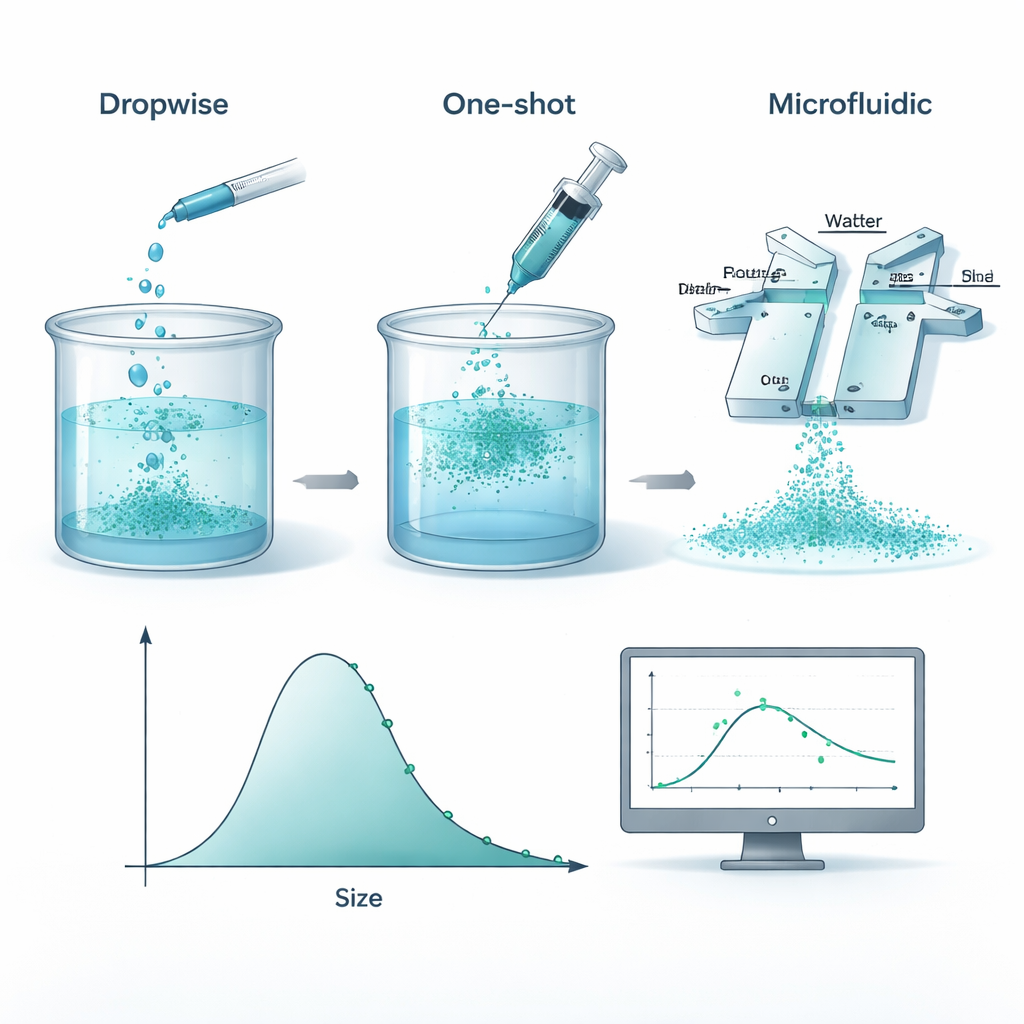
Para crear estas nanopartículas, los investigadores disuelven un plástico biodegradable llamado policaprolactona (PCL) en un solvente orgánico y luego lo mezclan con agua de modo que el polímero «caiga» fuera de la solución y forme pequeñas esferas. El equipo comparó tres maneras prácticas de hacerlo: añadir lentamente la solución polimérica gota a gota, verterla de golpe y hacer confluir ambos líquidos a través de un pequeño chip microfluídico donde se encuentran en canales estrechos. En condiciones cuidadosamente controladas, los tres enfoques produjeron partículas con tamaños medios y dispersiones de tamaño muy similares. Esto significa que, al menos en los rangos estudiados, importa más lo que se pone en la mezcla—cantidades de polímero y estabilizante—que el dispositivo exacto de mezcla.
Cómo la viscosidad y las moléculas auxiliares moldean las partículas
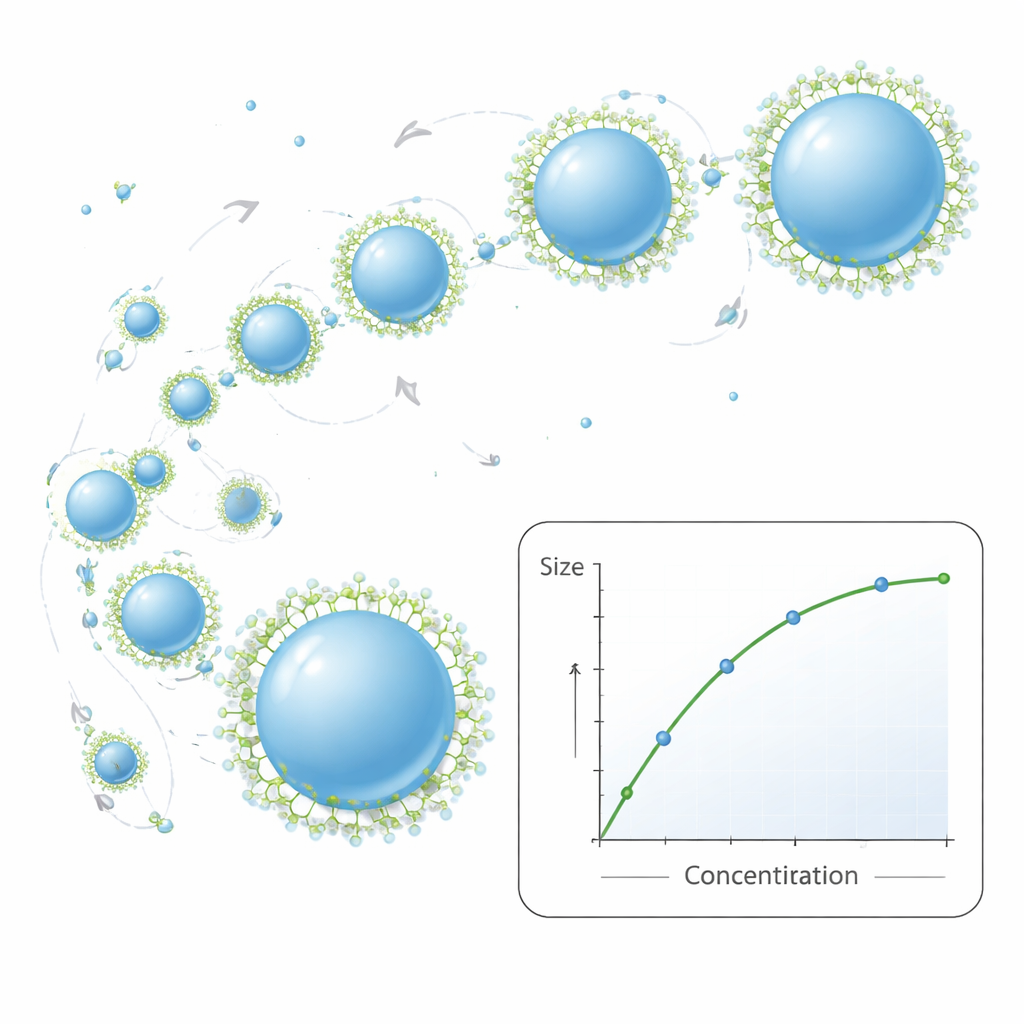
Los autores exploraron luego cómo los ingredientes de la receta controlan el tamaño final de las partículas. Aumentar la cantidad de PCL en la fase orgánica hace que ese líquido sea más espeso, o más viscoso. Piense en intentar mezclar un jarabe en agua en lugar de jugo: un jarabe más espeso se fragmenta en gotitas más grandes. Aquí, las soluciones poliméricas más viscosas dieron lugar a nanopartículas mayores y con distribuciones de tamaño algo más amplias. Añadir un segundo solvente, etanol, ayudó a mantener el proceso estable incluso a niveles poliméricos muy altos, pero a costa de producir partículas mayores en el rango de concentración superior. Un segundo componente, un tensioactivo llamado Pluronic F-127, actúa como agente anticonglomerante molecular. A bajos niveles de tensioactivo, las partículas tienden a chocar y adherirse, creciendo y volviéndose menos uniformes. Al aumentar la concentración de tensioactivo, este recubre las superficies de las partículas, evita que se fusionen y produce nanopartículas más pequeñas y estables—hasta cierto punto, más allá del cual las mejoras son modestas y la distribución de tamaños puede volverse más heterogénea.
Una regla simple de crecimiento que concuerda con la realidad
En el núcleo del trabajo hay un modelo matemático compacto que describe cómo crecen las nanopartículas después de su aparición inicial. Trata su movimiento como un vaivén aleatorio en el líquido, donde las colisiones a veces conducen a que dos partículas se fusionen en una de mayor tamaño. Modelos anteriores asumían que siempre que las partículas se encontraban se fusionaban instantáneamente y formaban esferas perfectas. El modelo nuevo añade dos matices realistas: primero, permite un tiempo finito para que dos partículas en contacto se relajen de una forma alargada a una única esfera; segundo, deja que las moléculas de tensioactivo vayan «bloqueando» gradualmente la superficie, ralentizando o deteniendo más fusiones. Con solo unas pocas entradas medibles—como temperatura, viscosidad del líquido y concentración inicial de polímero—el modelo predice cómo el tamaño medio de las partículas debe cambiar según las condiciones de la formulación. A lo largo de muchos experimentos, los tamaños predichos coincidieron estrechamente con los medidos por dispersión de luz, captando también las tendencias generales en la anchura de la distribución de tamaños.
Usar el modelo como herramienta de diseño
Para comprobar si este enfoque es realmente útil, el equipo invirtió el problema: en lugar de pedir al modelo que explicara datos previos, le pidieron que sugiriera formulaciones que deberían dar tres tamaños y grados de uniformidad específicos. A continuación prepararon estas formulaciones «diseñadas» en el laboratorio. Los diámetros medidos de las partículas difirieron de los objetivos solo entre un 1 y un 7 por ciento—muy dentro de la variación experimental típica—demostrando que el modelo puede orientar con fiabilidad las elecciones de formulación. Las predicciones sobre lo estrecha o amplia que sería la distribución de tamaños fueron menos exactas, pero suficientes para distinguir poblaciones relativamente uniformes de otras más dispersas. En comparación con métodos de simulación pesados que siguen cada molécula o cada remolino del flujo, este modelo simplificado se ejecuta rápidamente en ordenadores modestos y es fácil de adaptar a otros polímeros y configuraciones de procesamiento.
Qué significa esto para la nanomedicina futura
Para los no especialistas, el mensaje clave es que fabricar nanopartículas útiles ya no tiene por qué depender únicamente del minucioso ensayo y error en el laboratorio. Al capturar la física esencial de cómo pequeñas gotas plásticas se mueven, colisionan y son protegidas por tensioactivos, este trabajo ofrece un «mapa» práctico que conecta las decisiones de formulación—cuánto polímero, qué mezcla de solventes, cuánto estabilizante—con el tamaño final de las partículas. Dado que la PCL es un material biodegradable común en liberación de fármacos, implantes y agentes de imagen, este modelo podría ayudar a los investigadores a diseñar nanomedicinas más seguras y eficaces con mayor rapidez y menos material desperdiciado. Los mismos principios pueden extenderse a otros polímeros, aportando mayor predictibilidad y eficiencia al mundo de las terapias a escala nanométrica.
Cita: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Palabras clave: nanopartículas poliméricas, nanoprecipitación, liberación de fármacos, modelado numérico, policaprolactona