Clear Sky Science · es
La nicorandil atenúa el dolor neuropático e inflamatorio mediante TNF-α, IL6/MAPK ERK1/2 y la señalización NO/cGMP
Por qué aliviar el dolor nervioso importa
Millones de personas conviven con un dolor ardiente, lancinante o con hormigueo que persiste mucho después de que la lesión se ha curado. Este dolor “neuropático” puede ser obstinadamente resistente a los analgésicos comunes y a menudo va acompañado de efectos secundarios por el uso prolongado de medicamentos. El estudio resumido aquí explora si la nicorandil —un fármaco cardiaco ya administrado a pacientes con angina— podría también calmar las vías del dolor sobreactivadas en el sistema nervioso y cómo lo hace a nivel celular.
Un medicamento cardíaco entra en la investigación del dolor
La nicorandil se prescribe de forma rutinaria para tratar la angina porque relaja los vasos sanguíneos. Lo logra mediante dos acciones principales: dona pequeñas cantidades de óxido nítrico, una molécula mensajera, y abre ciertos canales de potasio en las células. Trabajos previos en animales insinuaron que la nicorandil también puede disminuir el dolor al actuar sobre receptores nerviosos implicados en sensaciones de calor y picante, y al implicar el propio sistema opioide del organismo. En el presente estudio, los investigadores se propusieron mapear qué ocurre aguas abajo de estos efectos iniciales, centrándose en la inflamación, el estrés oxidativo (una especie de “oxidación” química) y rutas concretas de señalización dentro de las neuronas sensoriales.
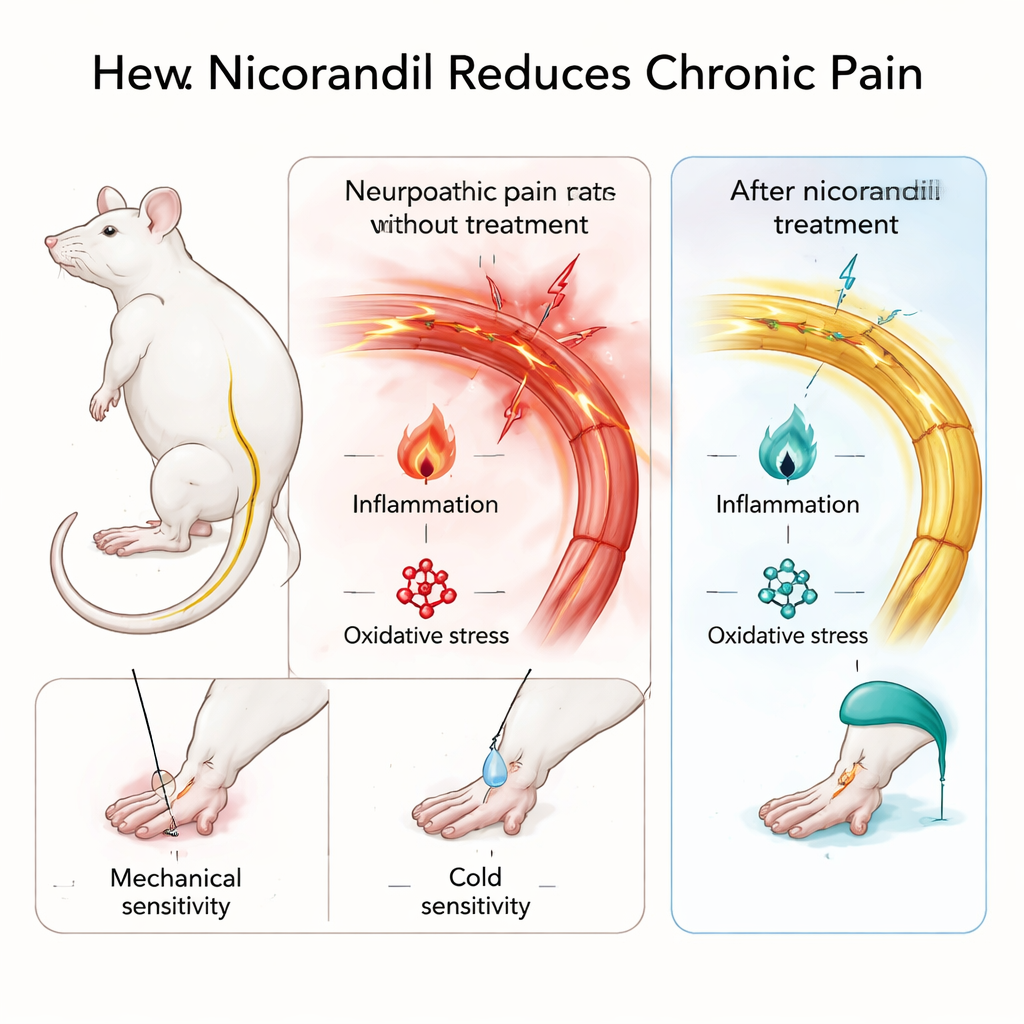
Probando la nicorandil en modelos de dolor persistente
Para imitar el dolor nervioso de larga duración, el equipo ató ligeramente el nervio ciático de ratas, un procedimiento clásico que produce hipersensibilidad al tacto y al frío similar al dolor neuropático humano. También usaron la prueba de formalina, en la que se inyecta un irritante químico leve en una pata para generar un dolor inflamatorio bien definido y prolongado. Las ratas recibieron nicorandil por vía oral en dos dosis, y los científicos midieron la respuesta al tacto ligero y al frío en la pata lesionada, así como cuánto se lamían o estremecían tras la formalina. Es importante que la nicorandil no provocó somnolencia ni falta de equilibrio en una prueba de campo abierto, lo que sugiere que la reducción del comportamiento relacionado con el dolor no se debió simplemente a sedación.
Reduciendo las “señales de alarma” químicas
La nicorandil redujo claramente tanto el dolor inducido por la lesión nerviosa como el dolor provocado por la formalina. Las ratas tratadas toleraron mejor el tacto y el frío y mostraron menos estremecimientos y tiempos de lamido más cortos. Los análisis de sangre revelaron que la nicorandil disminuyó los niveles de potentes mensajeros inflamatorios —factor de necrosis tumoral alfa (TNF-α) e interleucina-6 (IL-6)— así como de ciclooxigenasa‑2, una enzima que contribuye a la producción de prostaglandinas relacionadas con el dolor. También redujo la malondialdehído, un marcador de estrés oxidativo, lo que indica menos daño químico a las membranas celulares. Al microscopio, los nervios de los animales tratados con nicorandil se veían más sanos: hubo menos daño estructural e hinchazón en el nervio ciático y en el agrupamiento de neuronas sensoriales conocido como ganglio de la raíz dorsal.
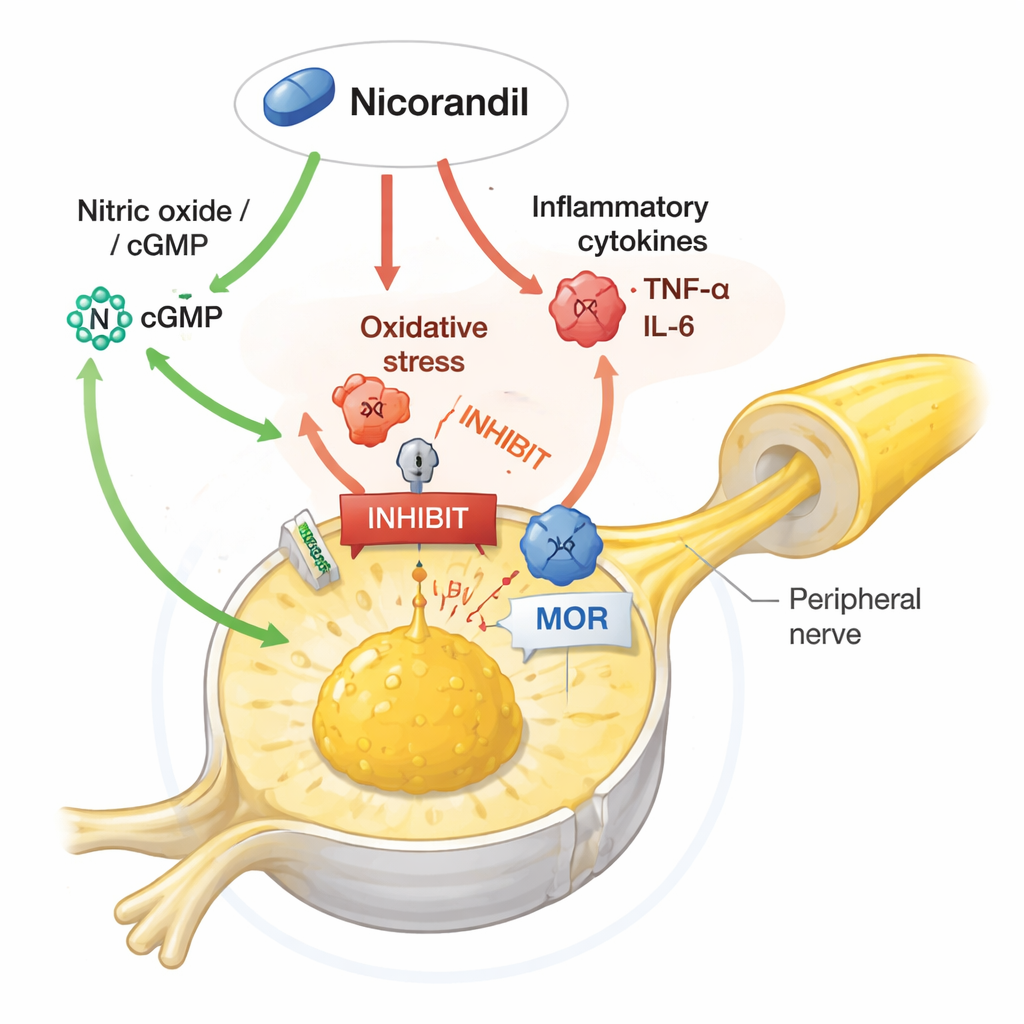
Desenredando la red de señalización dentro de las neuronas del dolor
El estudio avanzó indagando qué vías moleculares eran necesarias para los beneficios de la nicorandil. Cuando los investigadores administraron fármacos que potenciaron el óxido nítrico o aumentaron el GMP cíclico (una molécula mensajera vinculada al NO), atenuaron en parte la capacidad de la nicorandil para reducir el dolor y normalizar proteínas clave. La nicorandil impidió el aumento habitual de ERK1/2, un miembro de la familia MAP quinasa que amplifica las señales dolorosas, y redujo los niveles de TRPV1, un canal que vuelve a las neuronas más sensibles al calor y a irritantes químicos. Potenciar la señalización del óxido nítrico o del GMPc revirtió estos cambios protectores, mientras que bloquear las enzimas que producen óxido nítrico a veces reforzó el alivio del dolor por nicorandil. Sorprendentemente, bloquear los canales de potasio que caracterizan la acción clásica de la nicorandil no abolió sus efectos antinociceptivos, lo que sugiere que, en este contexto, su poder analgésico depende más de modular el óxido nítrico, el estrés oxidativo, la inflamación y la señalización relacionada con los opioides que de su acción vascular clásica.
Qué podría significar esto para las personas con dolor
En conjunto, los hallazgos presentan a la nicorandil como un modulador del dolor con múltiples objetivos: calma las vías nerviosas sobreactivas al reducir el daño oxidativo y los mensajeros inflamatorios, silenciar ERK1/2 y TRPV1 dentro de las neuronas sensoriales e interactuar con el óxido nítrico y el propio sistema opioide del organismo. Aunque estos resultados provienen de modelos en ratas y de dosis a corto plazo, sugieren que un medicamento ya en uso clínico para enfermedades cardíacas podría algún día reutilizarse o adaptarse para ayudar a tratar dolores neuropáticos e inflamatorios difíciles de manejar. Serán necesarios estudios futuros en personas para determinar dosis seguras, efectos a largo plazo y si los mismos mecanismos protectores operan en los nervios humanos.
Cita: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Palabras clave: dolor neuropático, nicorandil, inflamación, estrés oxidativo, señalización del óxido nítrico