Clear Sky Science · es
La alteración de la homeostasis del zinc reduce los niveles de acetilación de histonas en células normales y tumorales
Cuando un metal útil se vuelve dañino
El zinc es más conocido como el nutriente en los multivitamínicos que ayuda a nuestro sistema inmunitario y a la cicatrización. Pero dentro de las células, el zinc debe mantenerse en un rango muy estrecho de “punto justo”. Este estudio muestra que cuando los niveles de zinc en las células se elevan demasiado, pueden silenciar silenciosamente genes importantes al compactar la forma en que se empaqueta el ADN e incluso impulsar a las células hacia un proceso de autolimpieza llamado autofagia. Dado que los suplementos de zinc, los ingredientes anticaspa y fármacos experimentales contra el cáncer pueden alterar los niveles de zinc, entender este sistema de control oculto importa tanto para la salud cotidiana como para futuras terapias.
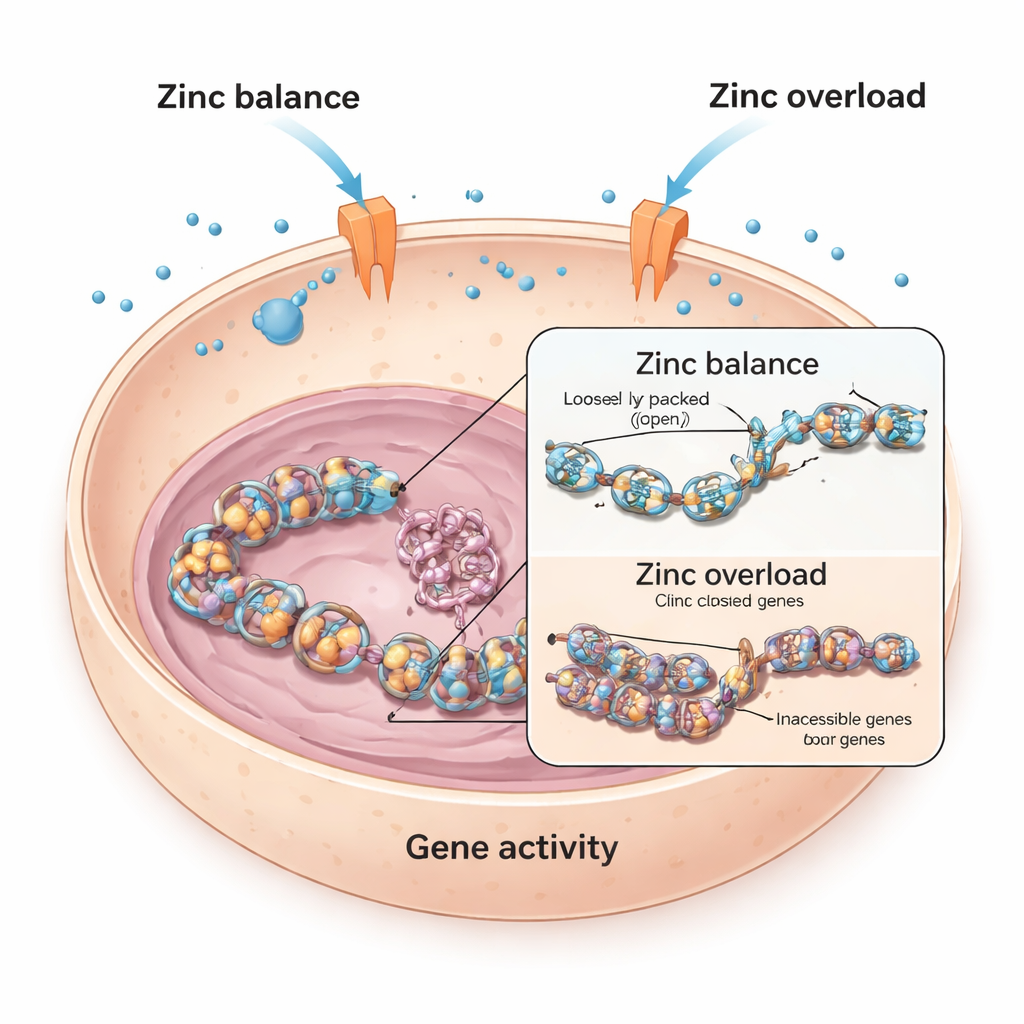
Equilibrar el zinc dentro de las células vivas
Cada célula depende del zinc, que ayuda a miles de proteínas a cumplir su función. Para evitar tanto la escasez como la sobrecarga, las células usan “puertas” especiales en sus membranas, llamadas transportadores de zinc, para mover el zinc hacia dentro y hacia fuera. Los investigadores empezaron con células del músculo cardíaco de ratón y humano, preguntándose qué sucede cuando estas células se exponen a zinc adicional. Encontraron que en las células cardíacas de ratón, niveles altos de zinc redujeron drásticamente la actividad de un gen clave relacionado con el corazón llamado Bmp4, que ayuda a orientar el desarrollo y la función cardíaca. En contraste, las células cardíacas humanas se vieron mucho menos afectadas, lo que sugiere que diferentes células se defienden de la sobrecarga de zinc de maneras distintas.
Cómo el zinc compacta el empaquetamiento del ADN
Para descubrir cómo el zinc silencia genes como Bmp4, el equipo examinó las histonas, las proteínas en forma de carrete alrededor de las cuales se enrolla el ADN. Cuando se añaden pequeñas marcas químicas llamadas grupos acetilo a las histonas, el ADN se vuelve más suelto y más fácil de leer; cuando estas marcas se eliminan, el ADN se empaqueta con más fuerza y los genes son más difíciles de activar. El estudio mostró que el exceso de zinc en las células cardíacas de ratón provocó una caída en la acetilación de histonas en un sitio específico (conocido como H3K9), que siguió de cerca la disminución de la actividad de Bmp4. Los fármacos que bloquean las enzimas desacetilasas de histonas pudieron revertir el efecto del zinc y restaurar Bmp4, lo que sugiere que el zinc desplazaba el equilibrio de este sistema de marcado químico.
Demasiado zinc dentro, no sólo fuera
El paso crucial resultó ser el zinc dentro del citoplasma acuoso de la célula, no sólo en el fluido circundante. Usando una sonda fluorescente que se ilumina en presencia de zinc libre, los investigadores observaron un aumento de zinc dentro de las células cardíacas de ratón tras el tratamiento. Cuando emplearon una molécula portadora de zinc para forzar la entrada directa de zinc en las células, observaron la misma caída en la acetilación de histonas y en la actividad génica, incluso con niveles mucho más bajos de zinc en el medio exterior. En las células cardíacas humanas, por el contrario, los transportadores de la membrana celular se ajustaron rápidamente: algunos importadores de zinc se apagaron y los exportadores aumentaron su actividad, evitando un gran incremento de zinc interno y protegiendo la acetilación de histonas. Las células cardíacas de ratón mostraron una respuesta de transportadores más “desajustada”, permitiendo que entrara más zinc y perturbara el control génico.
Del control génico a la autolimpieza en células normales y tumorales
Los investigadores se preguntaron entonces si este estrechamiento del empaquetamiento del ADN impulsado por el zinc es exclusivo de las células cardíacas. Probaron varios tipos de células humanas normales y líneas celulares cancerosas del estómago, el útero y el ovario. Cuando se permitió que el zinc se acumulara en el interior con ayuda de una portadora, casi todas estas células mostraron una clara caída en la acetilación de histonas. En algunos tumores, como las células del cáncer gástrico, esto ocurrió a dosis de zinc especialmente bajas, lo que sugiere que ciertos cánceres son inusualmente sensibles al desequilibrio de zinc. El equipo también vinculó la reducción de acetilación con la autofagia, un proceso en el que las células reciclan partes envejecidas. Aumentos moderados de zinc interno estimularon la autofagia, pero zinc muy alto la debilitó finalmente, lo que sugiere una ventana estrecha en la que el zinc podría usarse para ajustar finamente esta vía de autolimpieza.
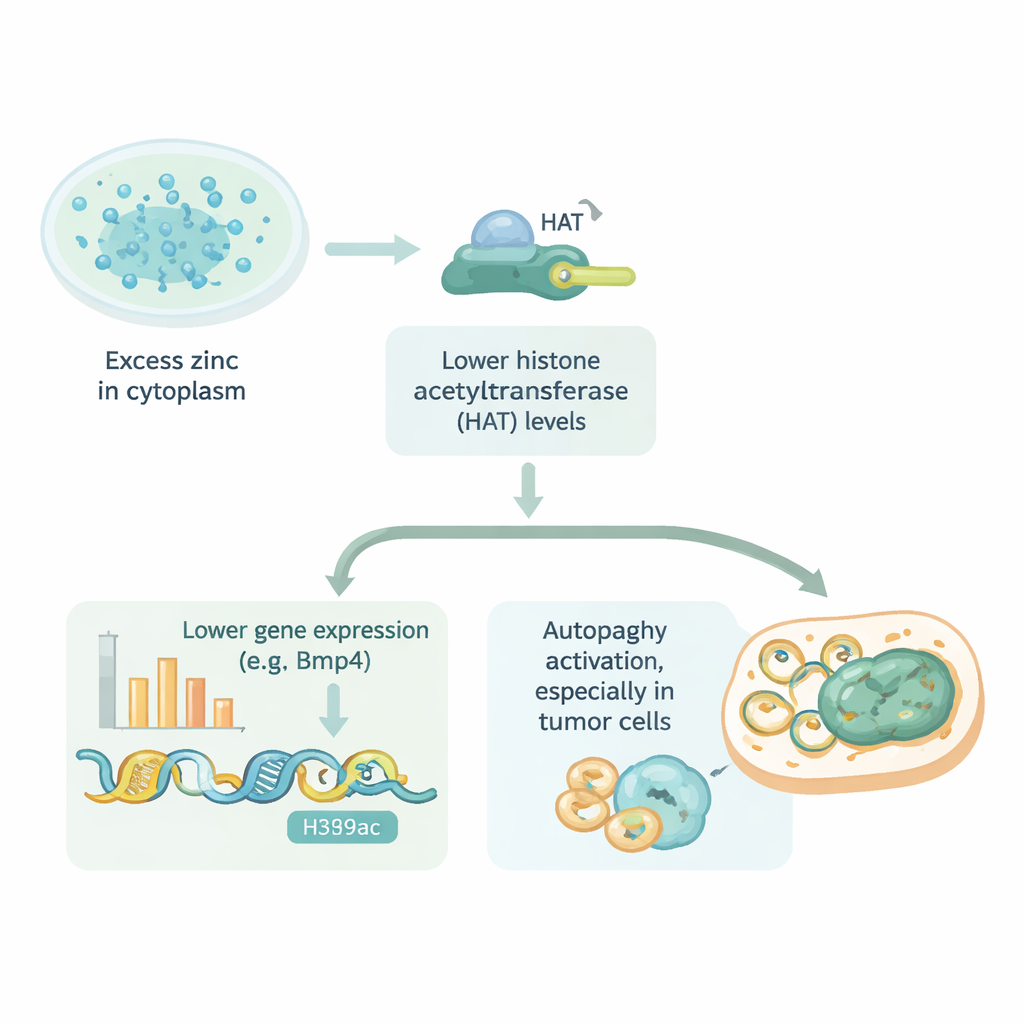
Qué significa esto para la salud y el tratamiento
En términos sencillos, este trabajo revela que demasiado zinc dentro de las células puede silenciar genes al dificultar el acceso al ADN, y que esa misma vía puede influir en la actividad con la que las células se limpian a sí mismas. El efecto no se limita a las células cardíacas; aparece en distintos tipos de células normales y cancerosas, aunque algunas son mejores que otras defendiendo contra la sobrecarga de zinc. Estas ideas sugieren que las diminutas “puertas” transportadoras de zinc en las membranas celulares podrían ser objetivos farmacológicos prometedores, ya sea para proteger tejidos sanos del daño relacionado con el zinc o para empujar a células tumorales vulnerables hacia la muerte. Si bien los hallazgos provienen de experimentos en cultivo celular, ofrecen una nueva perspectiva sobre cómo un nutriente cotidiano puede moldear la actividad génica y la enfermedad cuando su delicado equilibrio se altera.
Cita: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Palabras clave: homeostasis del zinc, regulación génica, acetilación de histonas, autofagia, células cancerosas