Clear Sky Science · es
La reprogramación metabólica aumenta la resistencia al estrés oxidativo en cardiomiocitos en diferenciación
Por qué importa la lucha de las células cardíacas contra el oxígeno
Cada latido de tu corazón depende de células musculares especializadas llamadas cardiomiocitos. A medida que crecemos, estas células afrontan un cambio vital: pasan de un entorno con baja disponibilidad de oxígeno y alimentado por azúcares en el útero a un mundo rico en oxígeno tras el nacimiento. El oxígeno es esencial, pero también genera subproductos dañinos que pueden lesionar el ADN y matar células. Este estudio explora cómo las células cardíacas en maduración reconfiguran su metabolismo para soportar más oxígeno, generar más energía y, al mismo tiempo, protegerse del daño oxidativo —insights que podrían orientar futuros tratamientos para enfermedades cardíacas y la regeneración.
De constructores sencillos a atletas de potencia
Las células cardíacas inmaduras, conocidas como cardiomioblastos, son pequeñas, se dividen y dependen principalmente de la degradación de glucosa para obtener energía. Al diferenciarse en cardiomiocitos maduros, dejan de dividirse y crecen, a menudo fusionándose en células polinucleadas y alargadas mejor adaptadas para una contracción potente. Usando microscopía de alta resolución, los investigadores observaron esta transformación durante diez días en un modelo celular de laboratorio. Los marcadores de proliferación celular descendieron, mientras las células se alargaron y se reorganizaron en estructuras fibrilares con apariencia cardíaca, confirmando que habían entrado en un estado más adulto y contráctil. 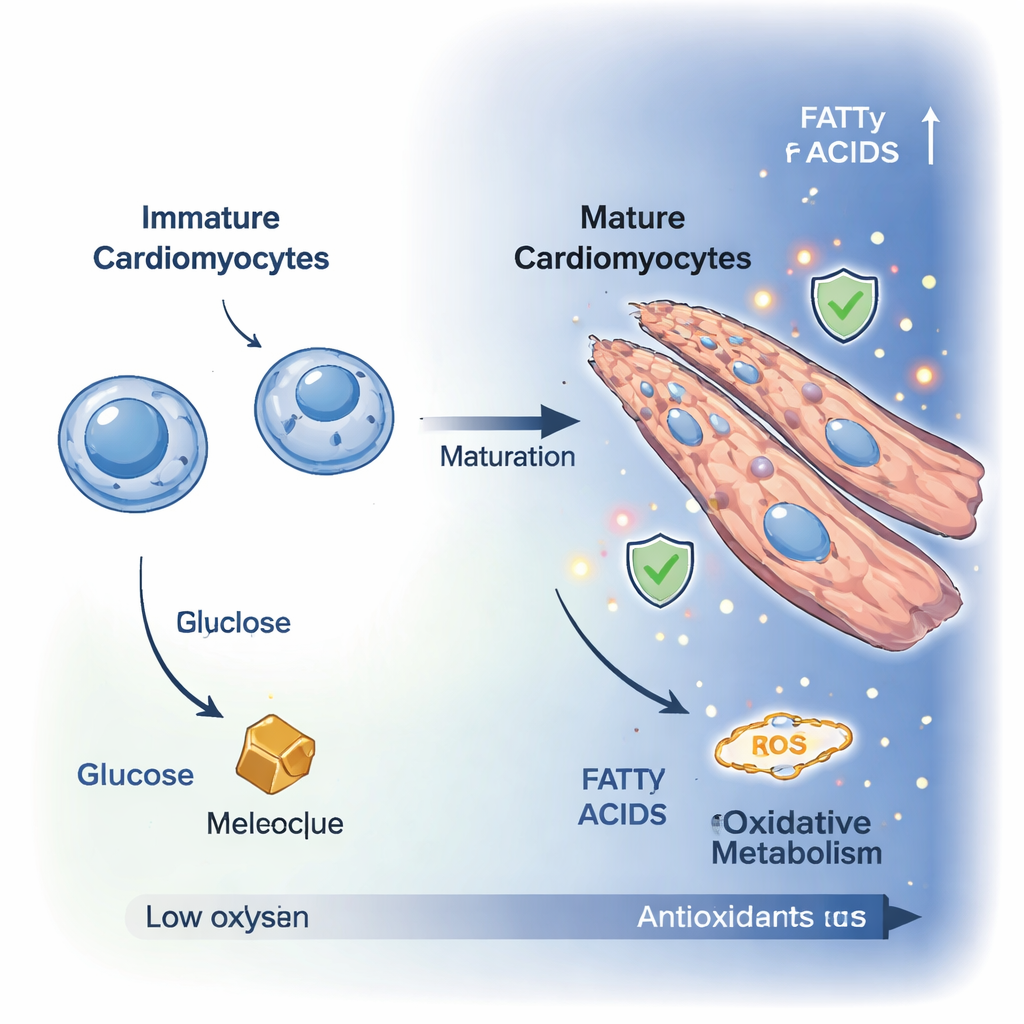
Cambio de fuentes de combustible y cableado de nuevas rutas energéticas
Para entender lo que ocurre bajo el capó, el equipo midió cientos de pequeñas moléculas dentro de las células y empleó imágenes avanzadas de la autofluorescencia celular para seguir el uso de energía en tiempo real. Juntas, estas técnicas mostraron un claro cambio desde un estado glicolítico, donde las células consumen principalmente glucosa, hacia un estado oxidativo dominado por la respiración mitocondrial. Los niveles de glucosa y fructosa disminuyeron, mientras que aumentaron intermediarios del ciclo de los ácidos tricarboxílicos (TCA), como el ácido cítrico, el malato y el oxoglutarato. El análisis de vías reveló una mayor actividad en rutas que alimentan combustible hacia las mitocondrias, incluida la lanzadera malato–aspártato y la degradación de aminoácidos, lo que indica que los cardiomiocitos maduros amplían sus opciones de combustible y canalizan la energía con mayor eficiencia hacia sus centrales energéticas.
Vivir con más oxígeno—y más estrés
Quemar combustible con mayor eficiencia en las mitocondrias tiene un coste: mayor producción de especies reactivas de oxígeno (ROS), moléculas químicamente agresivas que pueden dañar lípidos, proteínas y ADN. Los investigadores observaron que, a medida que los cardiomiocitos maduraban, sus mitocondrias se volvían más grandes y alargadas, y aumentaban los marcadores de estrés oxidativo. Las imágenes basadas en fluorescencia revelaron más gránulos tipo lipofuscina, un sello de lípidos oxidados, y una sonda nuclear mostró niveles más altos de ROS en las células diferenciadas. La metabolómica apuntó a cambios en el metabolismo del glutatión, un sistema antioxidante central que usa la molécula glutatión —compuesta a partir de aminoácidos como el glutamato y la glicina— para neutralizar las ROS. Estos hallazgos sugieren que, a medida que las células cardíacas elevan el metabolismo oxidativo, también afinan sus vías antioxidantes para mantener el daño bajo control. 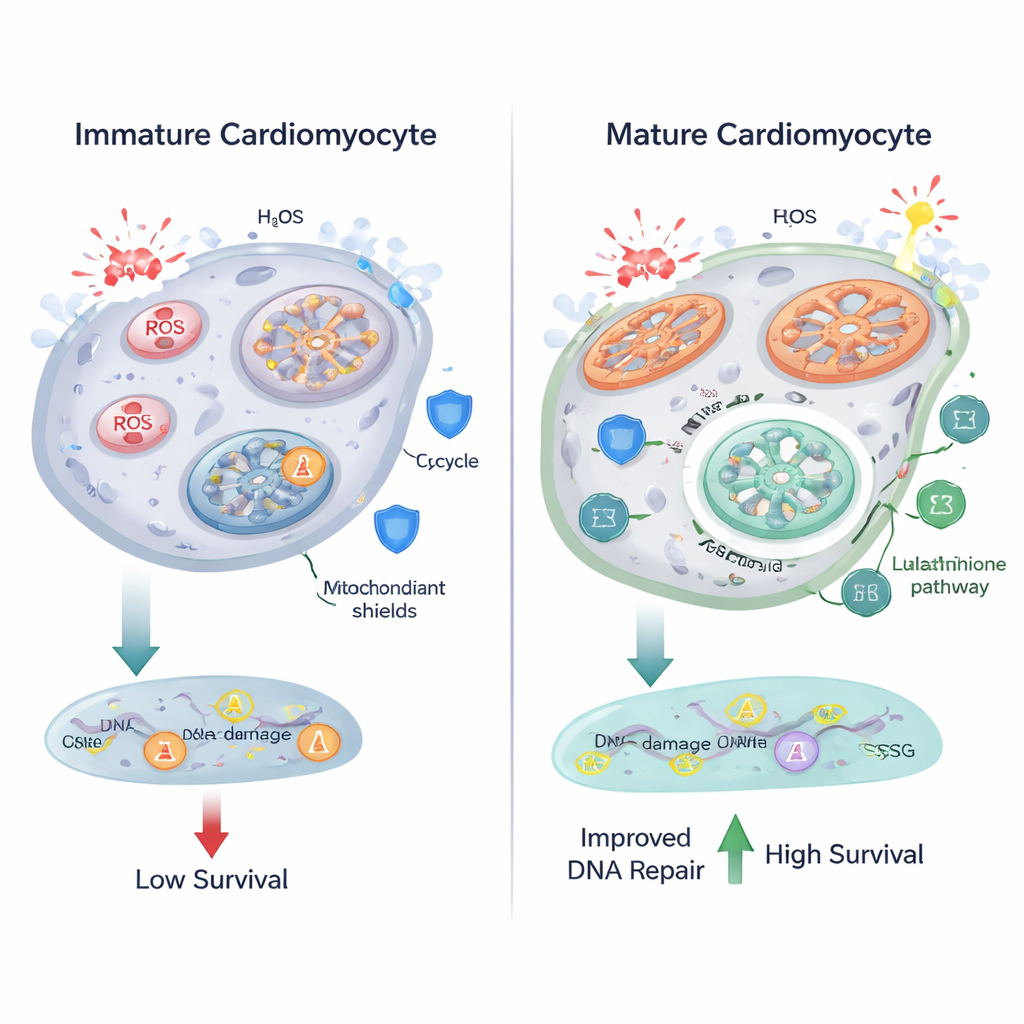
Daño contenido, defensas reforzadas
Sorprendentemente, a pesar de los niveles más altos de ROS, los cardiomiocitos diferenciados no mostraron más roturas de ADN que sus contrapartes inmaduras cuando se midió mediante focos de γ-H2AX, un marcador sensible de daño en el ADN. Cuando el equipo desafió a las células con peróxido de hidrógeno, un potente agente oxidante, tanto las células inmaduras como las maduras acumularon ROS y roturas de ADN —pero las células maduras se comportaron mejor. Presentaron proporcionalmente menos lesiones en el ADN en relación con sus niveles más altos de ROS, fueron menos propensas a activar señales vinculadas a la muerte celular como PUMA y mostraron tasas de supervivencia marcadamente mayores. Estos resultados indican que los cardiomiocitos en maduración no solo ajustan su metabolismo, sino que también mejoran sus mecanismos de reparación del ADN y de supervivencia, lo que les permite resistir condiciones oxidativas más severas.
Qué significa esto para proteger el corazón
En términos sencillos, este estudio muestra que, a medida que las células cardíacas maduran, aprenden a funcionar a mayor rendimiento sin consumirse. Cambian de un estilo de vida rico en azúcares y con poco oxígeno a otro intensivo en oxígeno y impulsado por las mitocondrias, y al mismo tiempo construyen mejores escudos y equipos de reparación para afrontar el estrés oxidativo. Comprender este equilibrio finamente ajustado entre producción de energía y autoprotección podría ayudar a los científicos a diseñar estrategias para hacer el tejido cardíaco adulto dañado más resistente, o para guiar células madre hacia cardiomiocitos más seguros y duraderos para terapias regenerativas.
Cita: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Palabras clave: diferenciación de cardiomiocitos, estrés oxidativo, mitocondrias, metabolismo celular, enfermedad cardíaca