Clear Sky Science · es
La desglucosilación induce una nueva conformación distal en el receptor de manosa CD206
Por qué importan los recubrimientos de azúcar en los sensores inmunitarios
Nuestras células inmunitarias dependen de “antenas” moleculares para detectar amenazas como microbios y células cancerosas. Una de estas antenas, llamada receptor de manosa CD206, ayuda a las células inmunitarias a atrapar moléculas decoradas con azúcares e incluso a localizar tumores. Como muchas proteínas, el propio CD206 está cubierto por pequeñas cadenas de azúcar. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones: ¿qué ocurre con la forma y la función de CD206 cuando se eliminan esos azúcares?
Un brazo flexible que interpreta señales azucaradas
CD206 se sitúa en la superficie de ciertas células inmunitarias, en especial macrófagos que patrullan tejidos y tumores. Tiene una estructura larga y articulada que se extiende desde la membrana celular y termina en varios segmentos “lectina” que reconocen azúcares en moléculas que pasan. CD206 también puede desprenderse al torrente sanguíneo, donde sus niveles se correlacionan con enfermedades inflamatorias y fibróticas, lo que lo convierte en un posible marcador de enfermedad. La proteína está fuertemente decorada con cadenas de azúcar N-enlazadas, que trabajos previos han mostrado que pueden influir en la capacidad de distintos segmentos del receptor para reconocer azúcares. Muchos de estos sitios azucarados están lejos de las cavidades de unión principales, lo que sugiere que podrían actuar más como interruptores remotos que como simples bloqueadores.
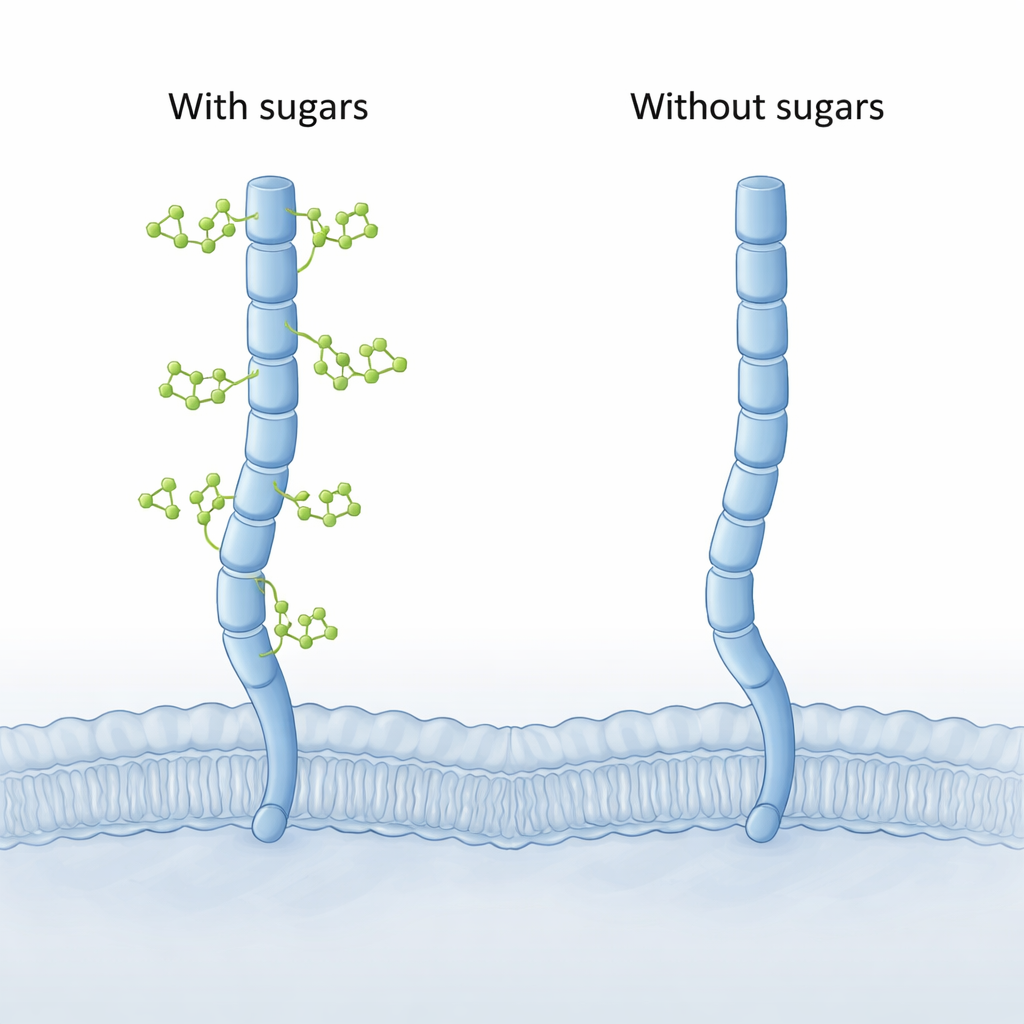
Modelos por ordenador revelan una curva oculta
Dado que la estructura 3D completa de CD206 aún no se ha capturado experimentalmente, los autores recurrieron a herramientas computacionales modernas. Primero usaron AlphaFold para construir modelos de longitud completa del receptor y luego ejecutaron largas y detalladas simulaciones de dinámica molecular de CD206 con y sin sus azúcares unidos. Ambas versiones se comportaron como un brazo molecular extendido, pero la forma “sin azúcar” mostró un movimiento nuevo y llamativo en su extremo distal. Los dos últimos segmentos de lectina (llamados CTLD7 y CTLD8) podían oscilar hacia el interior para formar una punta cóncava y curvada hacia dentro, una forma nunca observada en la versión glicosilada, que permanecía más curvada hacia fuera, es decir, convexa.
Cómo un pequeño cambio remodela el movimiento
Para entender esta diferencia, el equipo analizó los movimientos dominantes en sus simulaciones. Encontraron que el movimiento principal que distinguía las dos formas era esta flexión de la punta distal, y que solo aparecía cuando faltaban los azúcares. La eliminación de azúcares aumentó en general la flexibilidad del receptor, especialmente en los segmentos de lectina distales y, en menor medida, cerca del extremo N-terminal. Mapas de correlación de cómo se mueven conjuntamente distintas partes de la proteína mostraron que, sin azúcares, los dos últimos segmentos de lectina se mueven de forma más concertada y están más acoplados a otras regiones. En esencia, los azúcares no solo permanecen en la superficie; ayudan a afinar la flexibilidad del brazo entero y la comunicación a lo largo de su longitud.
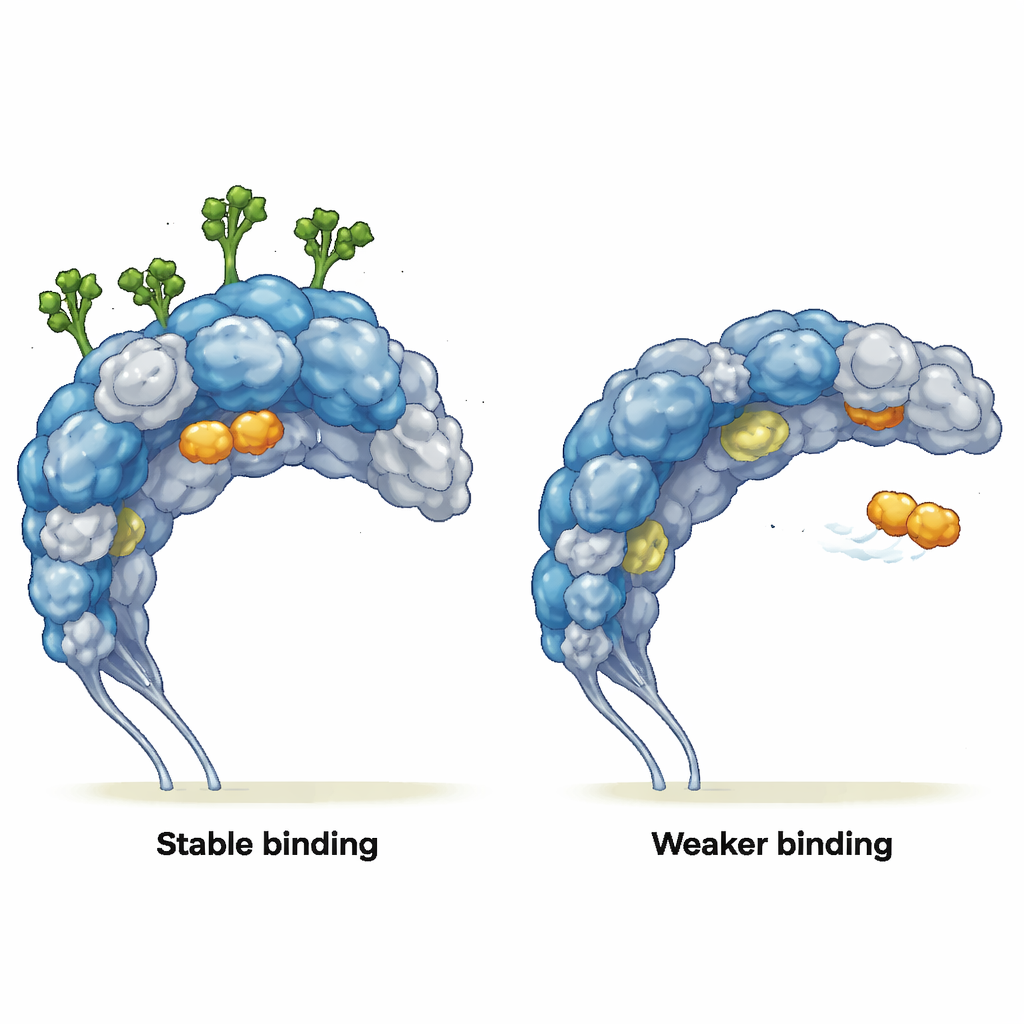
Cambio en la forma de unión de los socios
Los autores preguntaron entonces cómo afecta este movimiento alterado a socios de unión reales. Simularon interacciones con dos ligandos: un azúcar simple similar a la manosa (MMA), que encaja en una cavidad bien definida, y un péptido dirigido a tumores llamado mUNO, que tiene como diana a macrófagos asociados a tumores positivos para CD206. Cuando estaban presentes los azúcares, MMA permaneció encajado en su bolsillo de unión durante toda la simulación, manteniendo contactos clave, a pesar de que la estructura proteica cercana apenas cambiaba. Sin azúcares, MMA escapó del bolsillo, rozando la superficie de la proteína y formando solo contactos breves y superficiales. Para mUNO, el receptor glicosilado mostró varias conformaciones de unión estables con contactos frecuentes y duraderos. En el receptor desglucosilado, la unión de mUNO fue más débil y dispersa, y además empezó a explorar regiones que normalmente están bloqueadas por cadenas de azúcar, revelando nuevos sitios de interacción previamente ocultos.
Qué significa esto para la enfermedad y la terapia
En conjunto, estos resultados muestran que los azúcares unidos a CD206 actúan como reguladores remotos de su forma y adhesividad. Al restringir ciertos pliegues y organizar cómo se mueven sus segmentos de forma concertada, la glicosilación ayuda al receptor a retener con mayor firmeza algunos ligandos y a dirigir otros hacia puntos de acoplamiento preferentes, al tiempo que protege partes de su superficie. En enfermedades como el cáncer, donde los patrones generales de azúcares en las proteínas suelen alterarse, CD206 puede adoptar formas y comportamientos de unión distintos, cambiando la manera en que las células inmunitarias perciben su entorno. Comprender este “interruptor conformacional” dependiente de azúcares no solo aclara cómo funciona CD206, sino que también sugiere nuevas formas de diseñar fármacos o agentes de imagen que exploten su paisaje cambiante en tumores y otras condiciones patológicas.
Cita: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Palabras clave: receptor de manosa, glicosilación de proteínas, reconocimiento inmune, macrófagos asociados a tumores, dinámica molecular