Clear Sky Science · es
Pérdida de Snhg5 altera la regulación del ciclo celular sin modificar la cistogénesis en un modelo murino de enfermedad renal poliquística
Por qué importa un gen renal con un nombre extraño
La enfermedad renal poliquística (ERPK) es un trastorno hereditario común en el que innumerables sacos llenos de líquido invaden lentamente los riñones, conduciendo a menudo a insuficiencia renal. Los científicos saben que fallos en dos genes, PKD1 y PKD2, impulsan la enfermedad, pero muchos otros actores genéticos pueden influir en la velocidad de su progresión. Este estudio se centra en un tipo inusual de gen llamado ARN largo no codificante, denominado Snhg5, y plantea una pregunta simple pero importante: ¿esta molécula configura de forma significativa cómo se desarrolla la ERPK, o es mayormente una espectadora?
Una mirada más cercana a un mensajero genético oscuro
A diferencia de los genes típicos que proporcionan planos para proteínas, los ARN largos no codificantes actúan más bien como organizadores moleculares o interruptores dentro de las células. Trabajos anteriores mostraron que Snhg5 aumenta notablemente en modelos murinos de ERPK y se ha vinculado con varios cánceres y lesiones renales, lo que sugiere que podría promover un crecimiento dañino. Los investigadores primero mapearon dónde y cuándo está activo Snhg5 en ratones normales. Encontraron que se activa en muchos órganos, con niveles especialmente altos en el intestino, y que su actividad en el riñón cae bruscamente tras el nacimiento, cuando el órgano pasa de un rápido crecimiento a un estado más estable y maduro. Dentro de las células renales, casi todas las moléculas de Snhg5 residen en el núcleo, el centro de control que alberga el ADN, lo que sugiere que Snhg5 ayuda a controlar la actividad génica en lugar de producir proteínas directamente.
Los patrones en riñones enfermos no cuentan toda la historia
El equipo comparó luego los niveles de Snhg5 en una serie de modelos murinos de ERPK. En modelos de progresión rápida, donde los quistes se forman con rapidez, Snhg5 aumentó entre dos y tres veces en riñones enfermos, y la imagen a nivel celular único mostró señales nucleares intensas en las células que revisten los quistes y en el tejido circundante. Sorprendentemente, en un modelo murino más lento y leve que imita mejor el curso prolongado de la ERPK humana, Snhg5 no aumentó. Aún más llamativo, en tejido renal de personas con ERPK autosómica dominante avanzada, la contraparte humana del gen, llamada SNHG5, estaba reducida en más del 90 por ciento. En conjunto, estos resultados sugieren que los cambios en este ARN acompañan la formación de quistes, pero la dirección y el momento del cambio difieren entre especies y etapas de la enfermedad, lo que genera dudas sobre si Snhg5 por sí sola es un impulsor directo del crecimiento quístico.
Qué sucede cuando se elimina el gen
Para ir más allá de la correlación, los investigadores usaron edición genética CRISPR para eliminar por completo el gen Snhg5 en ratones, creando una línea global de “knockout”. Contrariamente a las preocupaciones de que eliminar una molécula tan fuertemente alterada pudiera ser dañino, los ratones sin Snhg5 nacieron en proporciones normales, vivieron vidas normales y tenían riñones que se veían y funcionaban como los de sus camadas sanas. El examen microscópico reveló una estructura renal normal sin cicatrización ni inflamación, y las pruebas sanguíneas no mostraron signos de filtración renal deteriorada. A nivel molecular, sin embargo, surgieron cambios más sutiles: tanto los riñones de ratón como las células de túbulo renal cultivadas sin Snhg5 mostraron desplazamientos consistentes en la actividad de genes relacionados con la división celular y la replicación del ADN. En cultivo celular, más células se quedaban estancadas en fases avanzadas del ciclo celular y en un estado dañado, sub-G1. Una proteína en particular, ARPC5, parte de un complejo que ayuda a las células a dividirse reordenando su armazón interno, se redujo cuando faltaba Snhg5, sugiriendo una posible cadena de causa y efecto.
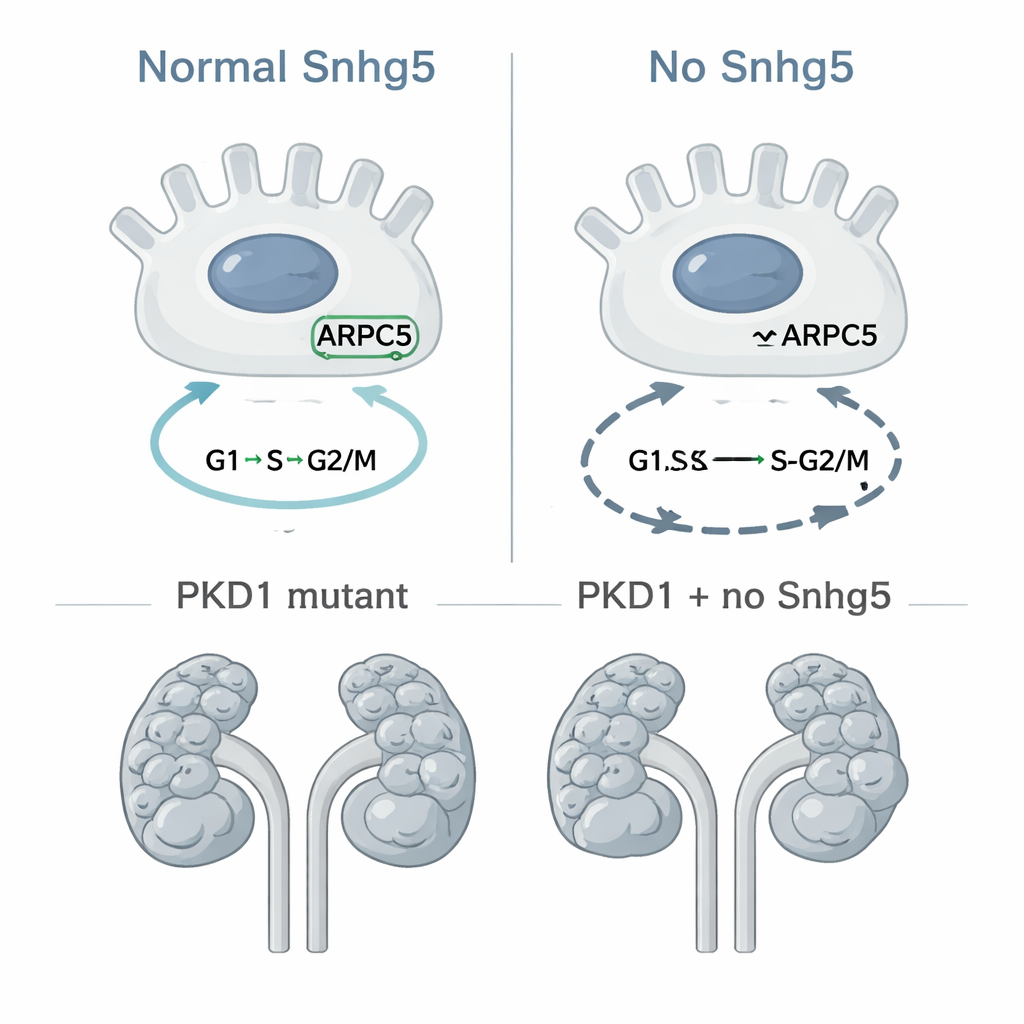
Probando su papel en el crecimiento de quistes directamente
Puesto que la división celular descontrolada es una característica central de la ERPK, el equipo preguntó si eliminar Snhg5 frenaría la formación de quistes en un modelo murino bien establecido donde el gen PKD1 está desactivado específicamente en las células del túbulo colector, fuente de muchos quistes. Cruzaron ratones de modo que algunos tuvieran solo la mutación en PKD1, mientras otros carecían tanto de PKD1 como de Snhg5. Al examinar a los animales a los 10 días de edad, ambos grupos mostraron riñones severamente quísticos, y medidas cuidadosas del tamaño renal, del área quística y del número de quistes no revelaron una protección significativa por la eliminación de Snhg5. Si acaso, los ratones doble mutantes tendían a tener una carga quística ligeramente mayor, aunque la diferencia fue pequeña y no estadísticamente concluyente. En otras palabras, aunque Snhg5 influye en genes del ciclo celular en células renales, su ausencia no cambia de forma notable la rapidez con la que aparecen o aumentan los quistes en este modelo particular de ERPK.
Qué significa esto para futuros tratamientos
Para pacientes y desarrolladores de fármacos, la conclusión principal es que Snhg5, a pesar de ser una de las señales genéticas más alteradas en la ERPK murina, no es una pieza clave de la formación de quistes—al menos no en la fase temprana y de rápido crecimiento derivada del túbulo colector. El gen sí parece afinar cómo las células renales avanzan por el ciclo de división, probablemente a través de su impacto en factores como ARPC5, pero esta influencia es lo bastante sutil como para que su pérdida completa deje el desarrollo renal y la progresión temprana de la ERPK en gran medida sin cambios. Estos hallazgos subrayan una lección más amplia: no todo cambio molecular llamativo en tejido enfermo es un objetivo terapéutico prometedor. Desentrañar causa y consecuencia requerirá probar los ARN largos no codificantes como Snhg5 en múltiples modelos de la enfermedad y en distintos momentos antes de plantearlos con confianza como candidatos a fármaco.
Cita: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Palabras clave: enfermedad renal poliquística, ARN largo no codificante, Snhg5, ciclo celular, quistes renales