Clear Sky Science · es
Nanocápsulas de quitosano y sulfato de dextrano para mejorar la eficacia de la tigeciclina frente a Salmonella enterica no tifoidea
Por qué esto importa para la seguridad alimentaria
La mayoría de la gente conoce a Salmonella como una causa desagradable de intoxicación alimentaria, a menudo asociada al pollo poco cocinado. Menos personas saben que algunas cepas se han vuelto tan resistentes a los antibióticos que incluso medicamentos «de último recurso» potentes pueden fallar. Este estudio explora una estrategia basada en nanotecnología para rescatar uno de esos fármacos, la tigeciclina, encapsulándola en pequeñas cápsulas a base de azúcares que le ayudan a entrar en las células infectadas y a bloquear mecanismos clave de resistencia en Salmonella.
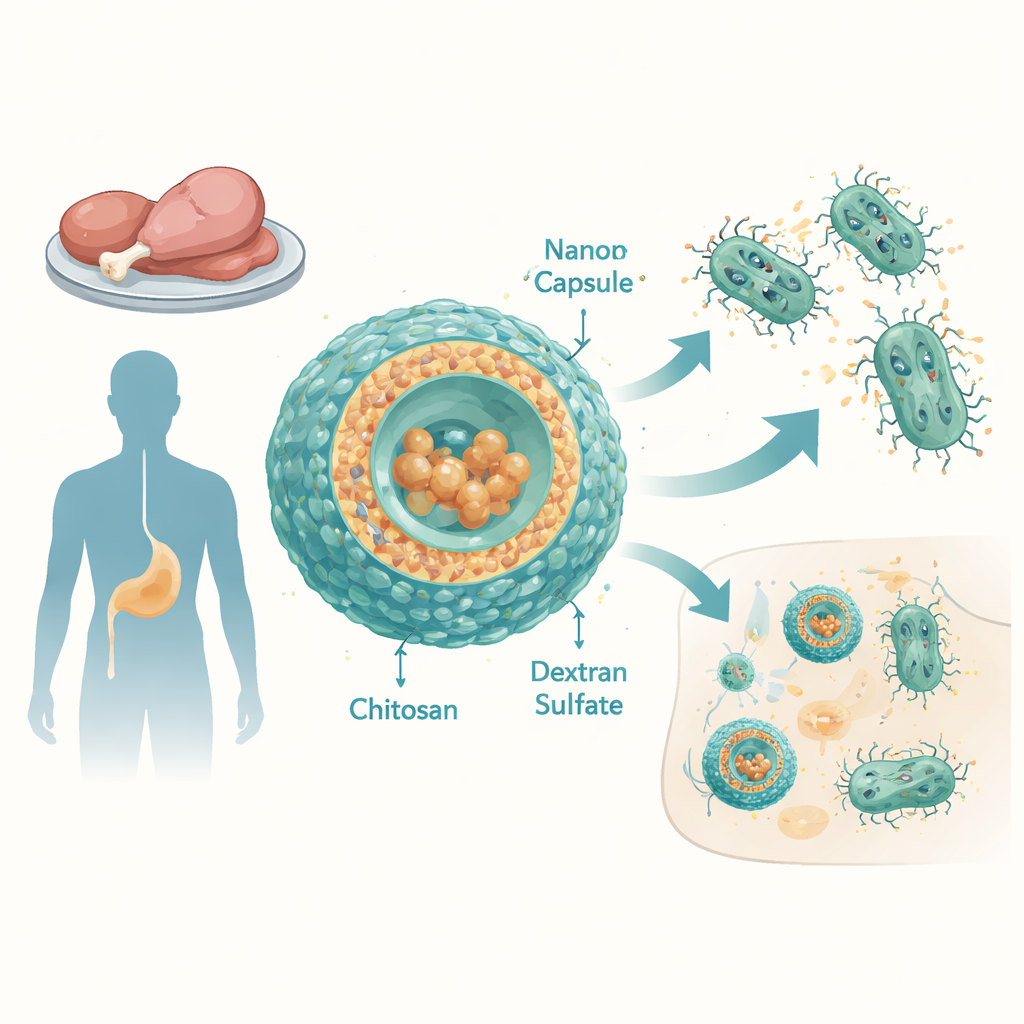
La amenaza creciente de Salmonella resistente
Los serovares de Salmonella no tifoidea (NTS) son una causa principal de diarrea e infecciones en el torrente sanguíneo a nivel mundial, especialmente en países de ingresos bajos y medios. Los investigadores examinaron 12 cepas de Salmonella enterica obtenidas de carne de pollo y pato en Egipto. Estas cepas eran resistentes a muchos antibióticos de uso común, incluidos penicilinas, cefalosporinas, tetraciclinas y otros, y mostraron puntuaciones elevadas de resistencia múltiple a antibióticos. Incluso la tigeciclina, un fármaco de amplio espectro reservado para casos difíciles, funcionó mal: las bacterias toleraban concentraciones muy altas. Una razón principal fueron las «bombas de eflujo» hiperactivas: máquinas moleculares en la membrana bacteriana que expulsan constantemente los antibióticos fuera de la célula.
Construir una cápsula de fármaco más inteligente
Para vencer esto, el equipo diseñó cápsulas a escala nanométrica hechas de dos polímeros naturales: quitosano, obtenido de la quitina (el material de las conchas de los mariscos), y sulfato de dextrano, una molécula de azúcar ramificada. Al ajustar cuidadosamente las proporciones de estos componentes, produjeron partículas estables de unos 100–150 nanómetros de diámetro, con carga superficial positiva que favorece su interacción con las membranas bacterianas y de las células del huésped. La tigeciclina se cargó en estas partículas con una eficiencia notablemente alta: esencialmente todo el fármaco quedó dentro de las cápsulas. En pruebas de laboratorio que imitan condiciones en el torrente sanguíneo, las cápsulas liberaron la mayor parte de su tigeciclina en pocas horas, lo que sugiere que podrían proporcionar un fuerte pulso de antibiótico en los sitios de infección.
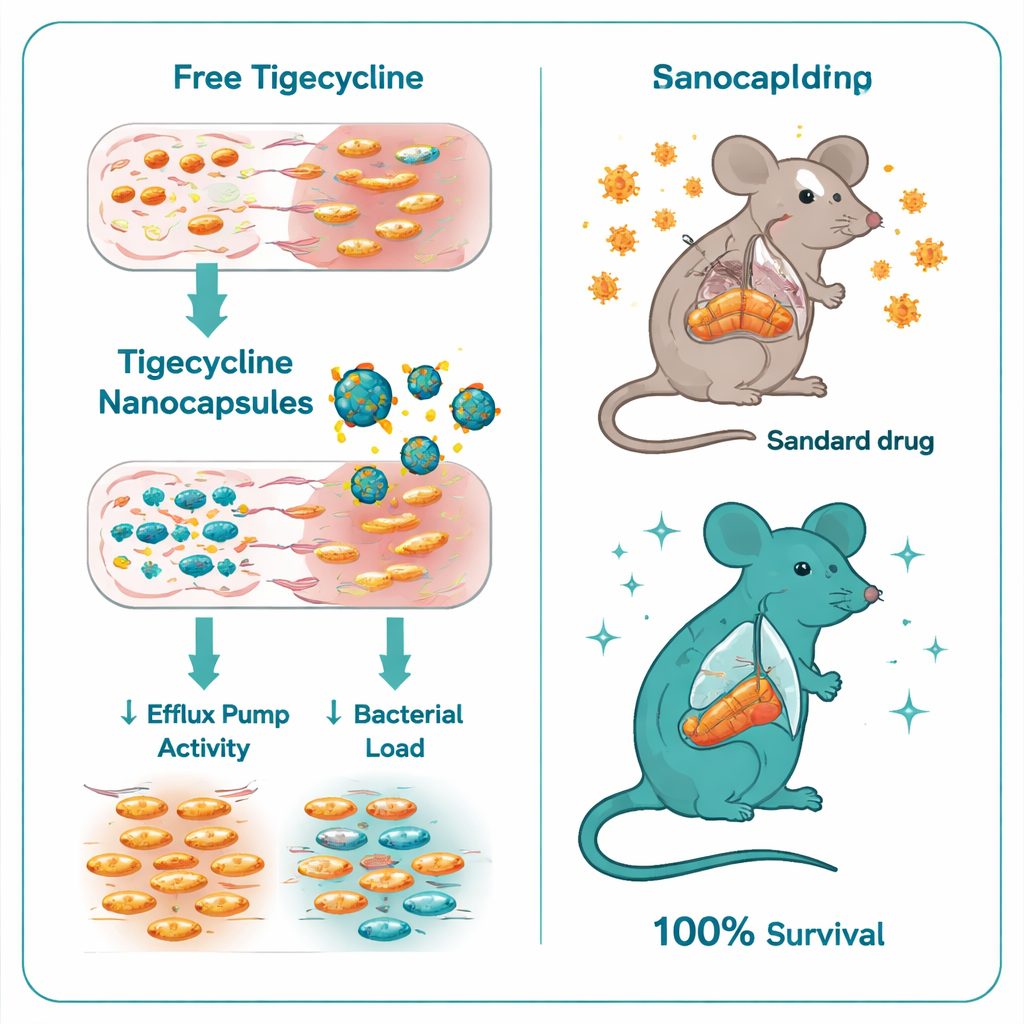
Apagando las defensas bacterianas
Cuando los investigadores compararon la tigeciclina libre con la tigeciclina encapsulada en nanocápsulas de quitosano–sulfato de dextrano, la diferencia fue notable. La concentración mínima de fármaco necesaria para detener el crecimiento bacteriano bajó de 32–128 microgramos por mililitro con la tigeciclina libre a solo 0,5–1 microgramo por mililitro con las nanocápsulas —una mejora de seis a siete veces. Experimentos de cinética bactericida mostraron que la forma encapsulada mataba a Salmonella de manera mucho más rápida y completa. A nivel genético, las nanocápsulas también disminuyeron reguladores clave de resistencia: la expresión de los genes ramA y acrB, que controlan y forman bombas de eflujo importantes, se redujo varias veces en las bacterias tratadas. En otras palabras, las cápsulas no solo administraron más fármaco; ayudaron a desactivar una de las principales vías de escape de las bacterias.
Protegiendo ratones infectados de una enfermedad letal
El equipo probó luego la nueva formulación en un modelo murino de infección severa por Salmonella Typhimurium. Los ratones infectados y no tratados murieron todos en ocho días. Los ratones que recibieron tigeciclina estándar lo hicieron mejor pero siguieron presentando una mortalidad alta, con solo un 40% de supervivencia. En marcado contraste, todos los ratones tratados con las nanocápsulas cargadas con tigeciclina sobrevivieron. Estos animales tenían muchas menos bacterias en hígado e intestinos, análisis sanguíneos más cercanos a la función hepática y renal normal, y daños tisulares mucho más leves al examen microscópico. Incluso las cápsulas «vacías» de quitosano–sulfato de dextrano, sin antibiótico, ofrecieron cierta protección, probablemente porque el quitosano posee efectos antimicrobianos y antiinflamatorios modestos, pero la combinación con tigeciclina fue claramente superior.
Qué podría significar esto para tratamientos futuros
Para el público general, el mensaje central es que encapsular un antibiótico existente dentro de una nanocápsula inteligente y biocompatible puede restaurar su eficacia frente a Salmonella altamente resistente. Al ayudar al fármaco a alcanzar bacterias que se esconden dentro de células y al reducir las bombas que normalmente expulsan el fármaco, el sistema de quitosano–sulfato de dextrano convirtió un antibiótico de último recurso en un tratamiento muy efectivo en ratones, con un 100% de supervivencia. Aunque se requiere más trabajo antes de que este enfoque pueda usarse en personas o en animales de granja, ofrece una vía prometedora para prolongar la vida útil de antibióticos importantes y mejorar la seguridad de los alimentos sin necesidad de inventar fármacos completamente nuevos desde cero.
Cita: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Palabras clave: Salmonella, resistencia a antibióticos, nanopartículas, administración de fármacos, tigeciclina