Clear Sky Science · es
La proteómica y metabolómica integradas revelan que lactonas sesquiterpénicas vegetales inhiben la actividad de células de CMTN al agotar la síntesis de ATP y reprogramar el metabolismo primario
Compuestos vegetales que privan de energía al cáncer de mama agresivo
El cáncer de mama triple negativo es una de las formas más difíciles de tratar porque carece de los habituales “puntos de agarre” hormonales que utilizan muchos fármacos. Este estudio explora dos moléculas extraídas de una planta medicinal que parecen apagar las centrales internas de estas células cancerosas, cortando su suministro de energía mientras respetan en gran medida a las células mamarias normales. Comprender cómo funciona esto podría abrir la puerta a tratamientos más selectivos y menos agresivos para pacientes que actualmente tienen opciones limitadas.
Por qué importa atacar la fuente de energía del cáncer
Cada célula depende de pequeñas estructuras llamadas mitocondrias para producir ATP, el combustible básico celular. Las células cancerosas, especialmente las más agresivas, suelen depender de forma inusual de sus mitocondrias para sostener el crecimiento rápido, la diseminación y la supervivencia bajo estrés. Los investigadores se centraron en células de cáncer de mama triple negativo, que representan alrededor del 15–20% de los cánceres de mama y tienden a recaer y metastatizar con más frecuencia que otros tipos. Estudiaron una molécula natural, deoxyelephantopin (DET), y su derivado refinado DETD‑35, ambas lactonas sesquiterpénicas de la planta medicinal Elephantopus. Trabajos previos mostraron que estos compuestos inducen estrés oxidativo y formas inusuales de muerte celular en células cancerosas, pero no se entendía bien cómo alteraban las centrales energéticas de las células.
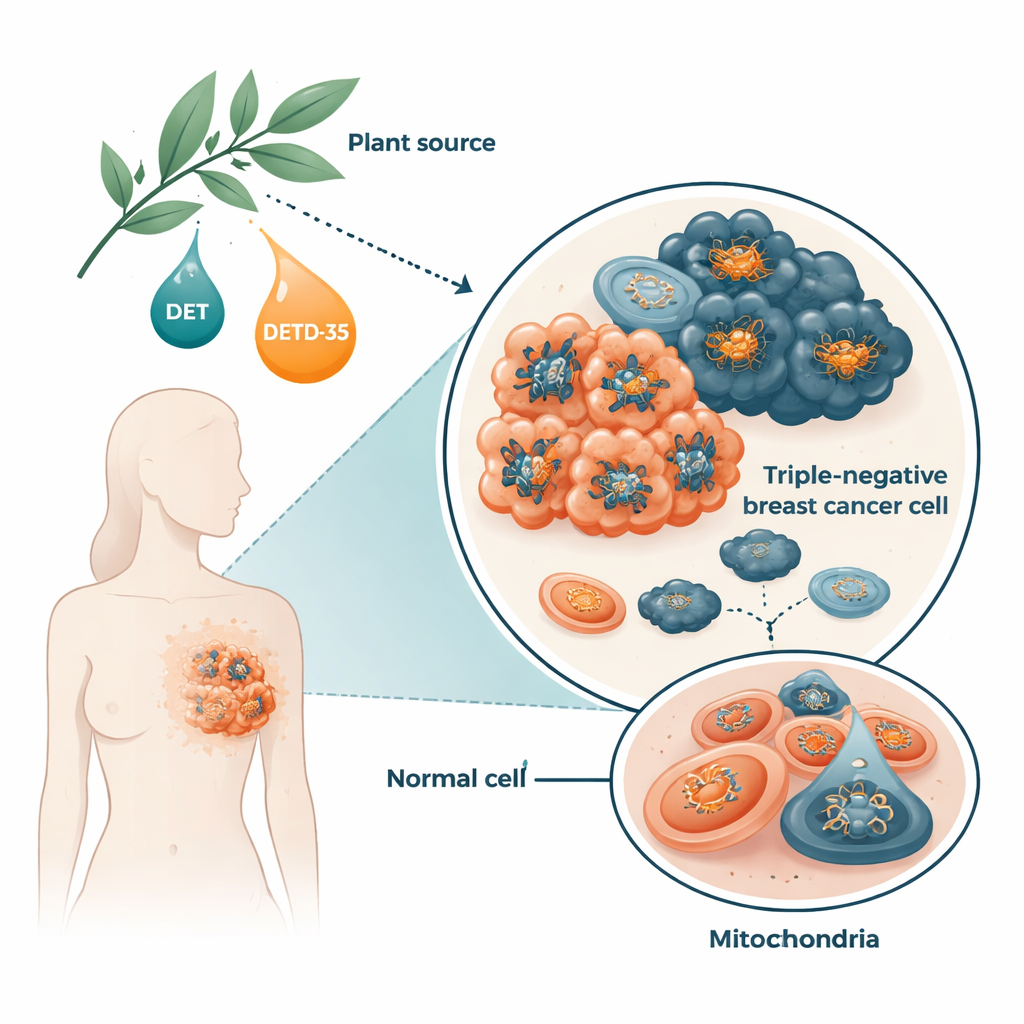
Cómo las moléculas vegetales alteran las mitocondrias de las células cancerosas
Usando células humanas de cáncer de mama triple negativo cultivadas en el laboratorio, el equipo observó que DET y DETD‑35 aumentaban rápidamente la producción de especies reactivas de oxígeno, un tipo de “escape” químico reactivo generado durante la producción de energía. En respuesta, las células aumentaron ciertas enzimas protectoras, pero no lo suficiente como para restaurar el equilibrio. Los compuestos también forzaron la apertura de un canal en la membrana mitocondrial conocido como poro de transición de permeabilidad, un cambio asociado con hinchazón, pérdida del potencial de membrana y los primeros pasos de la muerte celular. En cuestión de horas, los niveles de ATP dentro de las células cancerosas descendieron bruscamente. Cuando los investigadores añadieron un antioxidante con antelación, estos efectos dañinos se revirtieron en gran medida, lo que demuestra que el estrés oxidativo fue una pieza clave del proceso.
Mapeando el daño a proteínas y al metabolismo
Para comprender el panorama global, los científicos combinaron dos potentes enfoques “ómicas”. Catalogaron miles de proteínas mitocondriales y midieron muchos pequeños metabolitos en células tratadas frente a no tratadas. Esta visión integrada reveló que DET y DETD‑35 alteraron proteínas implicadas en la fosforilación oxidativa, la vía principal que usan las mitocondrias para generar ATP, y activaron señales relacionadas con la muerte celular. Al mismo tiempo, rutas metabólicas centrales que manejan aminoácidos, grasas y bloques de construcción para el ADN se reprogramaron. Ciertos lípidos que ayudan a dar forma a la membrana mitocondrial interna, así como moléculas vinculadas a defensas antioxidantes y a la degradación de azúcares, cambiaron de manera coherente con un estado de estrés y falta de energía en las células cancerosas. De forma crucial, estos cambios generalizados no se observaron en células mamarias normales expuestas a las mismas dosis, lo que sugiere cierto grado de selectividad hacia las células tumorales.
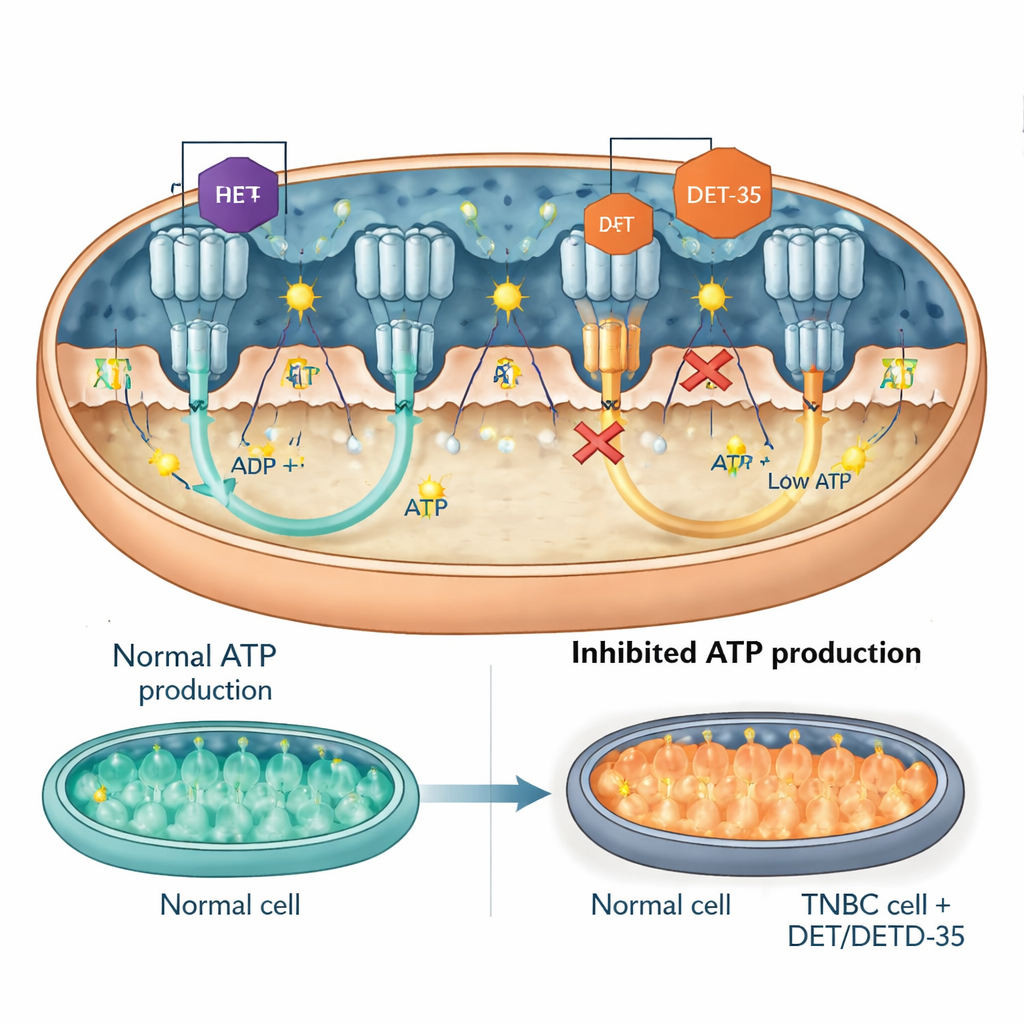
Una proteína señal clave y la propia turbina de ATP
El equipo se centró luego en actores específicos dentro de estas redes alteradas. Uno fue PRKCA, una proteína de señalización que puede desplazarse a las mitocondrias e influir tanto en la producción de energía como en las respuestas al estrés. DET y DETD‑35 aumentaron los niveles de PRKCA en las células cancerosas. Cuando los investigadores utilizaron herramientas genéticas para reducir PRKCA, los fármacos resultaron menos tóxicos: las células cancerosas tenían más probabilidades de sobrevivir, producían más ATP y mostraban menos signos de mal funcionamiento mitocondrial y apoptosis. Otro objetivo fue la ATP sintasa, la “turbina” molecular que gira para generar ATP. Las mediciones mostraron que DET y DETD‑35 redujeron directamente la actividad de la ATP sintasa en mitocondrias de células cancerosas. Modelos de acoplamiento por ordenador sugirieron que ambos compuestos se alojan en interfaces críticas de la enzima, las mismas regiones generales donde se unen fármacos conocidos que bloquean la ATP sintasa, obstaculizando físicamente su movimiento y reduciendo la producción de ATP. En ratones con tumores humanos de cáncer de mama triple negativo, el tratamiento con cualquiera de los compuestos disminuyó los niveles de componentes de la ATP sintasa en el tejido tumoral, respaldando los hallazgos de los ensayos celulares.
Qué podría significar esto para tratamientos futuros contra el cáncer
En conjunto, el estudio dibuja un panorama coherente: estos compuestos de origen vegetal empujan a las células de cáncer de mama triple negativo a una crisis energética al sobrecargarlas con estrés oxidativo, forzar la apertura de poros mitocondriales y bloquear directamente la maquinaria productora de ATP. A medida que el ATP se agota y el metabolismo se trastoca, las células cancerosas pierden su capacidad de crecer y sobrevivir, mientras que las células mamarias normales permanecen en gran medida indemnes bajo las mismas condiciones. Para un lector general, la conclusión es que los científicos podrían explotar la fuerte dependencia del cáncer en sus centrales internas, usando moléculas diseñadas con precisión—algunas inspiradas en plantas—para agotar las baterías de las células tumorales sin desconectar los tejidos sanos. Se necesitará más trabajo antes de que tales agentes puedan llegar a la clínica, pero esta visión integrada de proteínas, metabolitos y flujo energético ofrece una hoja de ruta prometedora.
Cita: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Palabras clave: cáncer de mama triple negativo, mitocondrias, sintasa de ATP, productos naturales, metabolismo del cáncer