Clear Sky Science · es
Derivación de un biomarcador de la actividad cerebral intrínseca para la predicción más temprana del deterioro cognitivo
Por qué importan los cambios cerebrales tempranos
Muchos adultos mayores advierten lapsos sutiles de memoria mucho antes de que un médico pueda diagnosticar demencia. En esta fase, las pruebas de imagen y los análisis de sangre estándar a menudo parecen normales, sin embargo el proceso patológico subyacente puede ya estar en marcha. Este estudio explora si una prueba sencilla y no invasiva de las ondas cerebrales —el electroencefalograma, o EEG— puede revelar cambios muy tempranos en la función cerebral y pronosticar de forma fiable quién tiene mayor probabilidad de experimentar un deterioro cognitivo grave años más tarde.
Escuchando las señales silenciosas del cerebro
Los investigadores se centraron en personas con “deterioro cognitivo subjetivo” (DCS): adultos mayores que perciben que su memoria falla pero que aún rinden de forma normal en las pruebas estándar. Ochenta y ocho voluntarios de entre 52 y 85 años tuvieron 20 minutos de EEG en reposo registrados con los ojos cerrados, y fueron seguidos durante 5–7 años. Durante el seguimiento, los médicos monitorizaron el estado cognitivo de cada persona usando escalas establecidas. Al final de este periodo, algunos participantes se mantuvieron estables, mientras que otros pasaron a deterioro cognitivo leve o desarrollaron demencia. Estos desenlaces permitieron al equipo plantearse si patrones sutiles en el EEG inicial podrían haber predicho quién empeoraría posteriormente.
Convirtiendo las ondas cerebrales en una huella predictiva
En lugar de inspeccionar el EEG a simple vista, el equipo empleó EEG cuantitativo (qEEG), que transforma las ondas cerebrales crudas en miles de características numéricas. Estas características capturan la potencia de distintas bandas de frecuencia (como los ritmos alfa y theta), cómo se sincronizan regiones cerebrales distantes entre sí (conectividad y desfase de fase), y cuán complejo o desorganizado parece el patrón de actividad general. Dado que el envejecimiento normal también altera el EEG, los investigadores ajustaron matemáticamente todas las características por edad y luego las estandarizaron de modo que “cero” representara el valor esperado para una persona sana de la misma edad. Para evitar sobreajuste, redujeron sistemáticamente más de 6.000 medidas candidatas a un conjunto compacto de características estables, no redundantes y con mejor capacidad para separar a quienes permanecerían estables de quienes empeorarían.
El aprendizaje automático como bola de cristal
Con este conjunto reducido de características, el equipo entrenó varios modelos de aprendizaje automático —regresión logística, máquinas de vectores de soporte y bosques aleatorios— para estimar la probabilidad de cada participante de sufrir un deterioro futuro. Se emplearon validación cruzada repetida y un método bootstrap especializado para evaluar el rendimiento de la forma más realista posible. Entre los modelos, la precisión predictiva fue de alrededor del 80%, con un área bajo la curva ROC (AUC) cercana a 0,90, lo que indica una fuerte discriminación entre individuos estables y en declive. Los modelos finales bloqueados usaron solo 14 características de qEEG, en su mayoría procedentes de regiones frontales registradas con un pequeño conjunto de electrodos, lo que hace que el enfoque sea práctico para su uso clínico rutinario.
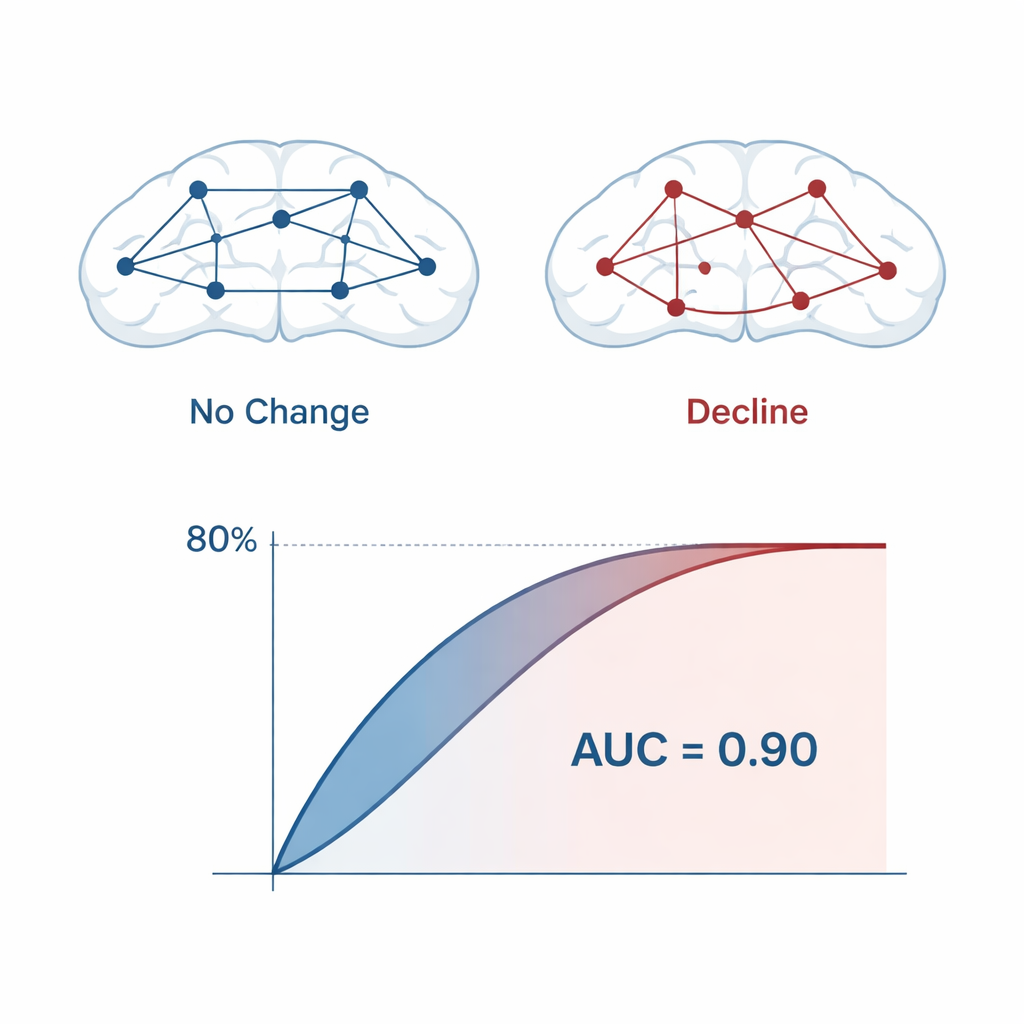
Qué está cambiando en el cerebro
Las características más responsables de la predicción precisa apuntaron a una alteración temprana en cómo las áreas cerebrales se comunican entre sí. Las medidas de conectividad, especialmente el desfase de fase y la asimetría entre regiones frontales izquierda y derecha, fueron centrales en el modelo. Destacaron anormalidades en las bandas de frecuencia alfa y theta: un incremento o desplazamiento de la actividad theta se ha relacionado en otras investigaciones con atrofia hipocampal y adelgazamiento cortical, mientras que cambios en la potencia y la frecuencia alfa pueden reflejar los intentos iniciales del cerebro por compensar el daño emergente. Es importante destacar que ninguna medida de EEG por sí sola contaba toda la historia. Fue la combinación específica —la “huella” del biomarcador— la que señalaba un riesgo elevado años antes de que surgieran los síntomas completos.
Poniendo la herramienta a prueba en el mundo real
Para ver si su biomarcador se generalizaba más allá del grupo original, los investigadores lo probaron en dos cohortes independientes de Estados Unidos e Italia, cada una con sus propios equipos de registro y características de los pacientes. Como era de esperar para datos verdaderamente nuevos, la precisión cayó modestamente, hasta aproximadamente 60–70%, pero el modelo siguió rindiendo muy por encima del azar, lo que sugiere que la señal que captura es robusta. El equipo también mostró que los clínicos pueden ajustar el umbral de decisión: bajarlo aumenta la sensibilidad (captando a más futuros declinantes a costa de más falsas alarmas), mientras que subirlo aumenta la especificidad (menos falsos positivos pero más casos perdidos). Esta flexibilidad permite a los proveedores adaptar la herramienta a diferentes prioridades clínicas.
Qué significa esto para pacientes y clínicos
En términos sencillos, este trabajo sugiere que una grabación EEG corta e indolora —usando solo un puñado de electrodos sobre la frente— puede ayudar a identificar a adultos mayores que hoy parecen normales pero que tienen alto riesgo de deterioro cognitivo en los próximos años. Aunque hacen falta estudios mayores y comparaciones con otros biomarcadores, el enfoque es barato, no invasivo y repetible, lo que lo hace atractivo para el cribado generalizado, especialmente en entornos donde las técnicas avanzadas de imagen o las pruebas de líquido cefalorraquídeo son impracticables. Si se valida más, estos biomarcadores basados en EEG podrían ayudar a los médicos a intervenir antes, monitorizar la progresión de la enfermedad y seleccionar participantes para ensayos clínicos en la fase en que los tratamientos tienen más probabilidades de lograr un impacto duradero.
Cita: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Palabras clave: predicción temprana de demencia, ondas cerebrales EEG, deterioro cognitivo subjetivo, biomarcador mediante aprendizaje automático, riesgo de Alzheimer