Clear Sky Science · es
Clasificación de leucocitos mediante una red neuronal profunda personalizada y visualización de las características de las imágenes mediante mapas de calor
Por qué importan las pruebas de sangre más inteligentes
Un análisis de sangre de rutina puede revelar signos tempranos de infección, alergia o incluso cáncer, pero hoy en día gran parte de esa información todavía depende de que expertos inspeccionen cuidadosamente las células bajo un microscopio. Este proceso es lento, costoso y no siempre está disponible en clínicas pequeñas u hospitales rurales. El trabajo descrito aquí presenta un sistema compacto de inteligencia artificial capaz de reconocer con precisión distintos tipos de glóbulos blancos a partir de imágenes de microscopio, lo que podría llevar análisis de sangre más rápidos y fiables a muchos más pacientes.
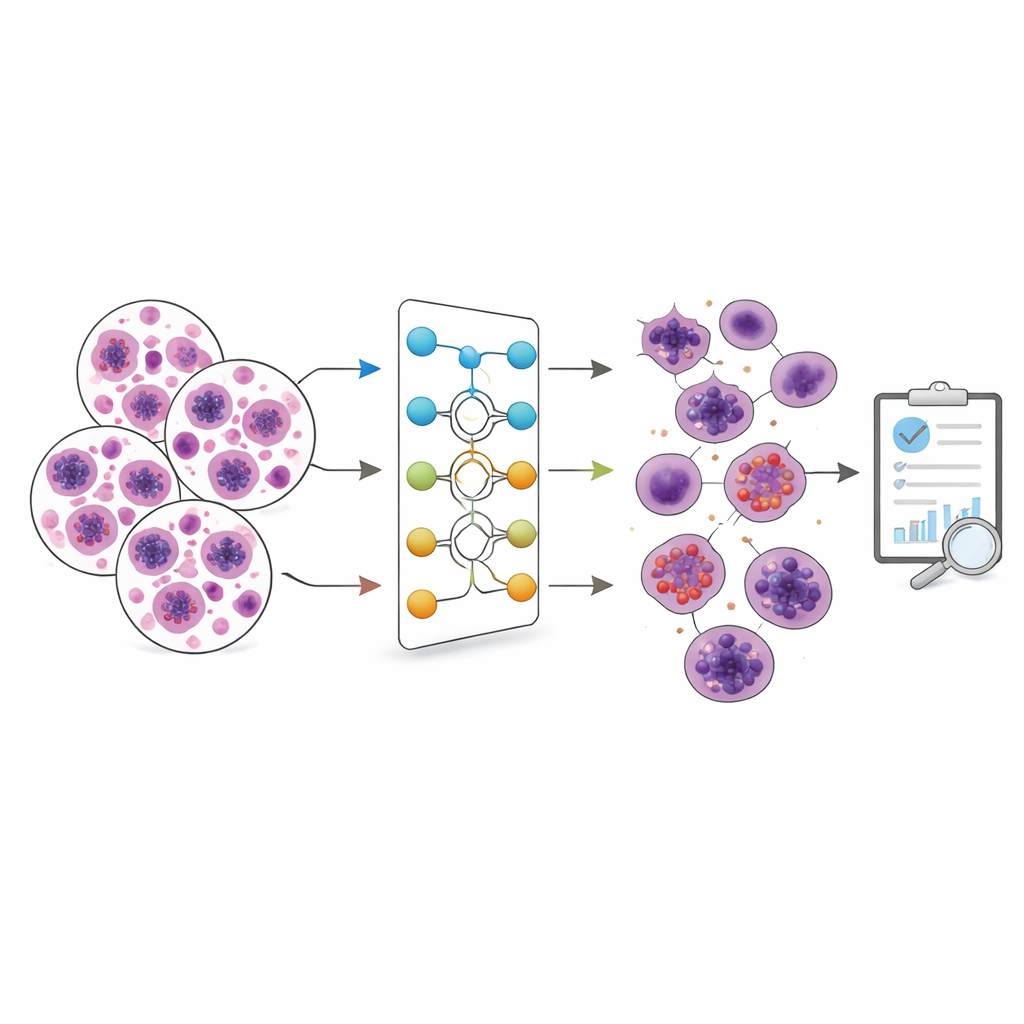
Los pequeños defensores del cuerpo
Los glóbulos blancos son los defensores de primera línea del cuerpo contra gérmenes y otras amenazas. Existen varias variedades principales, cada una con una función distinta: algunas atacan bacterias, otras combaten parásitos, responden a alergias o ayudan a coordinar la inmunidad a largo plazo. Los médicos suelen observar tanto el número como el tipo de estas células para diagnosticar enfermedades y monitorizar tratamientos. Hoy en día esto se hace comúnmente bien mediante el recuento manual bajo microscopio —una tarea que requiere habilidad y lleva tiempo— o mediante grandes máquinas automatizadas que muchos laboratorios pequeños no pueden costear.
Del recuento manual a ojos digitales
Durante la última década, los investigadores han recurrido a la visión por computador y al aprendizaje automático para ayudar a automatizar la identificación de glóbulos blancos. Los programas básicos pueden medir formas y colores, mientras que sistemas más avanzados usan aprendizaje profundo, que aprende patrones complejos directamente de las imágenes. Sin embargo, muchos modelos potentes de aprendizaje profundo son enormes, necesitan gran potencia de cálculo y memoria, y pueden sufrir problemas de entrenamiento como el desvanecimiento de las señales dentro de la red. Esto limita su uso en clínicas pequeñas, dispositivos móviles de salud o hospitales con recursos informáticos modestos.
Un microscopio digital ligero pero potente
Los autores presentan un modelo de aprendizaje profundo optimizado al que llaman red neuronal profunda personalizada, o CDNN. Está diseñado específicamente para reconocer glóbulos blancos en imágenes de microscopio. El modelo se entrenó y evaluó en dos conjuntos de datos populares de imágenes de células sanguíneas: uno grande y algo desequilibrado (Raabin WBC) con cinco tipos de glóbulos blancos, y otro más pequeño pero equilibrado (BCCD) con cuatro tipos. Antes del entrenamiento, todas las imágenes se redimensionaron, se normalizó su nivel de brillo y se alteraron ligeramente —rotadas, reflejadas y sesgadas— para imitar la variación natural y reducir el sobreajuste, que ocurre cuando un modelo memoriza ejemplos de entrenamiento en lugar de aprender patrones generales.
Dentro del “proceso de pensamiento” del modelo
CDNN se construye a partir de una serie de bloques que le ayudan a aprender de forma efectiva manteniéndolo compacto. Estos bloques incluyen conexiones “residuales” que permiten que la información omita algunas capas, evitando que las señales de entrenamiento se desvanezcan al cruzar la red. El modelo incrementa gradualmente el número de filtros internos a medida que las imágenes avanzan por él, capturando tanto detalles finos como formas más amplias del núcleo celular y del material circundante. A pesar de tener muchos menos parámetros ajustables que modelos de imagen conocidos como VGG16 o ResNet-50, CDNN alcanza una precisión muy alta: alrededor del 98 % en el conjunto Raabin y casi el 99,6 % en el conjunto BCCD, superando a muchos métodos modernos más grandes.
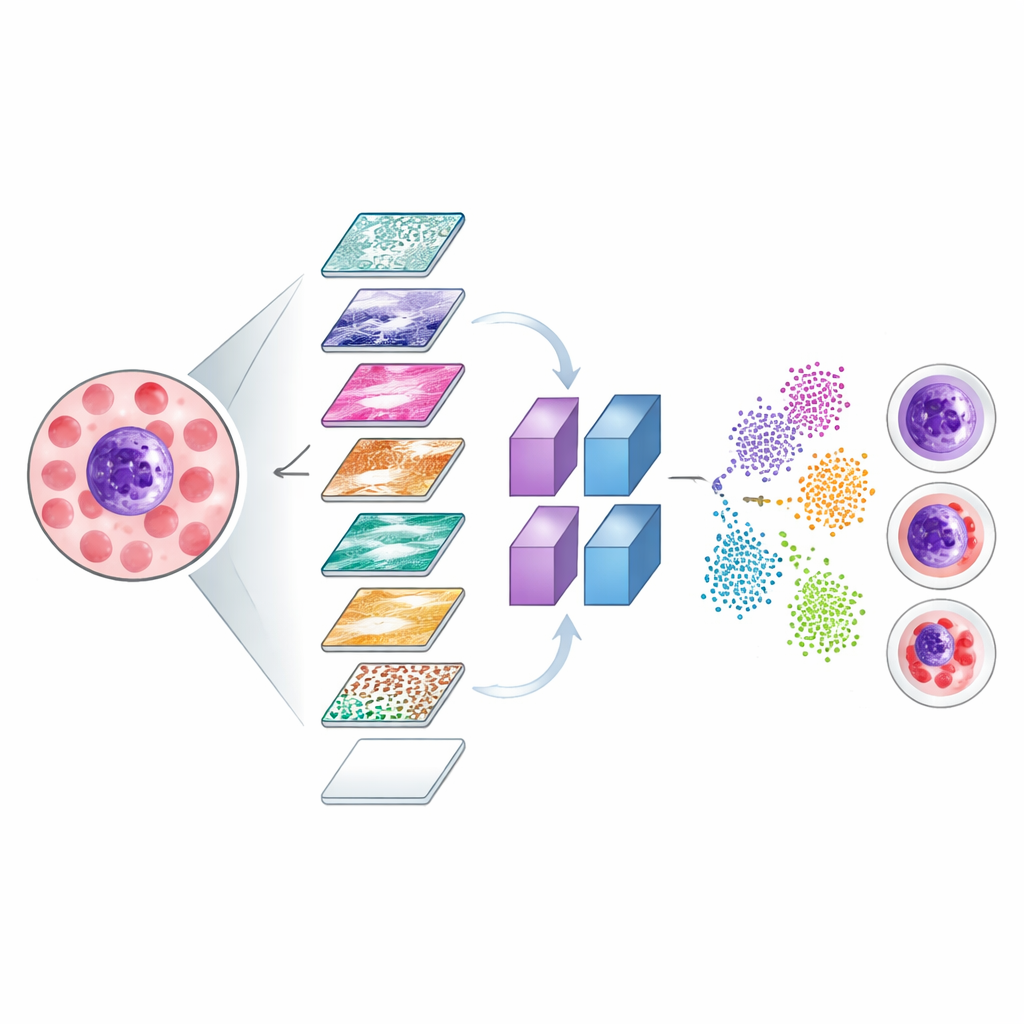
Haciendo visibles las decisiones invisibles
Para asegurar que el sistema se centre en partes de las imágenes con significado médico, los investigadores emplearon dos herramientas de visualización, conocidas como Grad-CAM y LIME. Estos métodos generan mapas de calor en color que resaltan qué regiones de una imagen celular influyeron con mayor fuerza en las decisiones del modelo. Las zonas brillantes en estos mapas tendieron a alinearse con estructuras esenciales como el núcleo de la célula y el citoplasma circundante, más que con el fondo irrelevante. El equipo también examinó cómo la red separa internamente los distintos tipos celulares proyectando sus señales internas en un mapa bidimensional, donde las células correctamente clasificadas forman agrupaciones claras y los casos mal clasificados pueden inspeccionarse para entender dónde falla el modelo.
Qué podría suponer esto para los pacientes
En términos sencillos, este trabajo demuestra que un modelo de IA diseñado con cuidado y relativamente pequeño puede clasificar glóbulos blancos en imágenes de microscopio con una precisión comparable o superior a la de muchos sistemas grandes y complejos. Debido a que el modelo es compacto y eficiente, resulta más adecuado para su uso en laboratorios pequeños, dispositivos de punto de atención o incluso equipos portátiles, lo que podría acercar análisis de sangre de alta calidad a los pacientes. Aunque aún se necesitan más pruebas en entornos clínicos reales, este enfoque apunta hacia herramientas más rápidas, accesibles y transparentes que pueden ayudar a los patólogos a diagnosticar enfermedades y detectar problemas antes.
Cita: Karaddi, S.H., Bitra, H., Bairaboina, S.S.R. et al. White blood cell classification using custom deep neural network and visualizing features of the images using heatmaps. Sci Rep 16, 9311 (2026). https://doi.org/10.1038/s41598-026-35138-9
Palabras clave: glóbulos blancos, imagen médica, aprendizaje profundo, diagnóstico sanguíneo, redes neuronales