Clear Sky Science · es
Diseño y análisis de rendimiento de un FET nanosheet de puerta envolvente apilada verticalmente con nanocavidad integrada para aplicaciones de biosensado
Sensores más pequeños para advertencias más tempranas
Detectar el cáncer en sus etapas iniciales suele depender de la rapidez y la precisión con que podamos identificar trazas diminutas de la enfermedad en la sangre u otros fluidos corporales. Este artículo explora un nuevo tipo de sensor electrónico ultrasmall—construido con la misma tecnología que se emplea en chips de ordenador avanzados—que puede detectar moléculas relacionadas con el cáncer con una sensibilidad muy superior a la de muchos dispositivos existentes, y consumiendo muy poca energía.
Convertir un transistor en un detector de cáncer
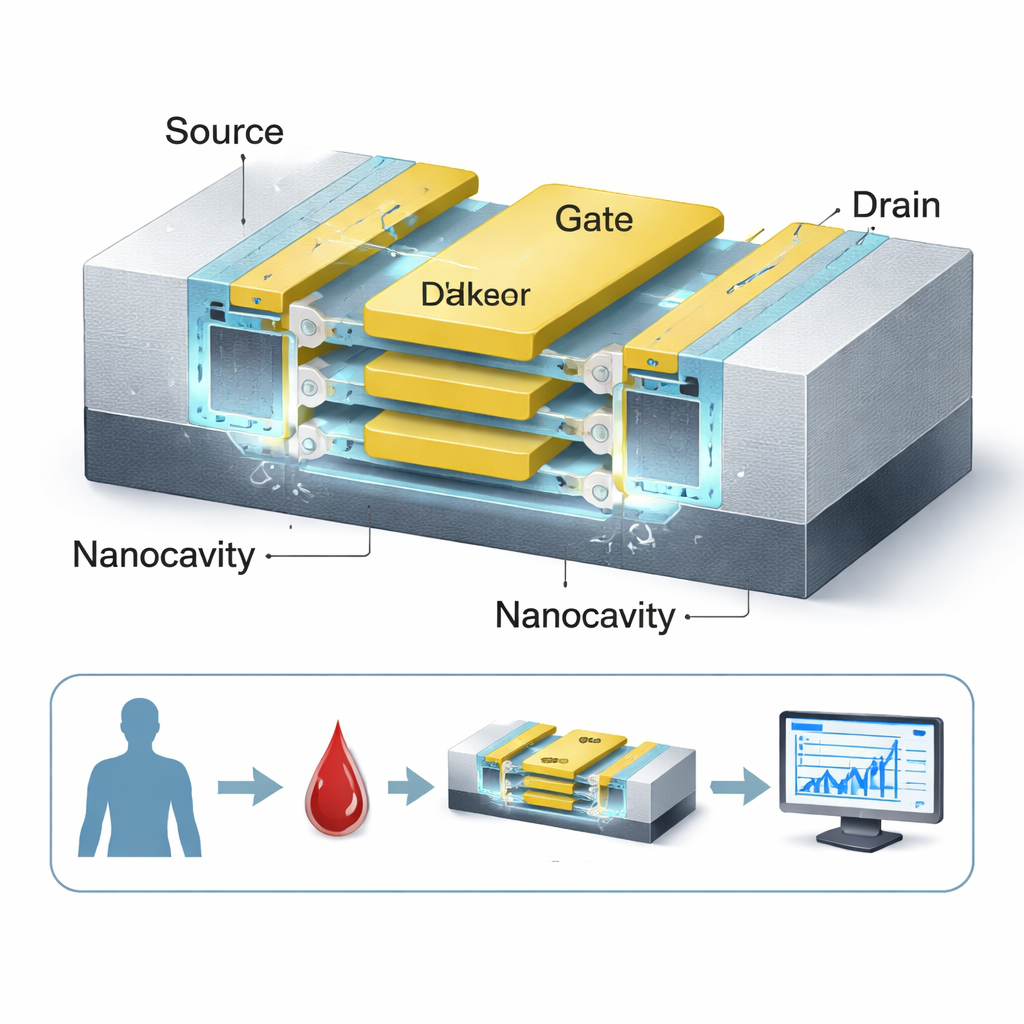
En el centro del trabajo está un transistor rediseñado, el elemento básico de conmutación en electrónica. Los autores parten de un estilo de dispositivo de vanguardia llamado FET nanosheet, ya adoptado por grandes fabricantes de chips para procesos de 3 nm. Lo reutilizan como biosensor excavando pequeñas cavidades huecas, o nanocavidades, alrededor de la puerta aislada que controla el flujo de corriente. Cuando biomoléculas vinculadas al cáncer—como células de tumores colorrectales o renales, hebras de ADN o proteínas gelatinosas—se depositan en estas cavidades, cambian sutilmente cómo se mueve la carga eléctrica dentro del dispositivo. El transistor “percibe” ese cambio como un desplazamiento en la corriente, convirtiendo un evento bioquímico en una señal eléctrica medible.
Apilar capas para señales más fuertes
Una innovación clave en el diseño es que el canal sensor no es un único hilo sino tres láminas de silicio ultrafinas apiladas verticalmente, todas rodeadas por una puerta común. Esta estructura de puerta envolvente otorga a la puerta un control mucho más estricto sobre el canal que en los transistores planos tradicionales, lo que agudiza la conmutación encendido/apagado del dispositivo y aumenta el cambio medible cuando hay biomoléculas presentes. Dos nanocavidades se sitúan a ambos lados de una capa aislante de alto k (HfO₂), maximizando la región donde las moléculas pueden interactuar con el campo eléctrico. Dado que el canal es «sin dopado», es decir, evita impurezas químicas intensas, la respuesta del sensor es más uniforme y menos vulnerable a variaciones de fabricación—una ventaja para pruebas médicas fiables.
Ajusatar pequeñas cavidades para máxima respuesta
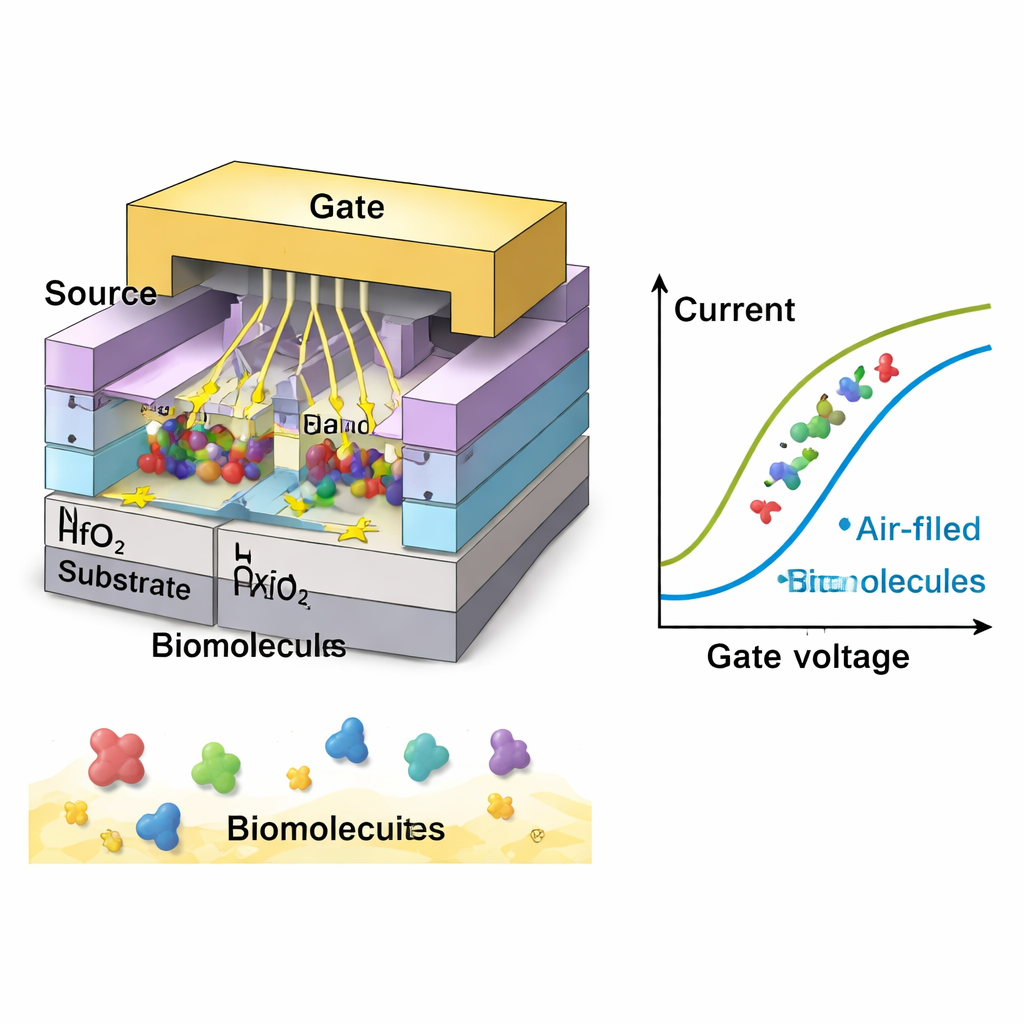
Usando simulaciones por ordenador detalladas (TCAD), los investigadores ajustan sistemáticamente la geometría de las cavidades: su longitud, espesor y el grado en que están llenas de moléculas. Cavidades más cortas y delgadas acercan la puerta y el canal en términos electrostáticos, incrementando la corriente en encendido y reduciendo lo que se conoce como subthreshold swing—una medida de cuán bruscamente se activa el dispositivo. En su diseño óptimo, el sensor alcanza un swing sorprendentemente bajo de unos 28 milivoltios por década, muy por debajo del límite de 60 mV/dec de los transistores estándar. Esto significa que el dispositivo reacciona fuertemente a cambios de voltaje muy pequeños, una cualidad crucial para detectar concentraciones bajas de biomoléculas. También muestran que conforme se ocupa más volumen de la cavidad—o cuando las moléculas se sitúan más cerca del punto donde comienza la corriente—la señal se hace más fuerte, lo que aclara cómo la aglomeración y la colocación de los objetivos afectan el rendimiento.
Leer pistas de cáncer en señales eléctricas
El equipo explora luego cómo se verían eléctricamente distintos tipos de biomoléculas. Especies neutras con mayor permitividad inherente (una propiedad eléctrica relacionada con cómo se polarizan en un campo) conducen a cambios de corriente mayores y mejor sensibilidad, con la respuesta más intensa en un valor típico de la gelatina y algunos tejidos biológicos densos. Las moléculas cargadas, como el ADN o ciertas superficies celulares, pueden potenciar aún más la señal. En las simulaciones, las biomoléculas con carga negativa producen el mayor desplazamiento de corriente, seguidas por las cargas positivas y luego las neutras. En condiciones óptimas, el dispositivo logra una sensibilidad de corriente más de 3.000 veces superior a su nivel base y más de 9.000 para cargas fuertemente negativas—superando a varios biosensores previos basados en nanosheet. El sensor también muestra tiempos de respuesta rápidos, operación estable cerca de la temperatura ambiente y buena especificidad, lo que significa que puede distinguir moléculas objetivo de otras similares no deseadas.
Hacia pruebas prácticas de cáncer a nivel de chip
Para asegurar que este concepto es realista, los autores describen un flujo de fabricación que sigue de cerca la manufactura avanzada de chips actual, usando sustratos estándar de silicio sobre aislante (SOI), capas conocidas de óxidos y metales, y pasos de grabado comunes para formar las nanocavidades. Porque la estructura se mantiene compacta y compatible con procesos CMOS convencionales, podría, en principio, integrarse en matrices densas sobre un único chip. Para el lector no especializado, la conclusión es que este trabajo acerca los biosensores basados en transistores a dispositivos prácticos tipo laboratorio en un chip que podrían, algún día, detectar marcadores de cáncer de forma rápida, con alta sensibilidad y sin necesidad de etiquetas o química compleja, empleando tecnología muy similar a la que ya impulsa la electrónica moderna.
Cita: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Palabras clave: biosensor de cáncer, FET nanosheet, laboratorio en un chip, sensor de nanocavidad, detección temprana