Clear Sky Science · es
La fosfatasa de doble especificidad 6 interfiere con la actividad represora del factor forkhead box O1 sobre CYP4A11 que media la acumulación de lípidos en el hígado
Por qué importa la grasa en el hígado
El exceso de grasa en el hígado, a menudo llamado enfermedad del hígado graso, es cada vez más común con las dietas modernas ricas en azúcar y grasa. Aunque mucha gente ha oído hablar del colesterol o de la glucemia, son menos los que saben que diminutos interruptores moleculares dentro de las células hepáticas ayudan a decidir si la grasa se quema o se almacena. Este estudio analiza tres de esos interruptores: proteínas llamadas DUSP6, FOXO1 y CYP4A11, y revela cómo su tira y afloja puede empujar a las células hepáticas hacia el almacenamiento excesivo de grasa. Entender este sistema de control oculto podría señalar nuevas vías de tratamiento para la enfermedad del hígado graso y problemas metabólicos relacionados.
Un controlador de tráfico oculto dentro de las células hepáticas
Los investigadores se centraron en una proteína llamada DUSP6, conocida principalmente por apagar una vía de señalización celular llamada vía ERK. Trabajos anteriores mostraron que ratones carentes de DUSP6 eran sorprendentemente resistentes al hígado graso inducido por la dieta, y sus hígados presentaban niveles más bajos de enzimas CYP4A, implicadas en el procesamiento de grasas. Aquí, el equipo se preguntó qué hace DUSP6 en células de origen humano y cómo podría afectar a una versión humana de estas enzimas llamada CYP4A11. Utilizaron dos líneas celulares estándar derivadas de cáncer hepático, HepG2 y HuH‑7, como sustitutas de células hepáticas humanas y las cargaron con una mezcla de ácidos grasos (palmitato y oleato) para imitar un entorno poco saludable y rico en grasas. 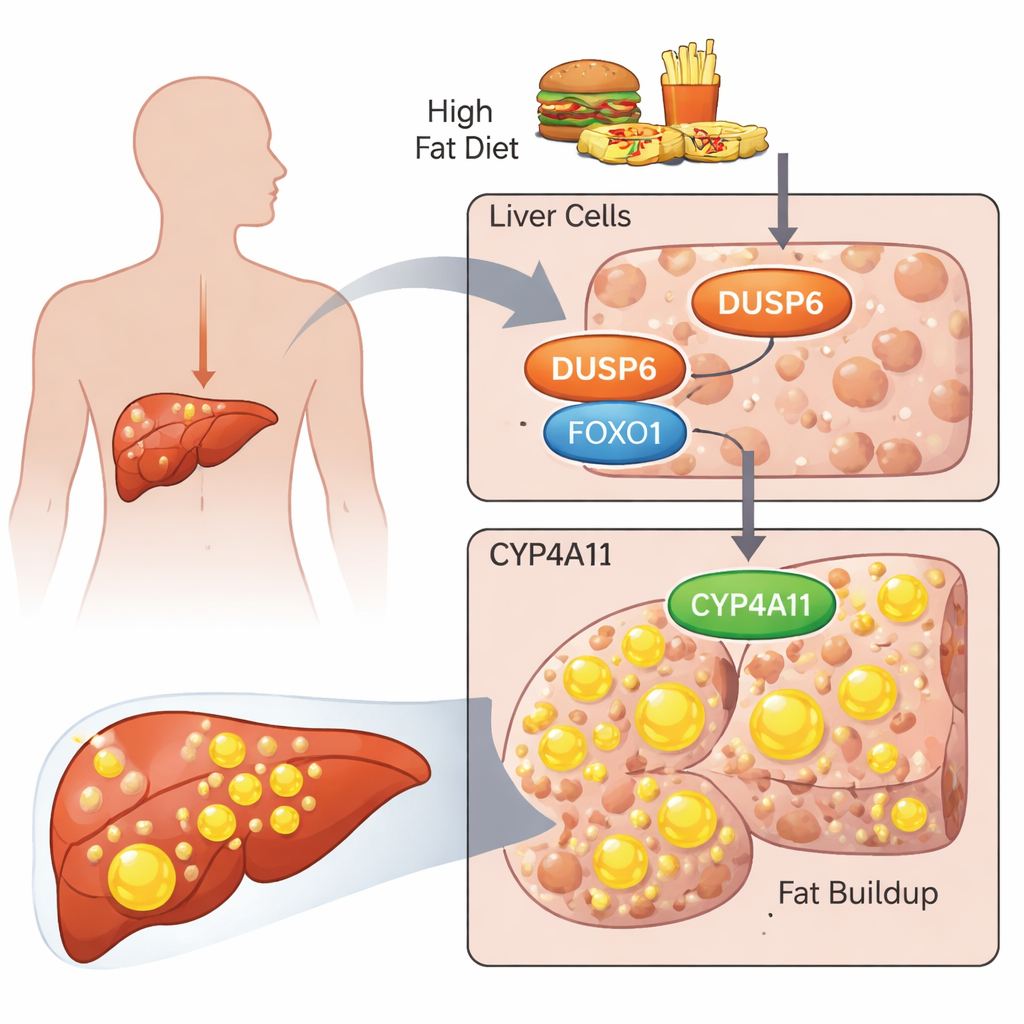
De los ácidos grasos a una célula llena de grasa
Cuando las células fueron desafiadas con estos ácidos grasos, acumularon visiblemente gotas de grasa, que los científicos tiñeron y cuantificaron. Al mismo tiempo, aumentaron los niveles de DUSP6 y CYP4A11, junto con las formas activadas de dos proteínas de señalización importantes, AKT y FOXO1. La reducción de DUSP6 mediante ARN dirigido invirtió este patrón: las células almacenaron menos grasa, los niveles de CYP4A11 disminuyeron, pero ERK, AKT y FOXO1 activados aumentaron. Bloquear solo la vía ERK empeoró en realidad la acumulación de grasa, mientras que bloquear solo AKT la redujo. Cuando se inhibieron ERK y AKT a la vez, la acumulación de grasa disminuyó y los niveles de CYP4A11 cayeron. Estos experimentos vincularon estrechamente a CYP4A11 con la cantidad de grasa acumulada y sugirieron que la actividad de AKT es especialmente importante para impulsar el almacenamiento de lípidos.
Un freno sobre genes que promueven la grasa
Otro actor clave, FOXO1, es un factor de transcripción: una proteína que puede entrar en el núcleo celular y activar o reprimir genes. Se sabe que FOXO1 actúa como un freno sobre varios miembros de la misma familia de enzimas que CYP4A11. El equipo encontró que reducir los niveles de FOXO1 hizo que las células acumularan más grasa y aumentara CYP4A11, mientras que aumentar directamente CYP4A11 hizo que las células fueran aún más grasas. En contraste, forzar a las células a producir más FOXO1 redujo tanto CYP4A11 como la acumulación de grasa. Un fármaco que bloquea la actividad de CYP4A11 (HET0016) disminuyó la grasa adicional causada por la reducción de FOXO1, lo que respalda la idea de que CYP4A11 no es solo un observador sino un impulsor de la acumulación lipídica. Pruebas químicas mostraron que HET0016 redujo 20‑HETE, un producto generado por CYP4A11 vinculado al estrés oxidativo y la inflamación, lo que relaciona aún más esta vía con el daño hepático.
Cómo DUSP6 desactiva el freno
Para entender cómo FOXO1 controla CYP4A11, los científicos examinaron la región de ADN delante del gen CYP4A11 y encontraron secuencias donde FOXO1 puede unirse. Usando un ensayo de inmunoprecipitación de cromatina, demostraron que FOXO1—específicamente su forma no fosforilada—se une directamente al promotor de CYP4A11, consistente con un papel represor sobre este gen. Experimentos de co‑inmunoprecipitación revelaron que DUSP6 interactúa físicamente con FOXO1 pero no con su versión fosforilada. Estudios de fraccionamiento y microscopía mostraron que DUSP6 se localiza en el citoplasma de la célula y, cuando está presente, mantiene a más FOXO1 fuera del núcleo. Cuando se redujo DUSP6, más FOXO1 se desplazó al núcleo, donde podía unirse al ADN y suprimir CYP4A11. En efecto, DUSP6 actúa como un ancla, secuestrando a FOXO1 en el citoplasma e impidiendo que cumpla su función de freno sobre CYP4A11. 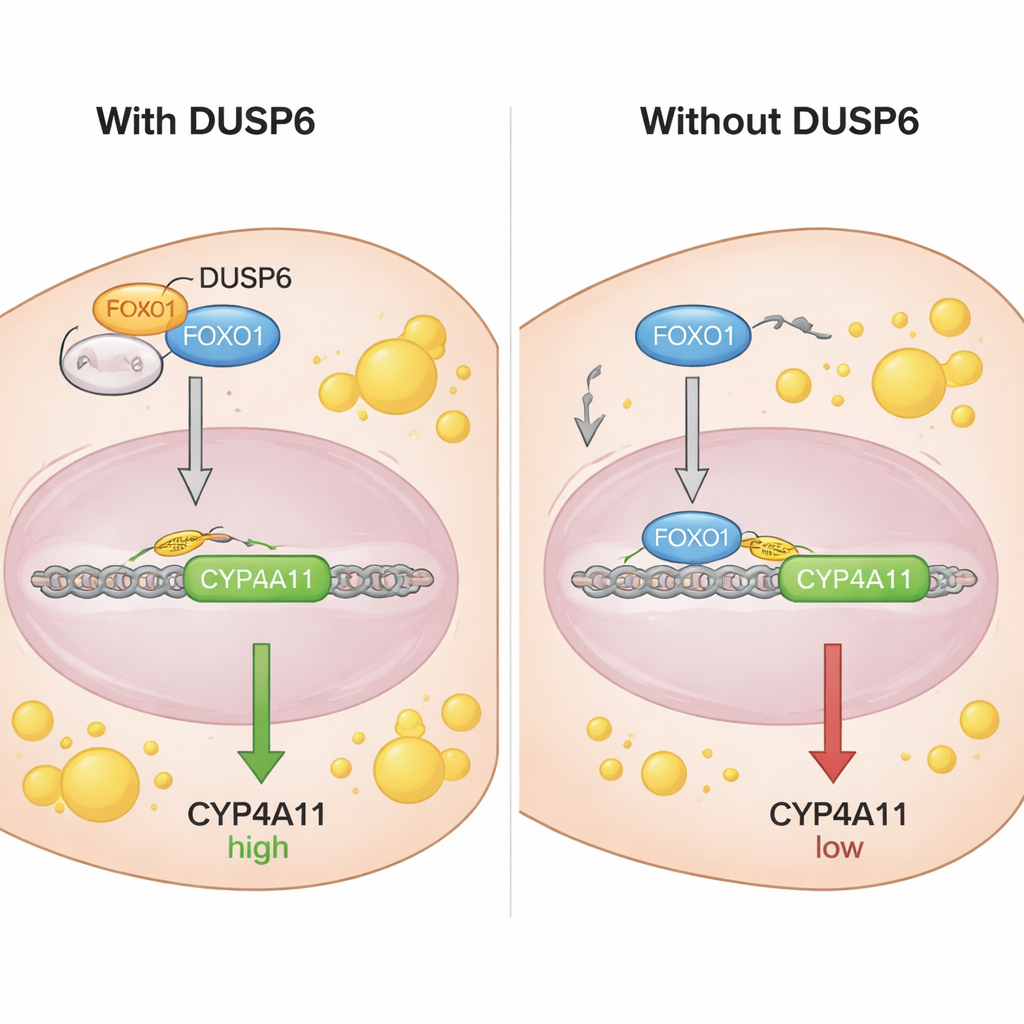
Qué significa esto para el hígado graso y más allá
En pocas palabras, este trabajo traza una cadena de eventos dentro de las células hepáticas: DUSP6 retiene a FOXO1 en el citoplasma, lo que debilita la capacidad de FOXO1 para apagar el gen CYP4A11. Con FOXO1 marginado, CYP4A11 se vuelve más activo, contribuyendo a que la célula almacene más grasa y produzca moléculas como 20‑HETE que pueden promover el estrés oxidativo y la inflamación. Aunque estos hallazgos provienen de células derivadas de hígado en cultivo y no de tejido hepático humano sano, ponen de relieve a DUSP6 y CYP4A11 como posibles nuevos objetivos para tratar la enfermedad hepática esteatósica asociada a disfunción metabólica. En teoría, terapias que reduzcan la actividad de DUSP6 o atenúen los efectos de CYP4A11 podrían restaurar la función de frenado de FOXO1 y ayudar a mantener bajo control la grasa hepática.
Cita: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Palabras clave: enfermedad del hígado graso, DUSP6, FOXO1, CYP4A11, metabolismo hepático