Clear Sky Science · es
Minería en DrugBank con aprendizaje automático revela nuevos candidatos para la inhibición de BCL-2
Por qué es importante encontrar fármacos oncológicos más inteligentes
Las células cancerosas a menudo se niegan a morir cuando deberían. Muchos tumores sobreviven abusando de una familia de proteínas “guardianas” llamadas BCL-2 que bloquean el programa de suicidio incorporado de la célula. Ya existen fármacos que apuntan a BCL-2, pero pueden causar efectos secundarios y no funcionan en todos los pacientes. Este estudio explora cómo el aprendizaje automático moderno puede cribar miles de fármacos ya existentes para hallar nuevos candidatos más seguros que podrían desactivar BCL-2 y ayudar a que las células cancerosas se autodestruyan.
Cómo las células eligen entre la vida y la muerte
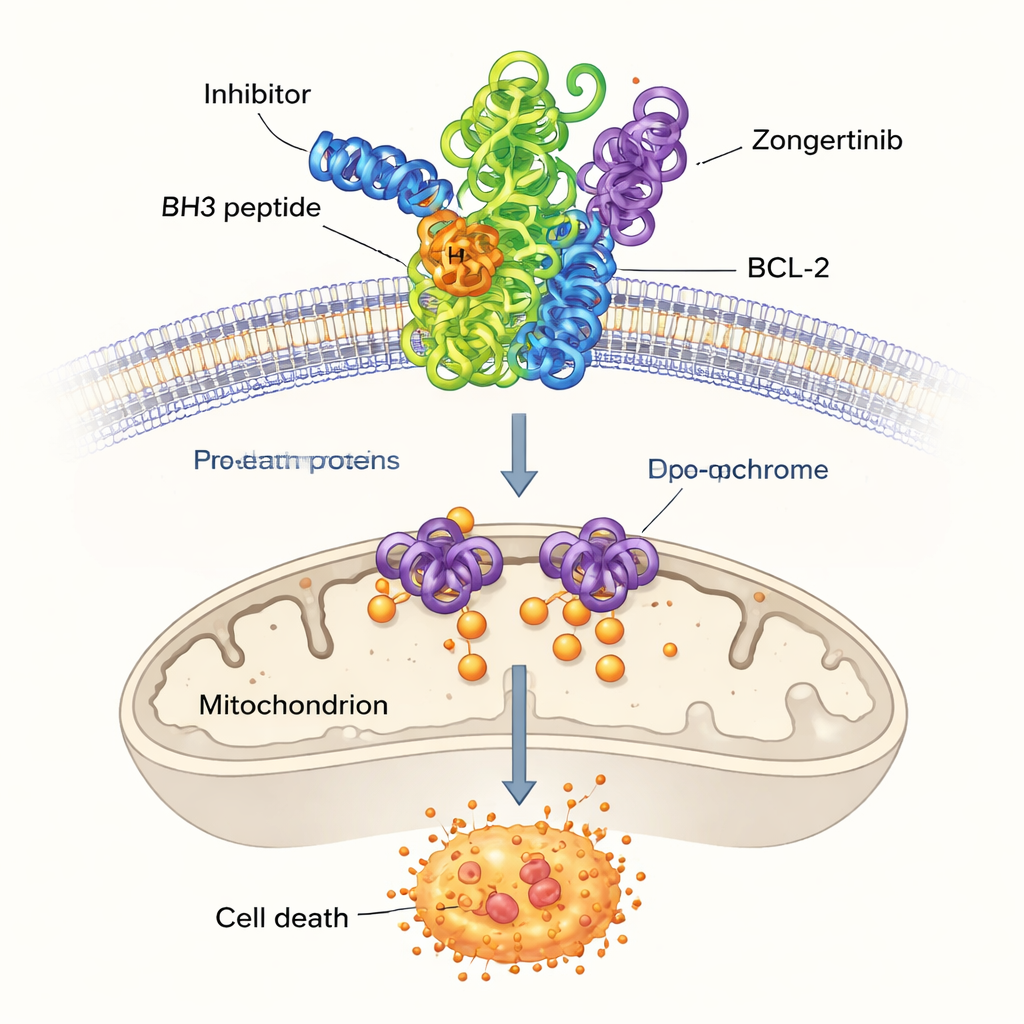
Los tejidos sanos eliminan constantemente las células dañadas o innecesarias mediante un proceso de autodestrucción controlada conocido como apoptosis, o muerte celular programada. Un grupo de proteínas llamado familia BCL-2 actúa como un interruptor central en esta decisión. Algunos miembros empujan a las células hacia la supervivencia, mientras que otros las empujan hacia la muerte. En muchos cánceres, los miembros que promueven la supervivencia, incluidos BCL-2 y su pariente cercano BCL-XL, se producen en exceso. Esta protección adicional permite a las células cancerosas ignorar las señales de muerte y resistir la quimioterapia. Por ello, bloquear BCL-2 se ha convertido en una estrategia atractiva en el tratamiento del cáncer, pero los fármacos actuales a menudo afectan también a proteínas relacionadas, lo que conduce a efectos secundarios como caídas peligrosas en el recuento de plaquetas.
Enseñar a las computadoras a reconocer moléculas prometedoras
En lugar de buscar nuevos compuestos desde cero, los investigadores recurrieron a bases de datos de moléculas que ya han sido estudiadas o usadas como fármacos. Comenzaron con un gran recurso público llamado ChEMBL, que contiene mediciones experimentales de la fuerza con la que distintos químicos se unen a BCL-2. Tras limpiar cuidadosamente esa información —eliminando duplicados, mediciones inciertas y moléculas excesivamente grandes o inusuales— obtuvieron 601 compuestos bien caracterizados. Cada molécula se tradujo en una especie de huella digital digital que captura sus rasgos estructurales. Estas huellas se usaron para entrenar y comparar siete modelos diferentes de aprendizaje automático en la tarea de decidir si una nueva molécula probablemente sería un potente bloqueador de BCL-2 o esencialmente inactiva. 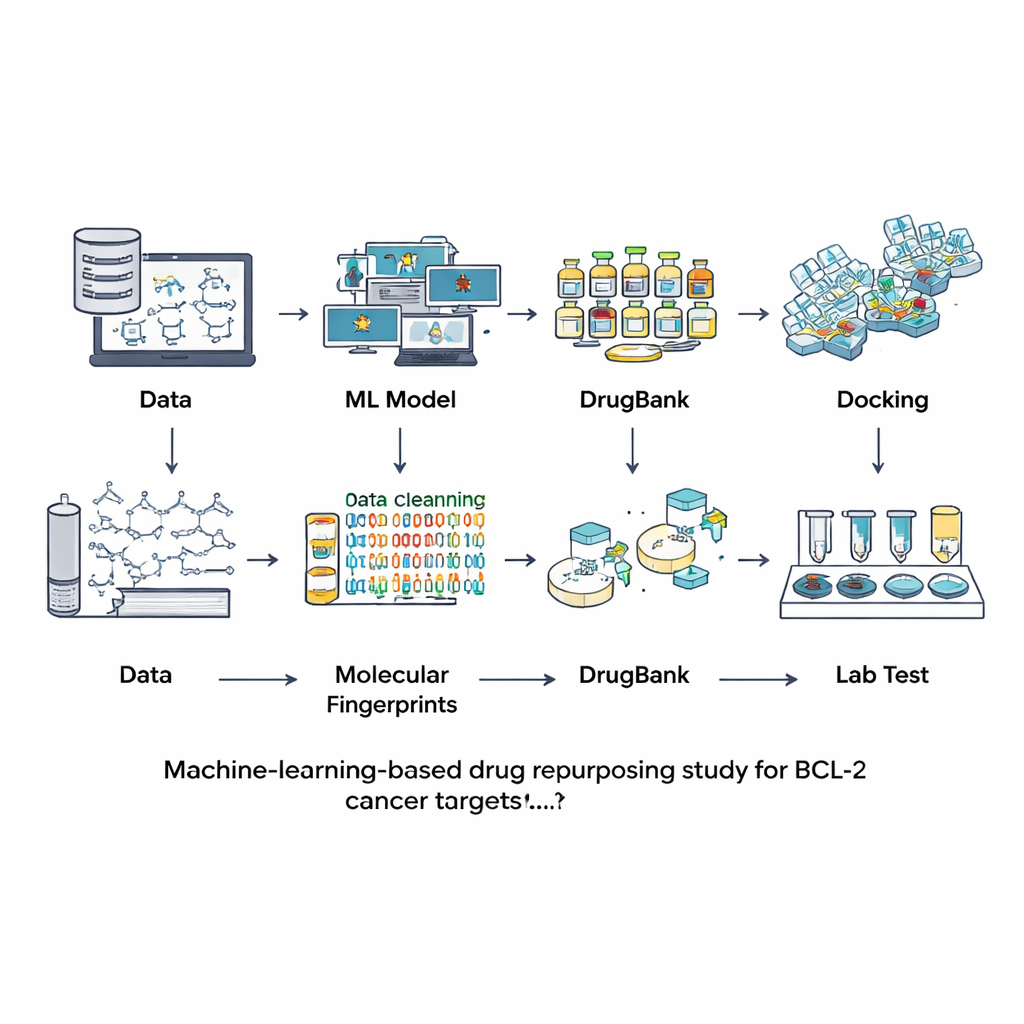
Elegir el mejor modelo y rastrear una biblioteca de fármacos
El equipo evaluó los modelos usando un conjunto de prueba independiente que no se había visto durante el entrenamiento, comprobando no solo cuántas veces acertaba cada modelo, sino también qué tan bien distinguía activos de inactivos y cuán equilibradas eran sus predicciones. Un modelo llamado LightGBM —un método moderno de boosting basado en árboles— fue el que mejor desempeño mostró en la mayoría de las métricas, incluida la precisión global y su capacidad para asignar probabilidades fiables. Con este modelo ajustado, los investigadores se dirigieron a DrugBank, una colección curada de más de 12.000 fármacos aprobados, experimentales y retirados. Tras calcular el mismo tipo de huellas, preguntaron a LightGBM cuáles de estas moléculas parecían potenciales inhibidores de BCL-2. Solo nueve compuestos obtuvieron puntuaciones altas, aproximadamente la décima parte de un uno por ciento de toda la biblioteca, lo que muestra que la búsqueda virtual fue muy selectiva. Cuatro de esos nueve ya eran inhibidores conocidos de BCL-2, lo que tranquilizó al equipo sobre la solidez del enfoque.
De los aciertos informáticos a las interacciones moleculares
Entre las restantes moléculas con puntuaciones altas, los investigadores se centraron en tres no vinculadas previamente a BCL-2: Dersalazina, Opelconazol y Zongertinib. Para ver si estos candidatos podían encajar plausiblemente en el bolsillo de unión de BCL-2, usaron acoplamiento por computadora (docking), una técnica que predice cómo una pequeña molécula podría alojarse en la superficie de la proteína. Las simulaciones sugirieron que Opelconazol y Zongertinib, en particular, forman redes de contactos favorables con los mismos aminoácidos clave que se unen a un fármaco de referencia bien estudiado, ABT-737. Sus fuerzas de unión predichas se acercaban a las de los inhibidores establecidos, lo que insinúa que el modelo de aprendizaje automático había descubierto moléculas capaces de desactivar BCL-2.
Poner las predicciones a prueba en el laboratorio
Las pistas computacionales solo son útiles si se mantienen en condiciones reales. Por ello, el equipo probó los tres candidatos en un ensayo bioquímico que mide qué tan bien un compuesto puede impedir que BCL-2 se una a uno de sus socios naturales. En un rango de concentraciones, Dersalazina mostró poco efecto. Opelconazol y Zongertinib, sin embargo, redujeron la actividad de BCL-2 a dosis altas, con Opelconazol casi suprimiendo la señal. Aunque estas concentraciones son más altas de lo que sería ideal para un fármaco listo para clínica, demuestran que los candidatos interactúan realmente con BCL-2 y validan la canalización completa de descubrimiento.
Qué significa esto para las futuras terapias contra el cáncer
Para un público no especializado, el mensaje clave es que los investigadores entrenaron con éxito a un sistema informático para reconocer cómo “se parece” una molécula que bloquea BCL-2, y luego lo usaron para explotar una gran biblioteca de fármacos y compuestos afines. El enfoque redescubrió fármacos conocidos contra BCL-2 y resaltó nuevos candidatos, dos de los cuales mostraron actividad inhibitoria real en pruebas de laboratorio. Aunque queda mucho trabajo por delante —mejorar la potencia, estudiar la seguridad y probar en células y animales— este estudio muestra cómo el aprendizaje automático y la curación inteligente de datos pueden acelerar la búsqueda de mejores medicamentos contra el cáncer reciclando y revaluando compuestos que ya conocemos.
Cita: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Palabras clave: Inhibidores de BCL-2, aprendizaje automático, reposicionamiento de fármacos, apoptosis, terapia contra el cáncer